Clear Sky Science · sv
Ett syntetiskt system för RNA‑känslig pyroptos baserat på typ III‑E CRISPR nukleas‑proteas
Förvandla dödliga cellexplosioner till riktade verktyg
Våra kroppar försvarar sig ibland genom att få infekterade eller skadade celler att explodera i en inflammatorisk självdestruktion. Denna urladdning tar inte bara bort farliga celler utan lockar också immunsystemet. Den nya studien introducerar en syntetisk genkrets, kallad DAMAGE, som kan läsa RNA‑meddelanden inne i en cell och avgöra om den cellen bör förstöras. Genom att koppla ett mikrobiellt försvarssystem till vår egen celldöds‑maskineri visar forskarna ett sätt att selektivt utplåna virusinfekterade, cancerösa eller åldrade celler samtidigt som friska grannar sparas. 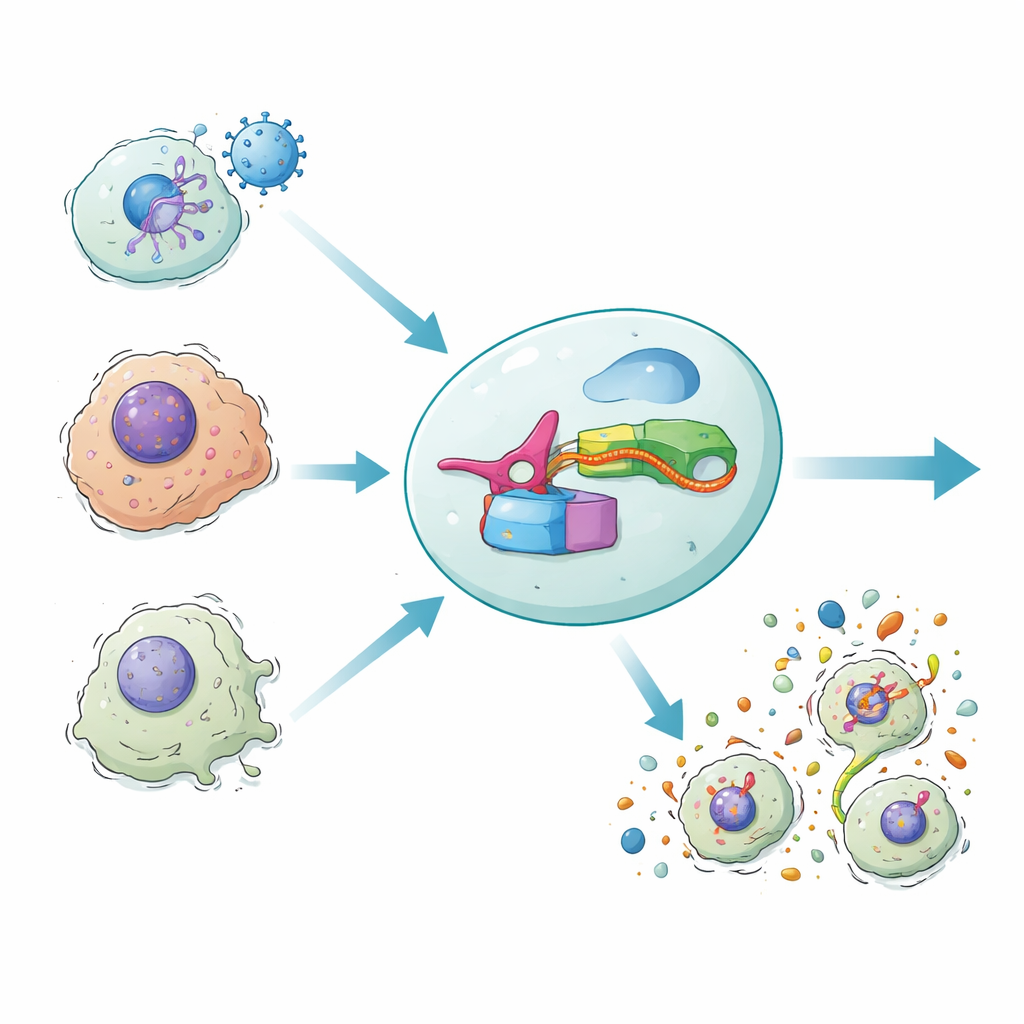
Hur celler normalt spränger sig själva
Vid inflammatorisk celldöd sitter en familj proteiner kallade gasderminer inne i cellerna som laddade sprängladdningar. Varje gasdermin har en ”dödlig” främre halva som kan göra hål i cellmembran och en bakre halva som fungerar som en ”säkerhetskåpa” som håller den dödliga delen i schack. När immunsensorer upptäcker fara klipper enzymer gasderminer i två delar, vilket frigör den främre halvan så att den kan sätta ihop porer i yttre membranet. Cellen sväller, sprängs och spyr ut larmmolekyler som samlar immunceller. Detta kraftfulla svar hjälper till att bekämpa infektioner och tumörer, men dess naturliga kontrollnätverk är invecklat och svårt att omskapa för terapi.
Låna bakterie‑försvar för att läsa RNA
Bakterier har utvecklat kompakta försvarsenheter som idag är kända genom CRISPR‑teknologi. Ett av dessa system, typ III‑E, använder ett protein kallat Cas7‑11 som kan fästa vid specifika RNA‑sekvenser med hjälp av ett kort guide‑RNA. När Cas7‑11 hittar ett matchande mål‑RNA slår det på ett följeslagarenzym, Csx29, som klipper ett partnerprotein, Csx30. Författarna insåg att Csx30 skulle kunna fungera som ett anpassningsbart ”gångjärn” mellan två proteinbitar. De fäste detta gångjärn mellan den dödliga och säkerhets‑halvan av mänskliga gasderminer och skapade artificiella utförare som endast delas när den CRISPR‑liknande sensorn upptäcker sitt valda RNA inne i en cell.
En programmerbar dödsknapp för sjuka celler
Denna konstruktion, kallad DAMAGE (för Death Manipulation Gene), byggs av fem delar: Cas7‑11‑sensorn, Csx29‑klipparen, en gasdermin–Csx30‑fusionsprotein, ett guide‑RNA och det mål‑RNA som finns i cellen. När rätt RNA‑meddelande dyker upp binder Cas7‑11 det, aktiverar Csx29, och Csx29 skär Csx30‑gångjärnet i fusionsproteinet. Gasderminets dödliga halva frigörs, borrar porer i membranet och cellen dör i en inflammatorisk explosion. Genom att enkelt byta guide‑RNA styrde teamet DAMAGE mot olika cellulära mål. De visade att det kunde känna igen RNA från respiratoriskt syncytialvirus, hög‑risk humant papillomvirus i cervixcancerceller och flera cancerdrivande KRAS‑mutationer som skiljer sig från normalt RNA med endast en enstaka nukleotid. I varje fall elimin erades celler som bar det misstänkta RNA:t selektivt, medan närliggande kontrollceller förblev intakta. 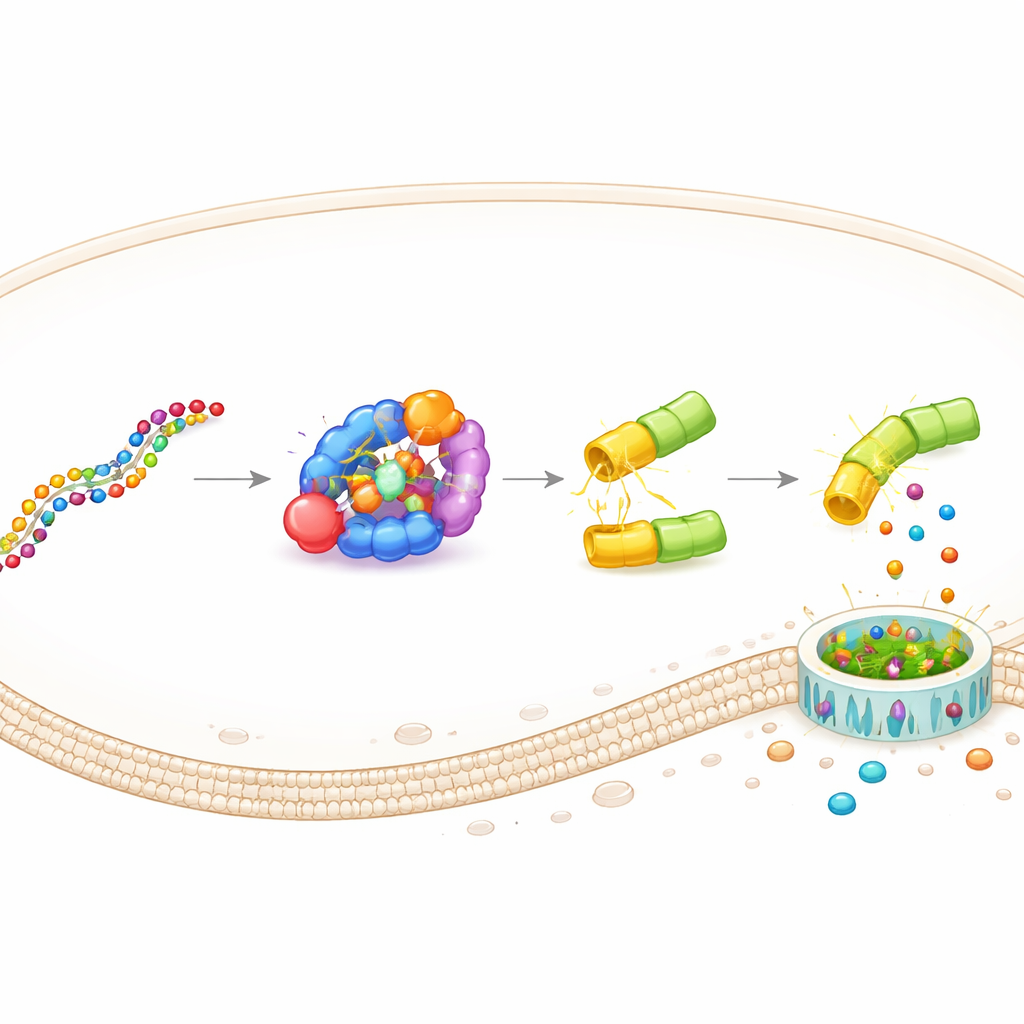
Rikta in sig på åldrande celler
Forskarna undersökte också om DAMAGE kunde jaga senescenta celler—åldrade eller stressade celler som slutat dela sig men ackumuleras i vävnader och bidrar till skörhet och kronisk sjukdom. Sådana celler ökar ofta produktionen av två grindvakter, p16 och p21. Genom att programmera guider mot RNA för p16 och p21 skapade teamet en variant kallad DAMAGE‑Aging. Denna krets dödade celler med höga nivåer av dessa budbärare samtidigt som celler där p16 genetiskt tagits bort undgick, vilket bekräftar att systemet läser realtids RNA‑nivåer snarare än fasta DNA‑förändringar. Läkemedelsbehandlingar som ökade p16‑ eller p21‑nivåer gjorde celler mer mottagliga för denna riktade självdestruktion.
Packa systemet för framtida terapier
För att närma sig praktisk användning komprimerade författarna de många DNA‑delarna av DAMAGE till en strömlinjeformad konstruktion, DAMAGE‑Plus, och visade att den fortfarande fungerade pålitligt. De transkriberade sedan denna konstruktion till syntetiskt mRNA, förpackade det i lipidnanopartiklar liknande de som användes i COVID‑19‑vacciner, och levererade det till celler i odling. mRNA‑versionen monterade kretsen framgångsrikt och utlöste riktad inflammatorisk död i celler som bar virus‑ eller cancerrelaterade RNA. Även om hela systemet fortfarande är klumpigt och hittills bara testats i cellinjer, antyder dessa resultat att programmerbar, RNA‑styrd celldöd en dag skulle kunna distribueras via injicerbara mRNA‑formuleringar.
Ett nytt sätt att läsa och reagera på cellulära meddelanden
Enkelt uttryckt är DAMAGE en molekylär vakthavare som kontrollerar varje cells interna RNA‑"ID" och kastar ut bara de som ser farliga ut—virusinfekterade, mutationbärande eller senescenta—genom att tvinga dem in i en explosiv form av självdestruktion. Arbetet visar att bakteriella RNA‑sensorer kan kopplas till mänskligt celldöds‑maskineri med hög precision, till och med så att de urskiljer single‑letter‑skillnader i genetiska budskap. Även om mycket ingenjörsarbete återstår innan ett sådant system säkert kan användas i djur eller människor, utgör det en kraftfull ny strategi: att läsa den levande RNA‑konversationen inne i celler och översätta den direkt till liv‑eller‑död‑beslut.
Citering: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Nyckelord: pyroptos, CRISPR, RNA‑riktad terapi, cancerimmunterapi, cellulär senescens