Clear Sky Science · sv
Påverkan från lösningsmedelskrafter och brutet symmetri vid sammansättning av designade proteiner vid ett vätska-fast gränssnitt
Varför denna lilla värld på en yta spelar roll
Från solceller till medicinska sensorer kommer många framtida teknologier att förlita sig på att bygga precisa strukturer där biologiska molekyler möter fasta material. Denna studie undersöker hur specialdesignade protein"stavar" ordnar sig på mineralytor i saltvatten. Den överraskande lärdomen är att vattnet direkt vid ytan, och subtila asymmetrier i kristallen under, kan helt förändra hur dessa proteiner riktar in sig—ibland framkallande mönster som klassisk teori säger inte borde uppstå.
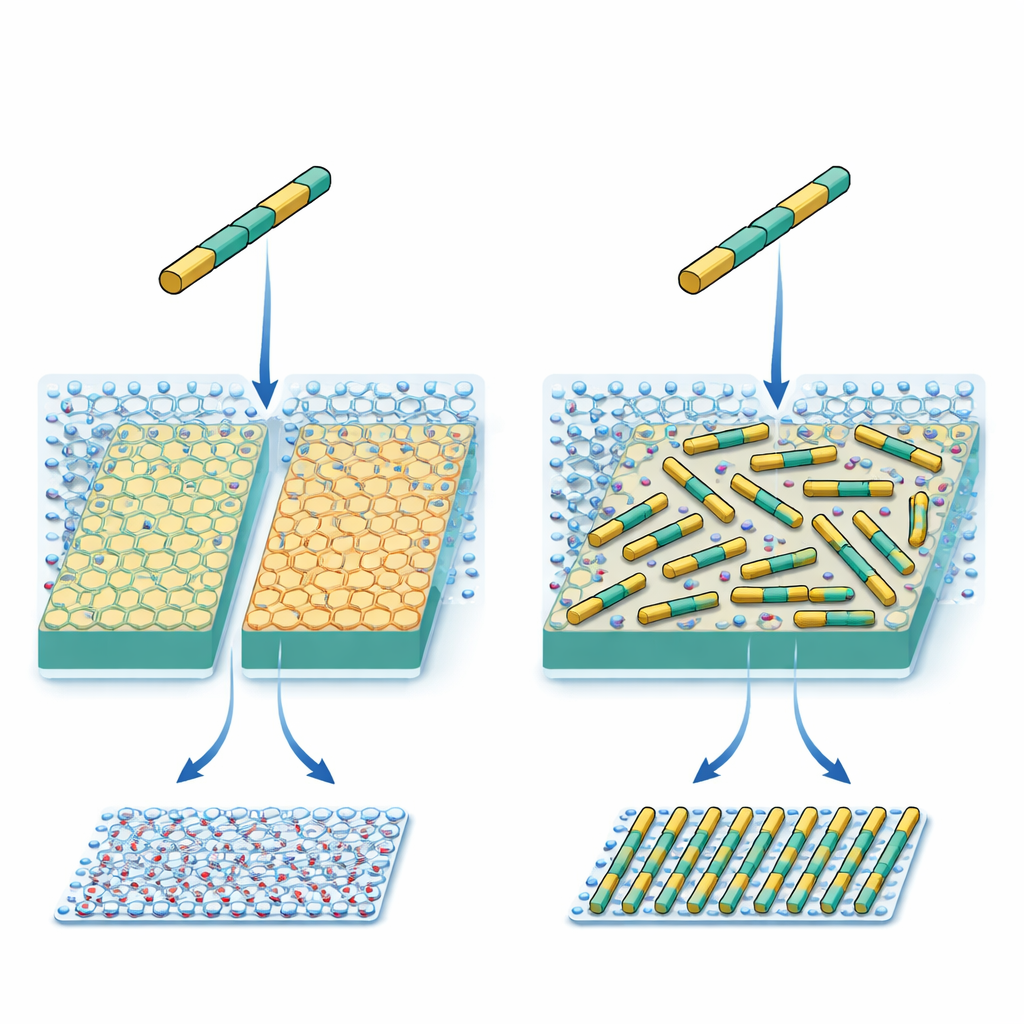
Att designa proteiner för att passa en kristall
Forskarna arbetar med ett konstgjort protein format som en kort, stel stav. Dess ytkemi och avståndet mellan laddade grupper har noggrant utformats för att matcha mönstret av kaliumjoner på ett vanligt mineral kallat glimmer (mica). I princip borde detta göra att varje proteinstav föredrar tre ekvivalenta riktningar på kristallytan, som att orientera sig längs tre ekrar på ett hjul. Tidigare arbete visade att även med sådan noggrann design bildade proteinerna flera oväntade mönster istället för bara det ena ingenjörer hade i åtanke. Denna inkonsistens antydde att någon viktig kraft saknades i rådande designregler.
Två nästintill identiska ytor, två mycket olika utfall
För att spåra vad som hände använde teamet högupplöst sveptunnelmikroskopi (high-speed atomic force microscopy), vilket kan följa individuella proteinstavar när de rör sig och monteras på en yta i realtid. De jämförde två nära besläktade former av glimmer. Båda har samma exponerade kaliumgitter, men deras inre atomstrukturer skiljer sig något, vilket i sin tur förändrar hur vatten organiserar sig i lager precis ovanför ytan. Vid måttliga salthalter bildade stavarna en tät men lokalt oordnad matta på båda ytorna, med endast små fläckar av inriktning. När salt koncentrationen ökades mycket hög blev beteendet dock delat: på den ena glimmer-typen förblev stavarna oordnade längs tre riktningar, medan de på den andra spontant bildade långa, parallella, jämnt åtskilda rader över hela ytan.
Vattenlager och brutet symmetri
Datormodellering av mineralen och det omgivande vattnet hjälpte till att förklara denna delade personlighet. På den mer symmetriska formen av glimmer bevarar det första och andra lagret av vattenmolekyler ett regelbundet, sexkantigt mönster. På den mindre symmetriska formen bryter inre atomer och begravda grupper i kristallen denna trefaldiga symmetri, och detta brutna mönster förmedlas in i de närliggande vattenlagren, som utvecklar randliknande regioner. Proteinerna kommer inte i kontakt med naken kristall ensam; de interagerar också med detta strukturerade vatten. Som ett resultat blir en orientering av stavarna något mer gynnsam än de andra två, även om den designade protein–kristall-matchningen skulle föreslå att alla tre borde vara lika.
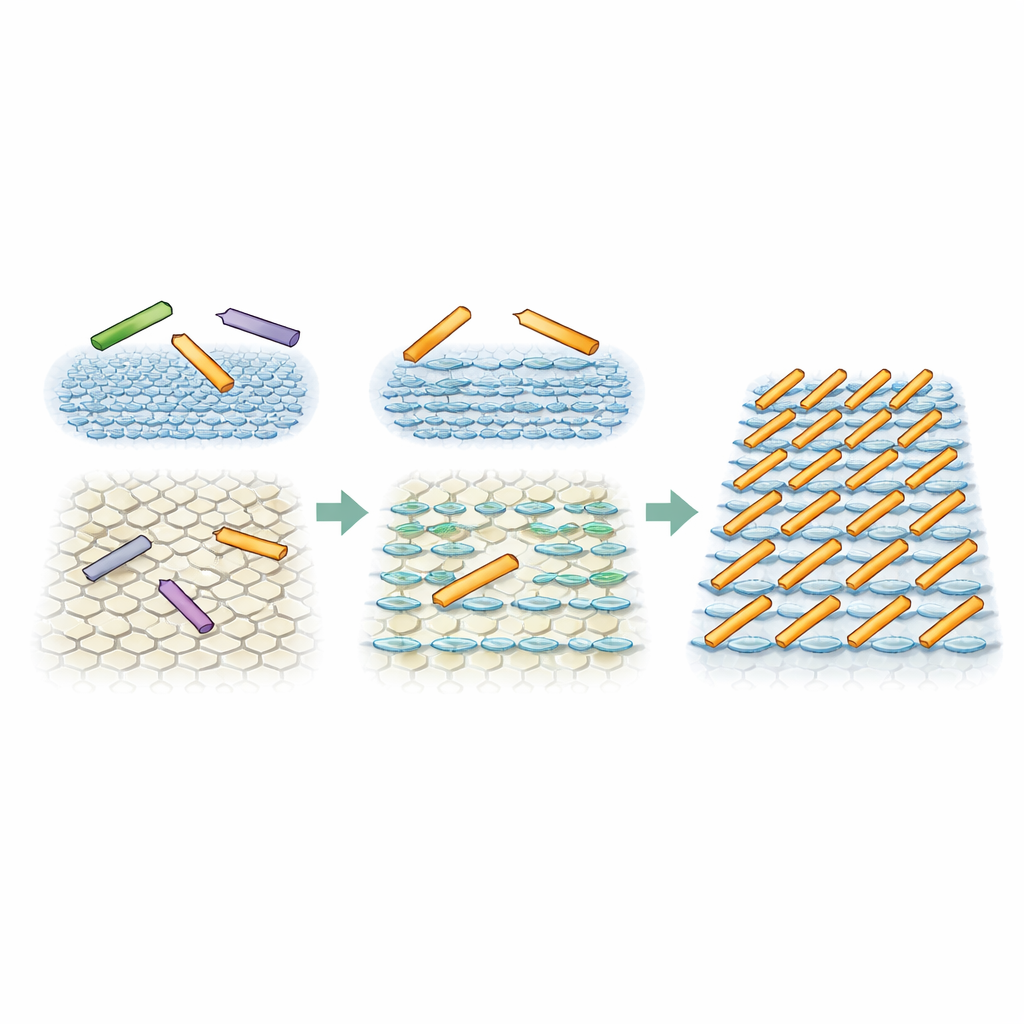
Simuleringar avslöjar en oväntad fas
För att testa om en subtil riktad bias från ytmiljön verkligen kunde förklara de observerade mönstren körde forskarna Monte Carlo-simuleringar av enkla hårda rektanglar som representerar proteinstavarna. I en uppsättning simuleringar var alla tre orienteringar lika sannolika, vilket efterliknade den fullt symmetriska ytan. I det fallet förblev stavarna i ett högdensitets men oordnat tillstånd, med endast tillfällig eller begränsad inriktning, precis som sågs på den ena glimmer-typen. I en andra uppsättning gjorde man en riktning endast måttligt mer gynnsam—ungefär dubbelt så sannolik som de andra två—för att stå för påverkan från de randiga vattenlagren. Under dessa förhållanden, och när stavarna kunde röra sig tillräckligt, utvecklades systemet naturligt till ett tillstånd med parallella, jämnt åtskilda rader. Detta är en så kallad smektisk fas, som långvarig teori säger inte borde uppträda för icke-interagerande stavar i två dimensioner, ändå gjorde den lilla riktade knuffen från gränsytan den stabil.
Ompröva hur vi designar bioinspirerade material
Enkelt uttryckt visar detta arbete att finjusterad protein–ytkemi inte räcker för att förutsäga hur designade proteiner kommer att ordna sig på verkliga material. Vattnet som sitter mellan proteinet och det fasta materialet, och sättet som kristallen subtilt bryter symmetrin på, kan styra monteringen in i mönster som läroböckerna aldrig skulle förutse. Genom att kombinera högupplöst mikroskopi, maskininlärning för att kvantifiera ordning, och fysikbaserade simuleringar, redogör studien för ett sätt att föra in dessa dolda lösningsmedels- och symmetrieffekter i framtida verkyg för proteindesign. För alla som hoppas konstruera pålitliga hybrid bio–oorganiska material är budskapet tydligt: du måste designa inte bara för proteinet och ytan, utan också för det strukturerade vattenskikt som förbinder dem.
Citering: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Nyckelord: proteinens självmontering, vätska-fasta gränsytor, interfacialt vattens struktur, smektisk ordning, bioinspirerade material