Clear Sky Science · sv
En multivalent adaptor-mekanism driver kärnimporten av proteasomer
Hur celler håller sina kontrollrum rena
Inuti varje cell fungerar kärnan som ett kommandocenter, fullt med DNA och de proteiner som styr vilka gener som slås på eller av. För att hålla detta kontrollrum i gott skick förlitar sig cellerna på kraftfulla molekylära ”förstörningsmaskiner” kallade proteasomer som bryter ner utslitna eller felaktiga proteiner. Denna studie avslöjar hur celler hanterar den överraskande knepiga uppgiften att frakta dessa otympliga proteasomer genom de trånga portarna in i kärnan vid precis rätt tidpunkt.
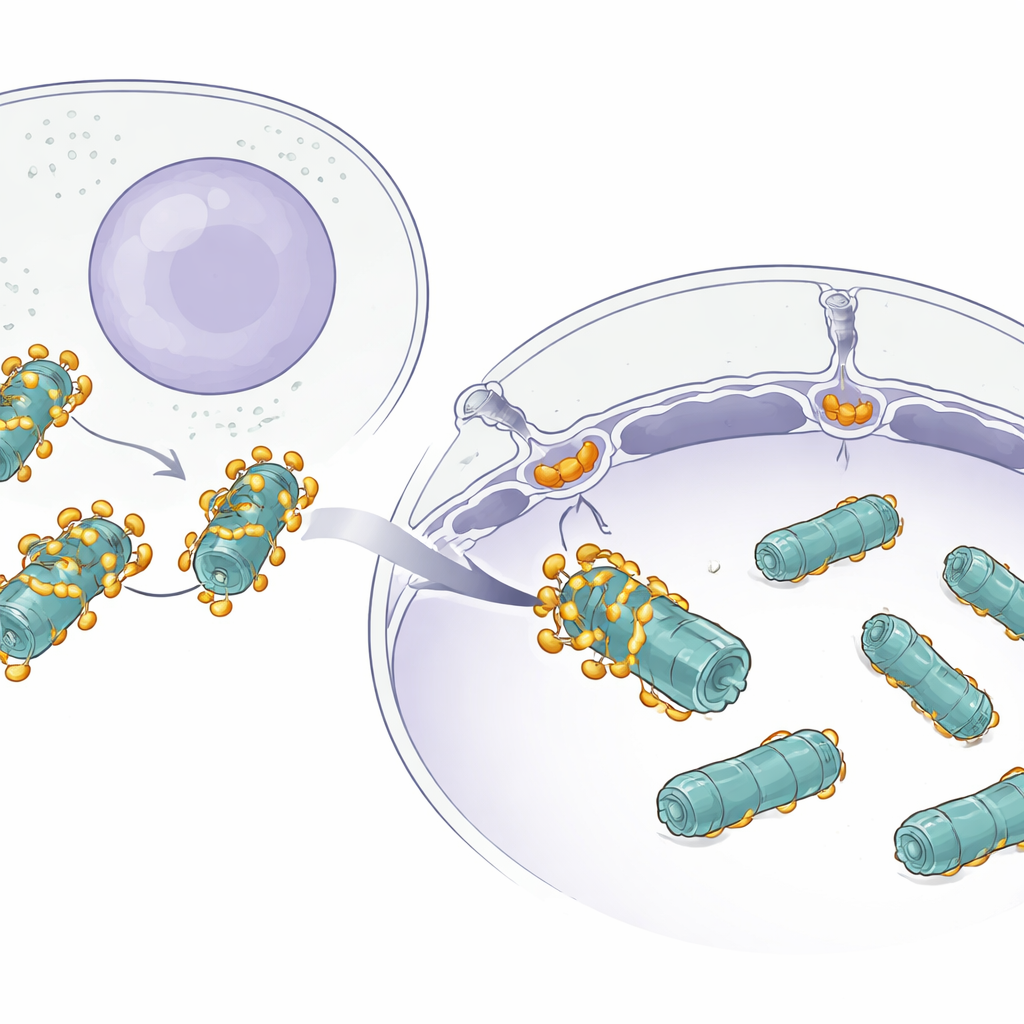
Utmaningen att flytta stora maskiner
Många proteiner transporteras tyst mellan cellens huvuddel och kärnan genom jättestora öppningar i kärnmembranet som kallas kärnporer. Små proteiner kan glida igenom lätt, men stora maskiner som proteasomer är annorlunda: de är massiva, tunnformade komplex byggda av många delar. Medan forskare redan visste att små lastbärare använder hjälpproteiner kallade importiner för att komma in i kärnan, var det oklart hur något så stort som en proteasom tar sig igenom effektivt utan att fastna eller gå vilse.
En formförändrande hjälpare träder fram
Gruppen fokuserade på ett litet, flexibelt protein kallat AKIRIN2, som tidigare arbete visat är helt nödvändigt för att proteasomer ska kunna komma in i kärnan. Celler som delar sig utan AKIRIN2 kan inte föra in proteasomer i kärnan och dör snabbt eftersom skadade kärnproteiner ansamlas. Med en kombination av metoder — inklusive en omfattande mutationsskanning som ändrade nästan varje aminosyra i AKIRIN2, högupplöst kryoelektronmikroskopi för att se komplexet i 3D, och noggranna biokemiska tester — kartlade forskarna vilka delar av AKIRIN2 som är viktiga och vad de gör. De upptäckte ett tidigare underskattat ”vingliknande” segment och en coiled-region som låter AKIRIN2 bilda dimrer (par), vilka båda spelar nyckelroller i att greppa proteasomer och andra partners.
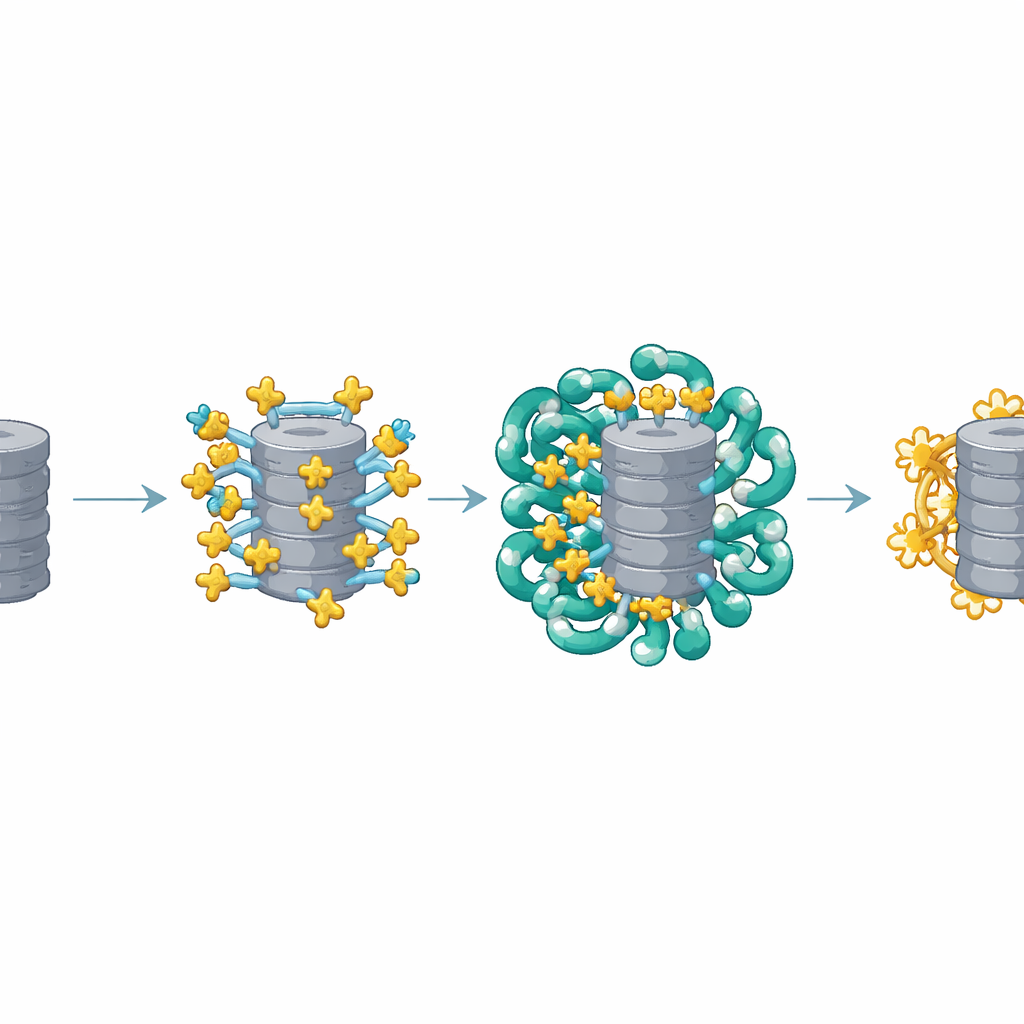
Bygga ett månghandigt transporthandtag
De strukturella bilderna visade att flera kopior av AKIRIN2 klustras på ena sidan av proteasomen som många händer som grabbar samma föremål. Varje AKIRIN2-par binder till specifika platser på proteasomens yta samtidigt som de engagerar olika importiner. En importin, IPO9, håller fast AKIRIN2 på ett ovanligt sätt, sveper runt det och ändrar form när komplexet monteras. Andra importiner, som också arbetar i par, känner igen korta kärninträdesignaler som bärs av AKIRIN2. Eftersom flera AKIRIN2-molekyler sitter på samma proteasom visar de tillsammans många av dessa signaler samtidigt. Detta multivalenta ”handtag” tillåter en skara importiner att haka i samtidigt, vilket ger den stora proteasomen tillräcklig dragkraft för att ta sig igenom kärnporen.
En smart monterings- och frisättningscykel
Rekonstruktionsexperiment i ett förenklat provrörssystem visade att proteasomer bara kommer in i kärnor effektivt när både AKIRIN2 och importiner finns närvarande samtidigt. Ju mer AKIRIN2, desto starkare och snabbare import. När proteasomerna väl är inne i kärnan måste transportmaskineriet avlägsnas så att proteasomerna kan arbeta. Här använder cellen en tvåstegsfrisättning. Ett litet switchprotein kallat Ran, i dess GTP-bundna form, rycker av de flesta importinerna från deras last. AKIRIN2 och vissa IPO9 sitter kvar mer envist, men kärnan har en backup: nukleära proteasomer bryter direkt ner AKIRIN2 självt, utan den vanliga märkningen med ubiquitin. Mätningar över cellcykeln visar att AKIRIN2 når sin topp under celldelning, när nya kärnor bildas, och sedan sjunker i tidig G1, förenligt med denna riktade upprensning.
Varför detta betyder något bortom ett protein
Tillsammans visar dessa fynd att AKIRIN2 fungerar som en flexibel ställning som samlar många importiner på en enda proteasom och förvandlar ett svårt transportproblem till ett koordinerat grupparbete. Genom att klustra kärninträdesignaler på en adaptor snarare än på proteasomen själv kan celler styra när och hur starkt stora maskiner flyttas in i kärnan utan att bygga om dessa maskiner. Liknande adapterbaserade strategier verkar användas för andra stora proteinkomplex, och till och med virus utnyttjar besläktade knep för att tränga in i kärnan. Att förstå denna generella transportlogik fördjupar vår bild av hur celler upprätthåller proteinkoncentrationen i sitt mest känsliga fack och kan så småningom peka ut nya sätt att ingripa när proteinnedbrytning eller kärnfunktion störs.
Citering: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Nyckelord: nuclear transport, proteasome, AKIRIN2, importin, protein degradation