Clear Sky Science · sv
En integrativ strukturell biologisk ansats avslöjar den dynamiska organisationen av chaperonkomplexet R2SP
Hur celler bygger komplexa molekylära maskiner
Inuti varje cell arbetar många proteiner inte ensamma — de måste sätta sig samman till invecklade maskiner innan de kan utföra sina uppgifter. Att få denna monteringssteg rätt är avgörande för frisk andning, rörelse och till och med fertilitet. Denna artikel utforskar en sådan monteringsassistent, en molekylär "byggnadsstyrka" kallad R2SP-komplexet, och visar hur den är organiserad och hur den fungerar. Att förstå R2SP är viktigt eftersom när dess komponenter sviktar så rör sig de små hårlika utskotten på celler, cilier, inte korrekt, vilket leder till kroniska andningsproblem och andra sjukdomar.
De cellulära bygglagen: R2TP och R2SP
Celler förlitar sig på team av hjälpproteiner, så kallade chaperonkomplex, för att vägleda andra proteiner till rätt mångdelade former. Ett länge studerat team, kallat R2TP, finns i många vävnader och hjälper till att montera stora maskiner som RNA‑syntesmaskiner och DNA‑skadesensorer. R2SP är en nära släkting till R2TP: båda är byggda runt samma ringformade motor bestående av två partnerproteiner, RUVBL1 och RUVBL2, som förbrukar energimolekylen ATP. Det som skiljer dem åt är de assisterande adaptrarna som kopplar klienter till denna motor. R2TP använder adaptrar kallade RPAP3 och PIH1D1, medan R2SP använder SPAG1 och PIH1D2. Dessa små skillnader i delar ger de två komplexen olika klientlistor och kopplar särskilt R2SP till konstruktionen av de rörliga cilier som sveper bort slem och vätskor över vävnader.
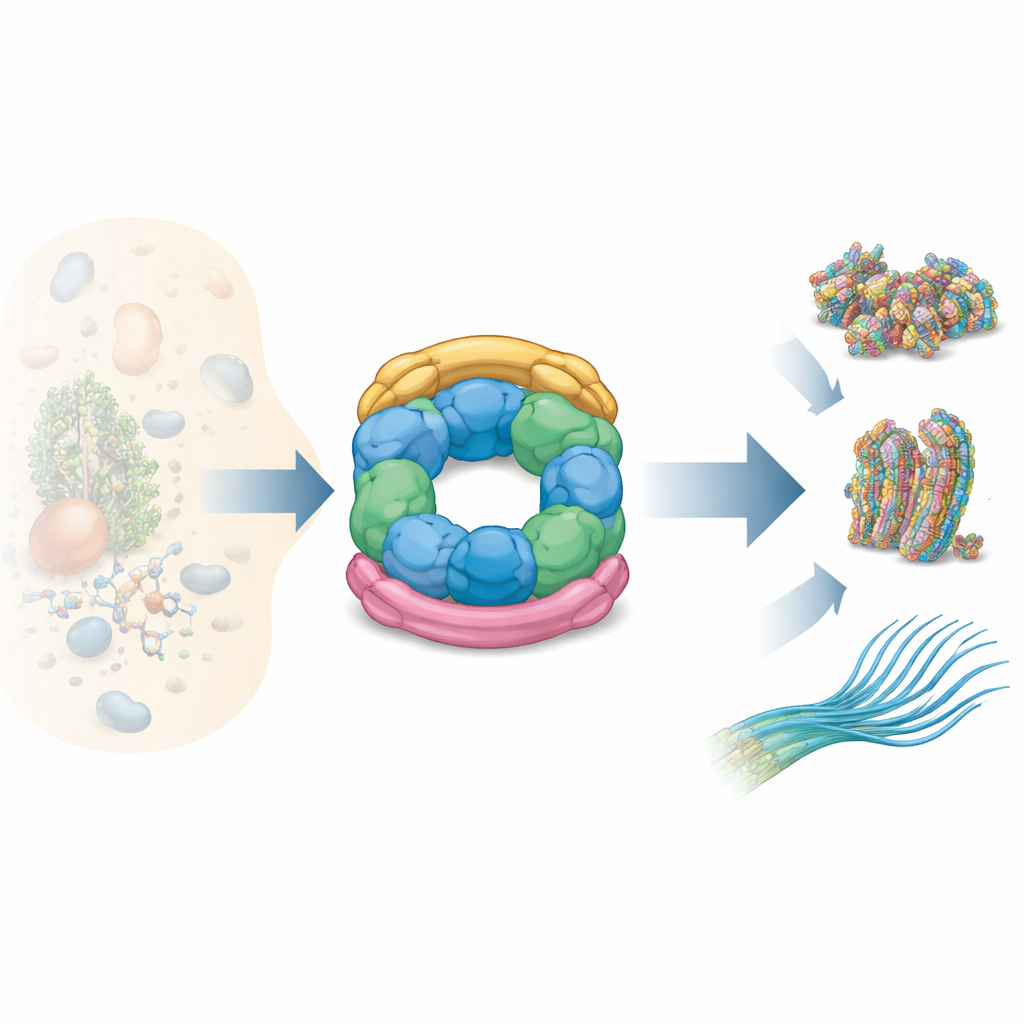
Hur R2SP‑delarna passar ihop
Författarna kombinerade flera strukturella tekniker — kärnmagnetisk resonans, kryoelektronmikroskopi och korslänknings‑masspektrometri — med biokemiska tester för att kartlägga hur R2SP är uppbyggt. De visade att svansen på SPAG1 greppar RUVBL1/RUVBL2‑ringen på ett sätt som liknar hur RPAP3 binder i R2TP, men med viktiga justeringar i form och kontaktpunkter. En andra adapter, PIH1D2, lägger sig under ringen och når även upp för att röra vid flexibla sidodomäner hos motorn. Dessa sidodomäner fungerar som gångjärnsarmar som hjälper till att överföra rörelser från ATP‑förbrukande kärnan till bundna klienter. Data visar att SPAG1 och PIH1D2 inte fäster oberoende av varandra: de samverkar och bildar en ihopkopplad enhet som klämmer ringen uppifrån och nedifrån och stabiliserar en karaktäristisk tredimensionell arkitektur.
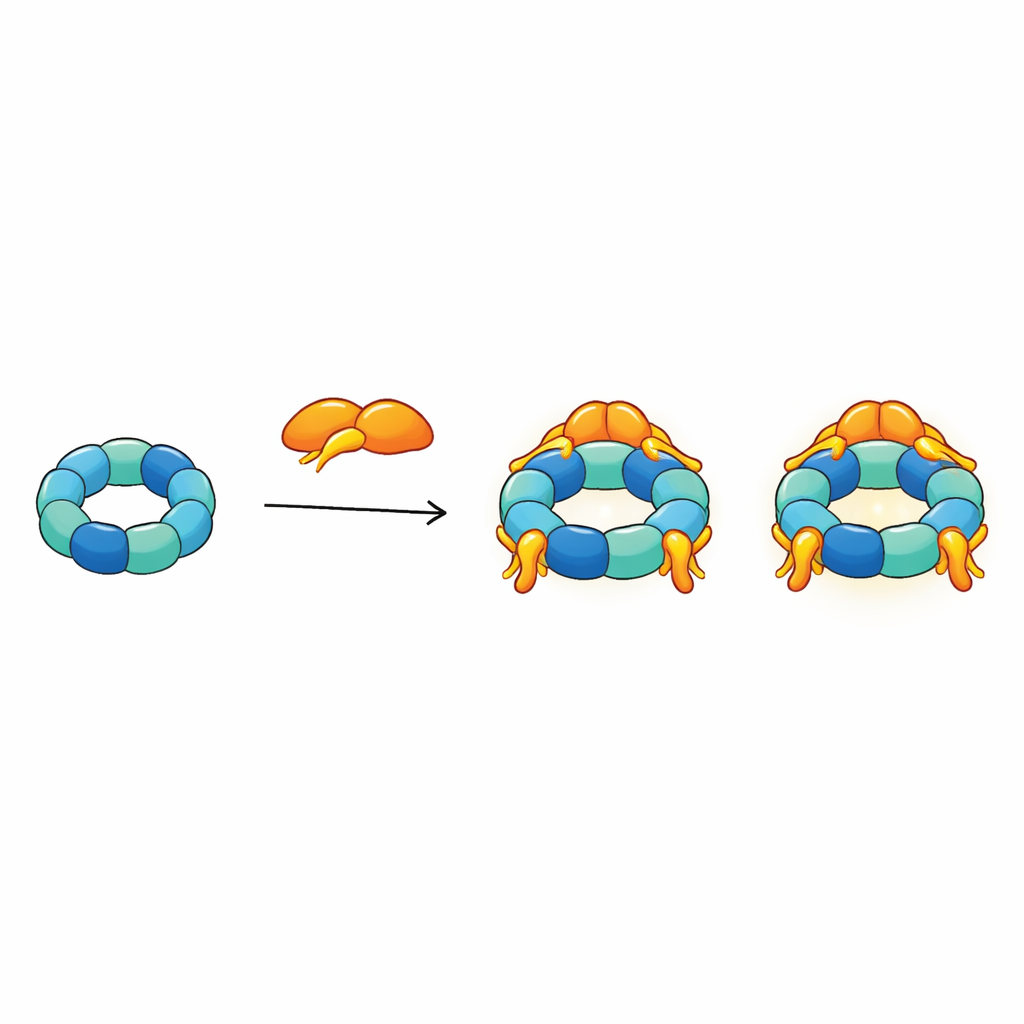
En dynamisk ring som växlar växel
Bortom statiska bilder frågade teamet hur R2SP beter sig i rörelse. Med interaktionsmätningar fann de att RUVBL1/RUVBL2‑motorn kan existera antingen som en enkel ring eller som en staplad dubbelring. När SPAG1 och PIH1D2 binder, flyttar de denna balans kraftigt mot enkelringsformen och kan pryda den med upp till tre adapterpar. Samtidigt ökar adaptrarna markant motorns ATP‑förbränningsaktivitet och ändrar hur snabbt ATP‑lika molekyler binder till och släpper från de aktiva ytorna. Jämfört med R2TP‑systemet favoriserar SPAG1 och PIH1D2 olika steg i nukleotidfrisättning, vilket tyder på att R2SP finjusterar energicykeln i kärnmotorn på sitt eget sätt. Denna noggrant kontrollerade energianvändning tros driva den stegvisa monteringen av klientkomplex som behövs för rörliga cilier.
En flexibel plattform för att bygga cilier‑komponenter
Genom att integrera alla sina strukturella begränsningar i en enda modell föreslår författarna att R2SP fungerar som en flexibel, mångaarmad plattform. SPAG1‑svansen förankrar stadigt på toppen av ringen, medan dess andra regioner och de två domänerna i PIH1D2 sträcker sig mot motorns mer öppna, arm‑lika sida. Det är på denna sida som klientproteiner och hjälpchaperoner såsom HSP70 och HSP90 sannolikt dockar. Eftersom upp till tre SPAG1–PIH1D2‑enheter kan fästa vid en ring och de flexibla armarna ständigt rör sig, liknar hela komplexet en bläckfisk vars tentakler kan greppa flera klientdelar samtidigt, koordinera dem och föra dem vidare för att byggas in i större cilierstrukturer.
Vad detta betyder för hälsa och sjukdom
För icke‑specialister är huvudbudskapet att R2SP är en specialiserad version av en generell cellulär byggmaskin, omkopplad genom att byta ut bara två adapterproteiner. Detta byte förändrar både hur den centrala motorn styrs och hur klienter positioneras, vilket förklarar varför R2SP fokuserar på att bygga delar för rörliga cilier medan R2TP tjänar andra cellulära fabriker. Fel i SPAG1 är redan kända för att orsaka primär ciliedyskinesi, en sjukdom som kännetecknas av kroniska infektioner och fertilitetsproblem. Genom att avslöja R2SP:s detaljerade struktur och verkningsprinciper lägger denna studie grunden för att förstå hur specifika mutationer stör ciliesammansättningen och kan så småningom vägleda riktade behandlingar som återställer eller modulerar denna viktiga molekylära byggstyrka.
Citering: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Nyckelord: molekylära chaperoner, proteinkomplexmontering, rörliga cilier, strukturell biologi, RUVBL1 RUVBL2