Clear Sky Science · sv
Molekylär mekanism för fosfatimport av den bakteriella transportören PstSCAB
Varför små näringsämnen spelar roll för oss
Varje levande cell, från mänskliga neuroner till markbakterier, är beroende av fosfor. Detta grundämne hjälper till att lagra energi, bygga DNA och hålla cellmembran intakta. I miljön är användbart fosfat—den form av fosfor som celler faktiskt kan importera—dock ofta knapp. Många sjukdomsframkallande bakterier förlitar sig på en extremt effektiv molekylär maskin, kallad PstSCAB-transportören, för att samla upp fosfat när det är ont om det. Att förstå exakt hur denna maskin fungerar är inte bara en grundläggande vetenskaplig fråga; det kan också öppna dörrar för nya sätt att oskadliggöra infektioner genom att svälta ut bakterier från detta livsviktiga näringsämne.
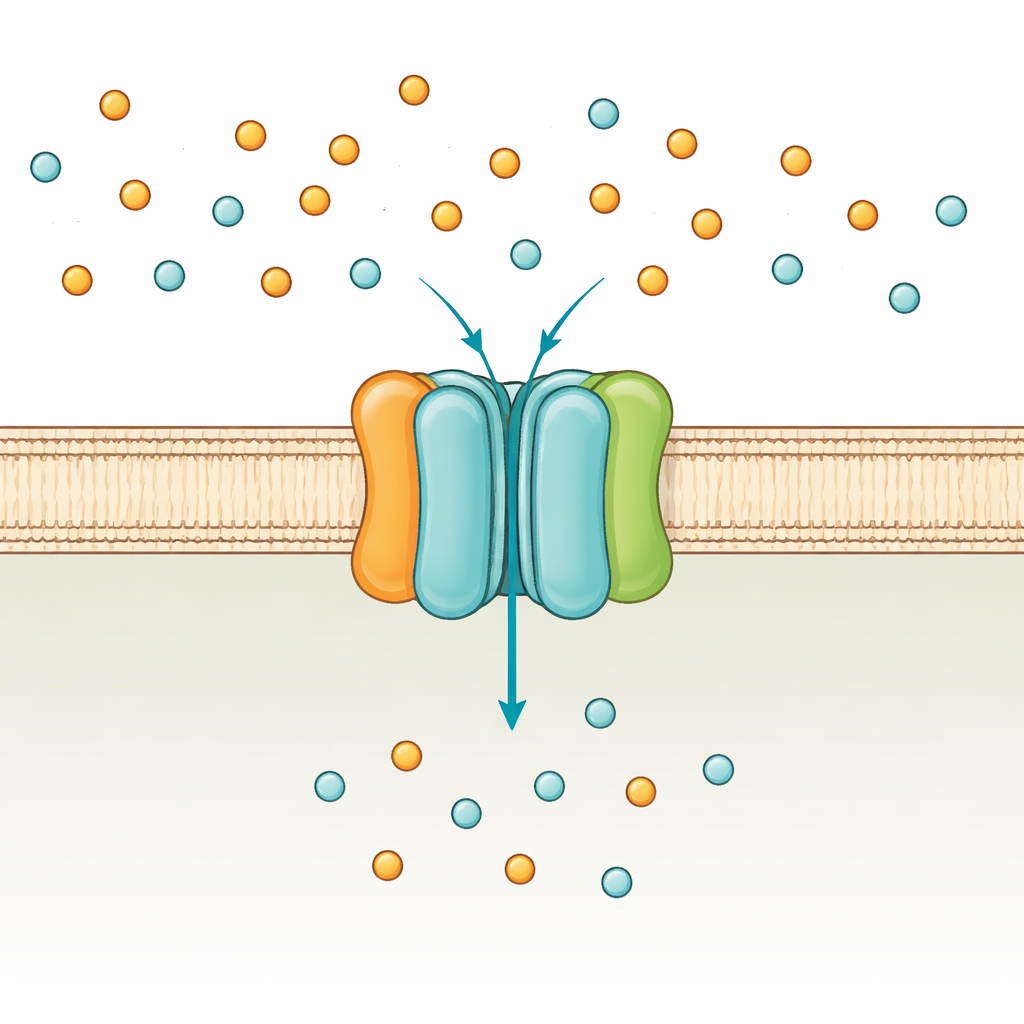
Cellens fosfatportvakt
Bakterier som Escherichia coli använder två huvudvägar för att ta upp fosfat: ett låg-affinitetssystem som fungerar när fosfat är rikligt, och det hög-affinitiva PstSCAB-systemet som slås på vid brist. PstSCAB sitter i cellmembranet och drivs av ATP, cellens universella energivaluta. Det är uppbyggt av fem delar: två membraninbäddade subenheter (PstA och PstC) som bildar passagevägen, ett lösligt ”fångar”-protein utanför membranet (PstS) som fångar fosfat, och ett par interna subenheter (PstB) som förbränner ATP för att driva transporten. Eftersom detta system också hjälper till att reglera många gener kopplade till bakteriell virulens kan mutationer i PstSCAB försvaga patogener som orsakar urinvägsinfektioner, sepsis hos lantbruksdjur och tuberkulos.
Att fånga maskinen i arbete
Hittills hade forskare endast partiella bilder av PstSCAB, mestadels av fångarproteinet PstS ensamt. I denna studie använde forskarna högupplöst kryo-elektronmikroskopi för att visualisera hela transportören i flera nyckelsteg i dess arbetscykel. De rekonstituerade de bakteriella proteinerna i konstgjorda membran-"nanodiskar" och frös dem så snabbt att molekylerna fångades mitt i rörelsen. Genom att noggrant justera proteinerna och tillsätta eller undanhålla ATP erhöll de strukturer av tre huvudtillstånd: en vilande inåtvänt form utan fångaren fäst, ett pre-translokationstillstånd där fosfatladdad PstS dockar vid membrankomplexet, och ett ATP-bundet katalytiskt intermediär där fosfat hålls inne i transportören.
Hur formförändringar förflyttar fosfat
Bilderna visar hur samordnade formförändringar förflyttar fosfat från utsidan till insidan av cellen. I vilotillståndet öppnar passagevägen som bildas av PstA och PstC endast mot cellens innandöme; utsidan är förseglad av en uppsättning ”grind”-rester, vilket betyder att fosfat ännu inte kan komma in från utsidan. När fosfatladdad PstS dockar i pre-translokationstillståndet, lägger den sig mellan flexibla slingor i PstA och PstC men, anmärkningsvärt, förändras membransubenheterna knappt i form. Den verkliga förskjutningen sker när PstS börjar öppna sina två lober för att släppa ut fosfat och samtidigt svänger de två PstB-subenheterna ihop för att binda ATP. Denna ATP-bindning klämmer PstB till en dimer och drar i förbindande helixar i PstA och PstC, vilket vrider hela poren till en utåtvänt konformation som exponerar en specifik fosfatbindande ficka mot utsidan.
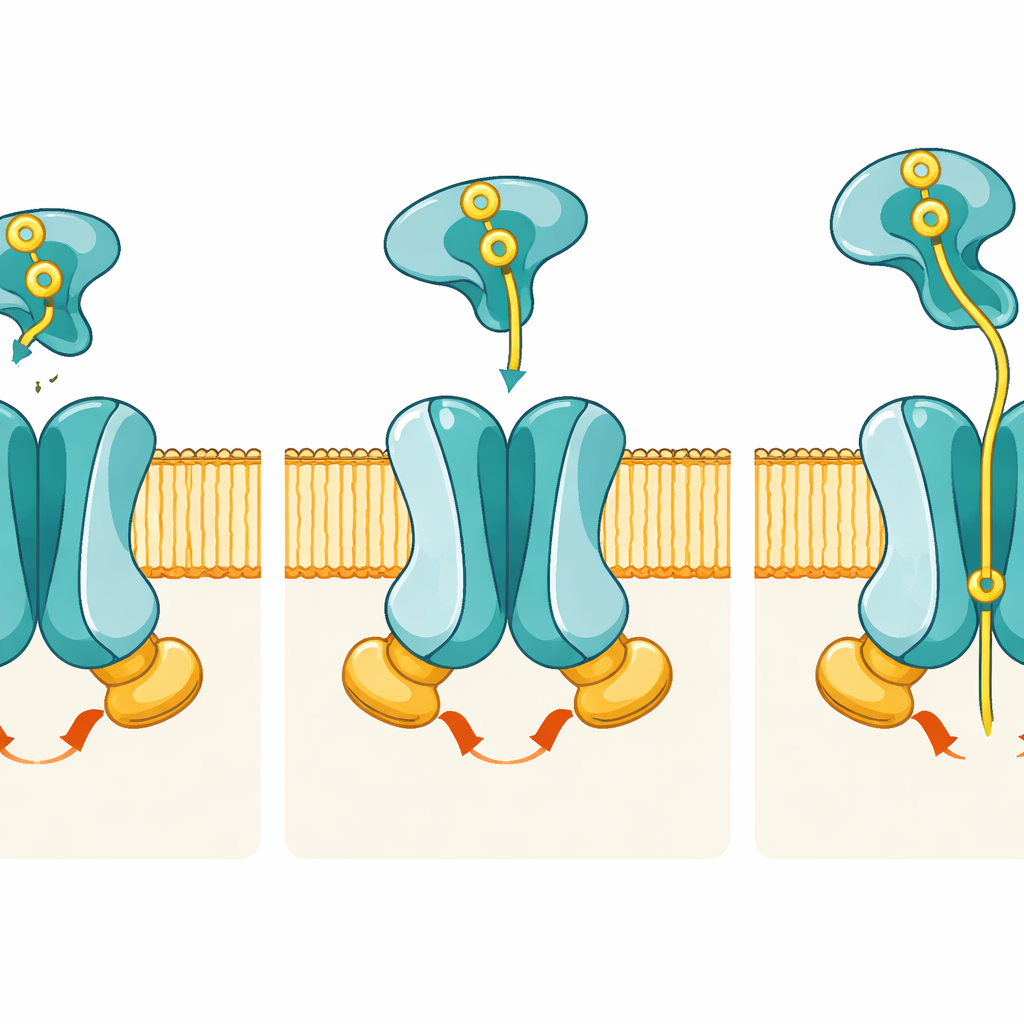
En specialgjord ficka för fosfat
I den utåtvända, ATP-bundna strukturen hittar författarna en densitet i mitten av membranområdet som stämmer överens med en fosfation. Denna jon omfamnas av positivt laddade aminosyror—särskilt två argininer, en från PstA och en från PstC—som fungerar som molekylära fingertoppar och greppar den negativt laddade fosfaten. Datorsimuleringar visar att fosfat förblir stabilt bundet i denna ficka över mikrosekunder, och genetiska experiment bekräftar dess betydelse: när dessa nyckelrester muteras förbrukar transportören fortfarande ATP men importerar fosfat mycket dåligt. Denna åtskillnad mellan ”var energi förbrukas” och ”var lasten känns igen” belyser hur precist maskinen är anpassad för fosfat.
Från strukturella ögonblicksbilder till medicinska löften
Tillsammans skisserar strukturerna och de stödjande biokemiska testerna en full cykel: PstS fångar fosfat utanför, dockar vid den inåtvända transportören, och sedan—kopplat till ATP-bindning och nedbrytning av PstB—utlöser en vändning som för vidare fosfatet in i membranfickan och slutligen in i cellens inre. Efter att ATP hydrolyserats slappnar maskinen tillbaka till vilotillståndet, redo för en ny runda. För en lekman är huvudbudskapet att vi nu har en atomnivåritning för hur många bakterier överlever i låg-fosfatmiljöer och reglerar sin virulens. Denna detaljerade karta kan vägleda designen av läkemedel, antikroppar eller peptider som sätter igen transportören eller blockerar dess fångarprotein, vilket potentiellt förvandlar en avgörande näringsport till ett sårbart terapeutiskt mål.
Citering: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Nyckelord: fosfattransport, bakteriellt näringsupptag, ABC-transportör, PstSCAB, antibakteriella mål