Clear Sky Science · sv
Sen-stadies N-Me-selektiv alkenylering och alkynylering av läkemedel och oaktiverade tertiära aminer med fotoredoxkatalys
Varför det fortfarande spelar roll att förändra gamla läkemedel
Många av dagens läkemedel fungerar bra men lämnar utrymme för förbättringar vad gäller säkerhet, biverkningar eller hur precist de träffar sina mål i kroppen. Kemi-forskare intresserar sig i allt högre grad för att varsamt "finjustera" befintliga läkemedel sent i utvecklingsprocessen, snarare än att uppfinna helt nya molekyler från grunden. Denna studie visar hur synligt ljus kan användas för att fästa nya delar på en vanlig typ av läkemedelsbyggsten, vilket skapar förbättrade kandidater till antidepressiva och öppnar en snabbare väg till förfinade behandlingar.
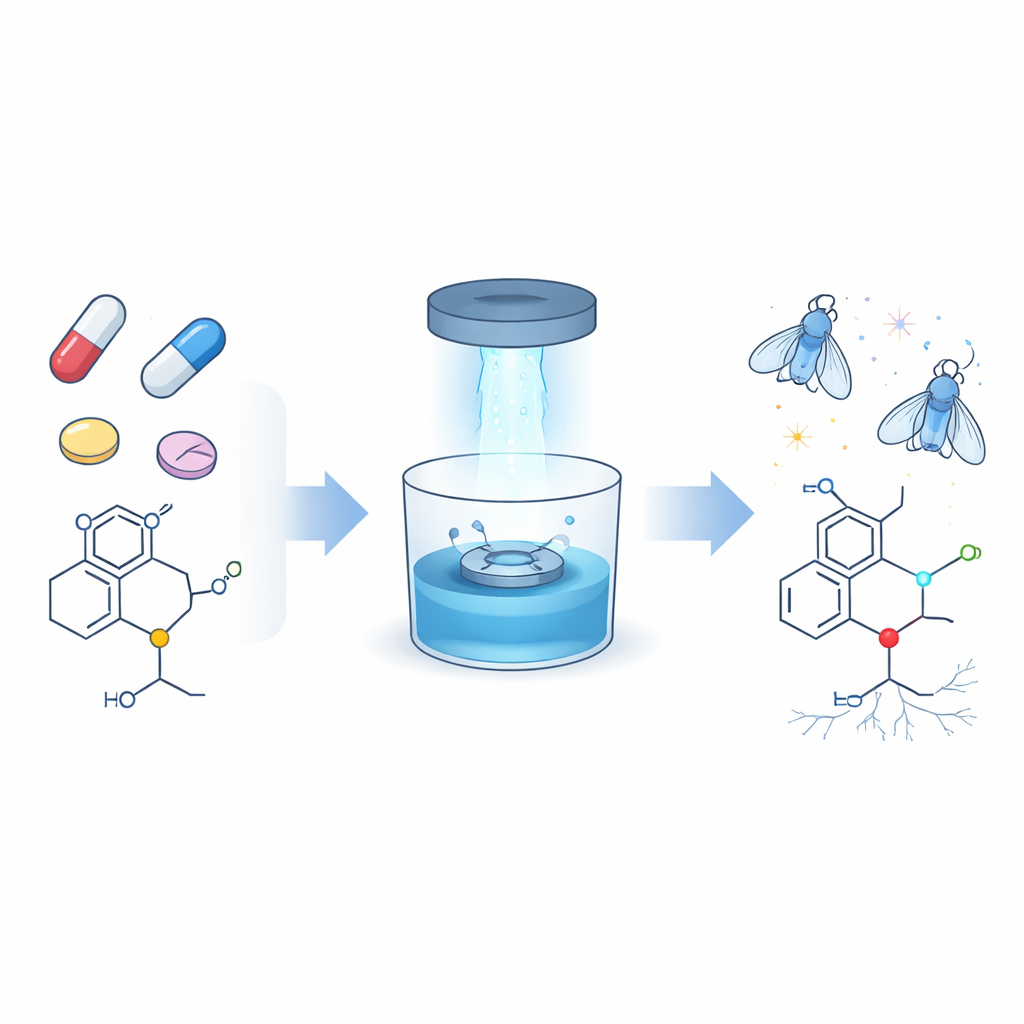
Uppgradering av en vanlig struktur i många läkemedel
En överraskande stor andel av moderna läkemedel — mer än två av fem — innehåller kväverika fragment kallade aminer, och de flesta av dessa är en undergrupp som kallas tertiära aminer. De förekommer i antibiotika, cancerläkemedel, allergitabletter, smärtstillande medel och antidepressiva. Hittills har kemister haft svårt att selektivt modifiera bara en liten del av dessa grupper, N-metyl-enheten, när den sitter bland flera nästan identiska kol–väte-bindningar. Författarna ville utveckla ett skonsamt, pålitligt sätt att fästa nya ”handtag”, specifikt kol–kol-dubbelbindningar (alkener) och trippelbindningar (alkyner), på den N-metyl-positionen utan att störa resten av läkemedelsmolekylen.
Använda ljus för att omkoppla en bindning i taget
Gruppen vände sig till fotoredoxkatalys, en teknik som använder synligt ljus och en ljuskänslig katalysator för att flytta enkel-elektroner och utlösa reaktioner under milda förhållanden. I deras system exciterar blått ljus en organisk katalysator, som tillfälligt drar ut en elektron från den tertiära aminen. Detta steg skapar en kortlivad radikal vid N-metyl-platsen som kan förena sig med noggrant utvalda partnermolekyler som bär vinyl- eller alkynylgrupper. Genom att finjustera reaktionsvillkoren — val av lösningsmedel, bas och tillsatser — uppnådde forskarna höga utbyten och utmärkt kontroll, så att den nya gruppen nästan uteslutande hamnar på N-metyl-positionen, även när flera liknande platser finns. De visade detta på en bred panel av enkla aminer och sedan på riktiga läkemedel, inklusive antihistaminer, hjärtmediciner, anti-infektiva medel och flera antidepressiva.
Från kemisk justering till bättre antidepressiv verkan
För att pröva om dessa strukturella justeringar kunde ha medicinsk betydelse fokuserade författarna på imipramin, ett länge använt tricykliskt antidepressivt läkemedel. De designade och modellerade mer än tjugo imipramin-varianter där den nya vinyl- eller alkynylutströmningen bar aromatiska ringar som kunde passa tätt in i en hydrofob ficka i den mänskliga serotonintransportören, ett protein som reglerar nivåerna av den stämningsrelaterade budbäraren serotonin. Datorsimuleringar (dockning) föreslog att många av dessa modifierade molekyler borde binda lika bra som, eller bättre än, moderläkemedlet. De mest lovande kandidaterna syntetiserades sedan med den nya ljusstyrda metoden och testades i levande system: en bananfluge-modell för depression baserad på social isolering och, för de två bästa föreningarna, i musens nervceller som aktivt transporterar serotonin.
Hur flugor och celler avslöjade starkare läkemedel
I isolerade hanbananflugor visar sig depressionsliknande beteende som förhöjd aggression. Att ge imipramin minskar denna aggression, vilket speglar dess antidepressiva verkan hos människor. Anmärkningsvärt nog minskade flera av de imipramin-derivat som framställdes med den nya metoden aggressionen lika bra, och fyra kandidater fungerade ännu bättre än imipramin självt. I odlade mus-hippocampusceller blockerade två ledande föreningar återupptaget av serotonin starkare än imipramin, vilket bekräftades både genom direkt kemisk mätning av serotonin och med en fluorescerande färg som lyser upp när den tas upp i cellerna. Dessa tester visar att subtila sen-stadie-ändringar vid N-metyl-platsen faktiskt kan öka antidepressiv potens snarare än bara förändra molekylen på papper.
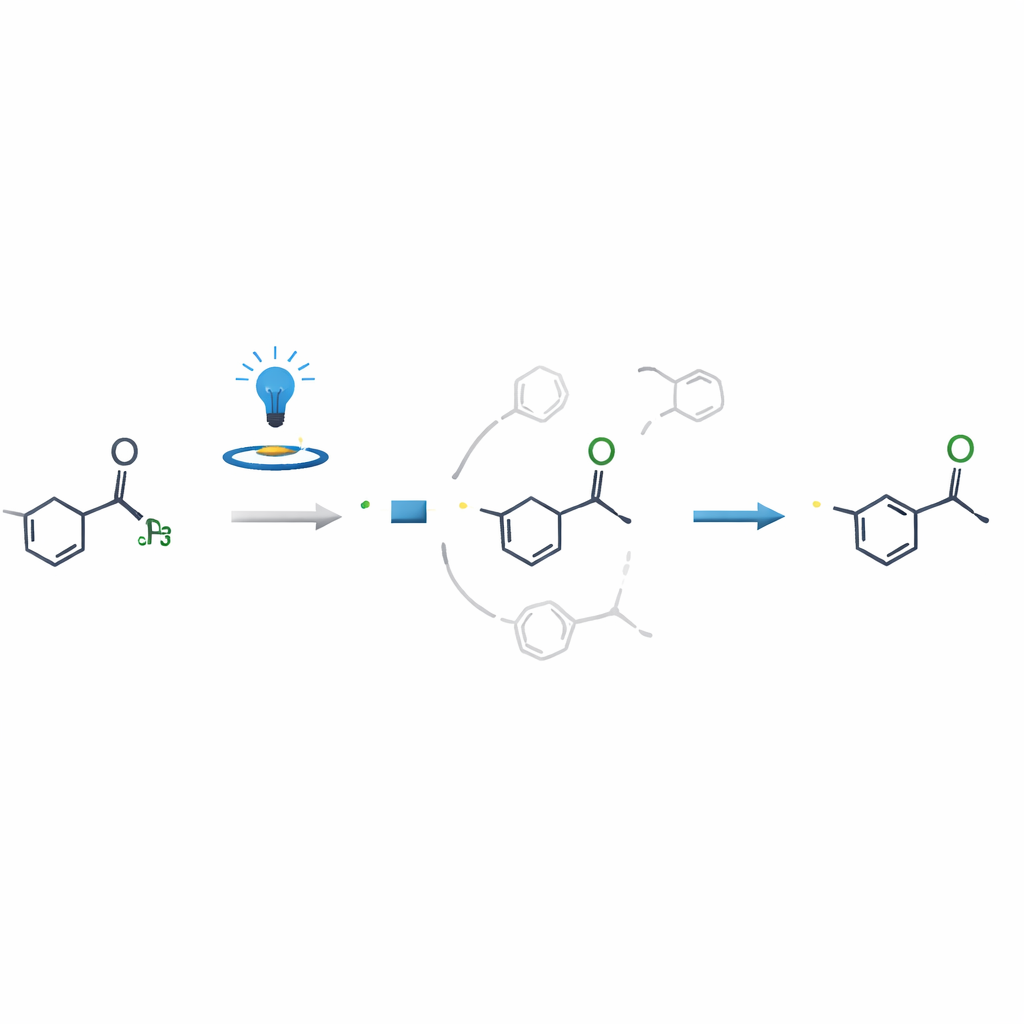
Varför reaktionen är så selektiv
En nyckelfråga var varför reaktionen modifierar N-metylgruppen så rent när andra närliggande positioner ser lika reaktiva ut. Genom kontrollexperiment, elektronspinnmätningar och detaljerade datorberäkningar visade författarna att den avgörande beslutspunkten inte är när radikalen först bildas, utan när den radikala adderar till vinyl- eller alkynylpartnern. Väg-leden från N-metyl-radikalen till slutprodukten är både energimässigt lättare och mycket snabbare än konkurrerande vägar, vilket effektivt styr reaktionen mot ett enda utfall. Denna insikt hjälper till att förklara den höga selektiviteten och kan vägleda liknande strategier på andra komplexa molekyler.
Vad detta arbete betyder för framtida läkemedel
Sammantaget introducerar studien ett praktiskt sätt att kirurgiskt uppgradera befintliga läkemedel som innehåller tertiära aminer, genom att lägga till kompakta kemiska handtag som kan finstämma hur de interagerar med biologiska mål eller länkas till andra komponenter. Genom att visa att sådana sen-stadie-modifikationer kan förvandla ett väletablerat antidepressivum till ännu mer effektiva varianter i enkla djur- och cellmodeller, pekar arbetet mot en kraftfull kombination av modern syntetisk kemi, beräkningar och biologi. När tillvägagångssättet utvidgas till andra läkemedel kan det påskynda förfiningen av läkemedelskandidater och hjälpa till att förnya äldre terapier med förbättrad prestanda och säkerhet.
Citering: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Nyckelord: fotoredoxkatalys, sen-stadie funktionalisering, tertiära aminer, design av antidepressiva läkemedel, serotonintransporter