Clear Sky Science · sv
Hämmningsmekanism för svampars β−1,3-glukan-syntaser av triterpenoida svampmedel
Varför det är viktigt att stoppa svampinfektioner
Svampinfektioner dödar i tysthet mer än en miljon människor varje år och hotar grödor och ekosystem över hela världen. Läkare har redan att göra med en begränsad lista av svampmedel, och vissa farliga svampar utvecklas för att undkomma dem. Denna studie avslöjar i molekylär detalj hur en ny klass av svampmedel fäster vid och inaktiverar ett nyckelenzym som svampar behöver för att bygga sin skyddande cellvägg. Att förstå denna process ger en karta för att utforma bättre behandlingar som kan överlista resistenta svampar.
Muraren som bygger svampcellväggen
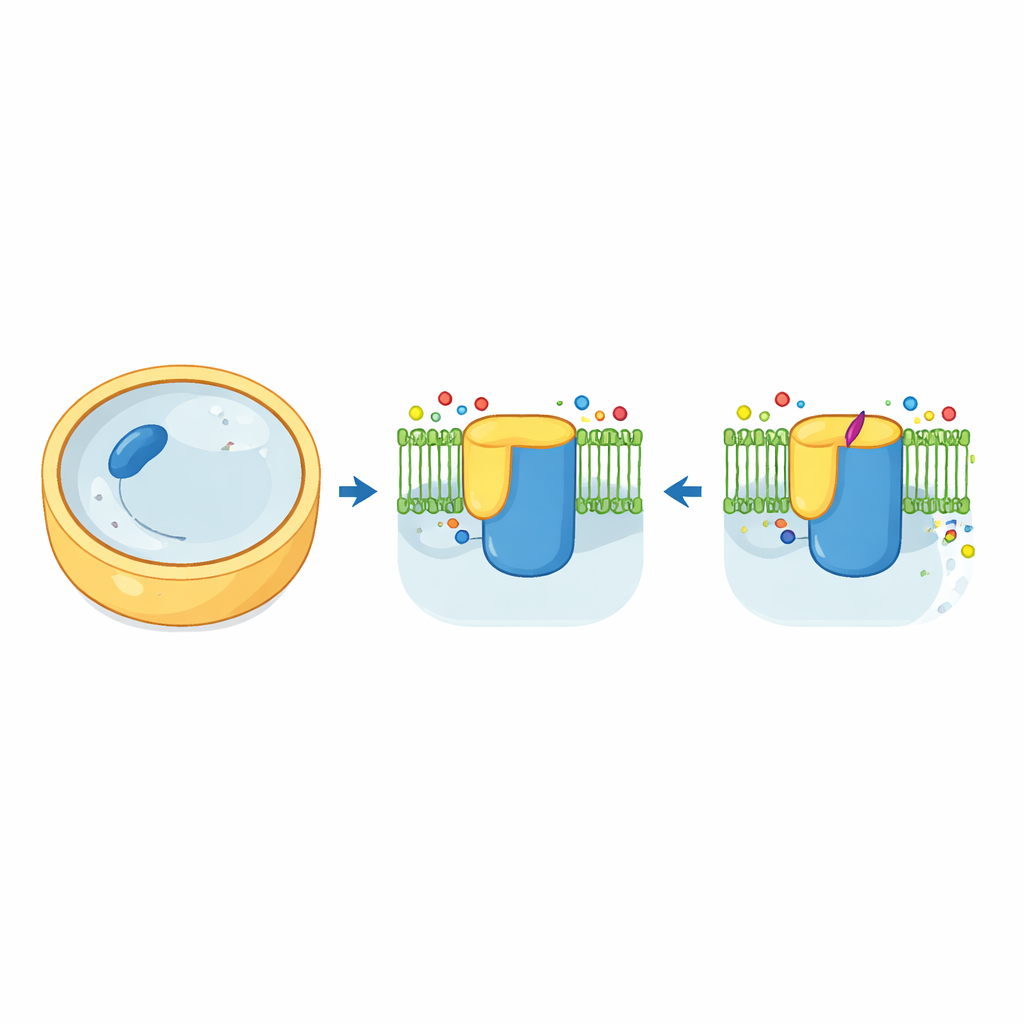
Svampceller är omslutna av en tålig vägg som till stor del består av en sockerbaserad polymer kallad beta-1,3-glukan. Enzymet som tillverkar och exporterar denna polymer, känt som beta-1,3-glukan-syntas, fungerar som en kombination av murare och transportband. I jästsvamp byggs detta maskineri av två mycket lika varianter, Fks1 och Fks2, var och en inbäddad i cellmembranet och reglerad av ett litet hjälpprotein kallat Rho1. Med kryo-elektronmikroskopi fångade forskarna högupplösta tredimensionella bilder av både Fks1 och Fks2 i deras naturliga form. Strukturerna visar ett stort cytosoliskt ”arbetsbord” förenat med en skog av membrangenomträngande helixar, med en central hålighet som sannolikt tjänar som tunneln genom vilken den växande glukankedjan lämnar cellen.
Hur ett naturproduktläkemedel griper enzymet
Kliniskt viktiga triterpenoida läkemedel, inklusive det orala preparatet ibrexafungerp, spårar sitt ursprung till en naturlig förening kallad enfumafungin. Fram till nu visste ingen exakt var på glukan-syntasen dessa läkemedel binder. Forskarna löste strukturer av både Fks1 och Fks2 bundna till enfumafungin. Överraskande nog kilas inte läkemedlet in i den aktiva ytan där sockerenheter kopplas samman. Istället ligger det inbäddat på utsidan av en enskild membranhelix kallad TM5, placerat i membranet ungefär tre nanometer från det katalytiska centret och nära den sannolika glukan-utgångskanalen. Nyckelaminosyror i detta område omfamnar läkemedlets hydrofoba kärna och kontaktar dess syrade svans, medan dess sockergrupp knappt rör vid proteinet — vilket förklarar varför kemister kunnat modifiera den delen utan att förlora verkan.
Läkemedel som fryser ett rörligt maskineri
Pvid första anblick ser enzymets övergripande form med och utan enfumafungin nästan oförändrad ut. Den avgörande skillnaden ligger i hur de omgivande lipiderna organiseras och hur flexibla vissa helixar är. När läkemedlet binder roterar en närliggande aromatisk sidokedja för att klämma fast enfumafungin, och tillsammans med en annan rest stabiliserar den en ordnad lipid intill läkemedlet. Ytterligare sterolliknande lipider ordnas snyggt runt ett set horisontella helixar som hjälper till att definiera vägen för glukanexport. Dessa lipider fungerar som kil och stöd, låser helixarna och kanalens ingång i en särskild ”basal” konfiguration. Genetiska tester visar att förändringar i många av kontaktpunkterna för läkemedlet eller dessa steroler försvagar läkemedelsbindningen eller förstör enzymfunktionen, och mutationer i dessa lägen överensstämmer med kända resistensmutationer i mänskliga och växtpatogener.
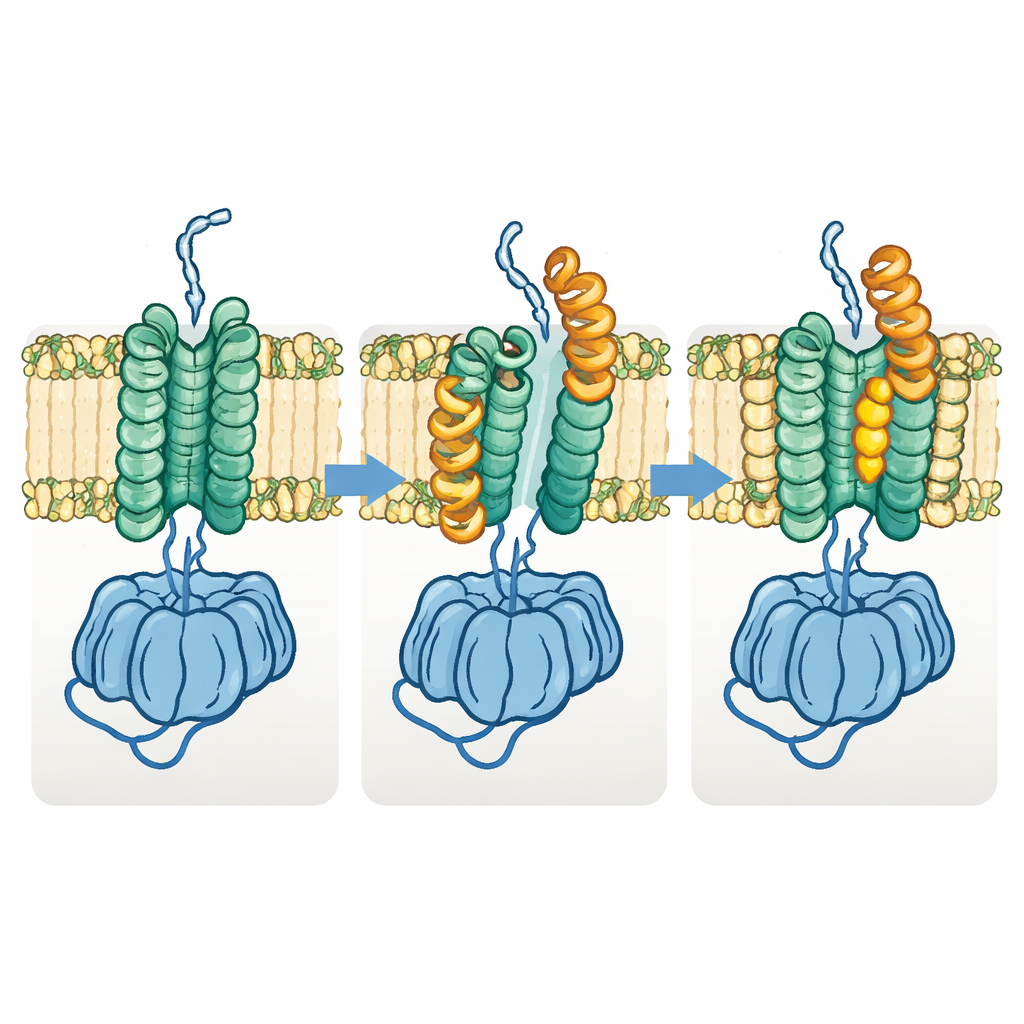
En nödvändig formförändring för polymertransport
Teamet upptäckte också en distinkt ”öppen” form av Fks1. I detta tillstånd förskjuts ena halvan av membranregionen sidleds och viktiga horisontella helixar svänger utåt, vilket öppnar utrymmet mellan de två membranpaketen och vidgar den uppenbara glukantunneln. Jämförelser av många strukturer tyder på att enzymet cyklar mellan den basala och den öppna formen under normal funktion: det basala tillståndet förbereder och initierar polymerkedjebildning, medan det öppna tillståndet tillåter den växande kedjan att röra sig lateralt genom membranet mot utsidan. När författarna konstruerade disulfidbindningar avsedda att låsa enzymet permanent i något av tillstånden, förlorade båda varianterna till stor del aktiviteten, vilket stöder idén att denna formförändring är avgörande för funktionen.
Vad detta betyder för framtida svampmedel
Genom att visa att enfumafungin och relaterade läkemedel inte verkar genom att blockera det katalytiska facket utan genom att omforma den lokala membranmiljön och frysa glukan-syntasen i dess basala tillstånd, avslöjar denna studie en okonventionell verkningsmekanism. Den visar också att Fks1 och Fks2 har nästan identiska strukturer och läkemedelssvar, vilket förklarar varför båda måste beaktas när man tacklar resistens. Mer generellt lyfter arbetet fram hur små molekyler kan kontrollera ”odrogerbara” membranproteiner genom att binda ytliga ytor och rekrytera lipider, och erbjuder en konceptuell ritning för att utforma nästa generationens svampmedel som förblir effektiva även när svampar utvecklas.
Citering: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Nyckelord: svampmedel, svampcellvägg, glukan-syntas, läkemedelsresistens, kryo-elektronmikroskopi