Clear Sky Science · sv
Cryo-EM-strukturer av bakteriofag T4:s portal-halsmonteringsintermediärer avslöjar en mekanism för kvarhållande av viral genom
Hur ett virus håller sitt DNA under tryck
Bakteriofag T4 är ett virus som infekterar E. coli-bakterier och packar sitt DNA så tätt i sitt huvud att trycket inuti kan vara fem till sju gånger högre än i en champagneflaska. Ändå läcker inte DNA:t ut medan viruset bygger färdigt resten av sitt skal. Denna studie visar i molekylär detalj hur T4 löser problemet med en liten dubbelgrind som fungerar som en luftsluss för dess genetiska material.
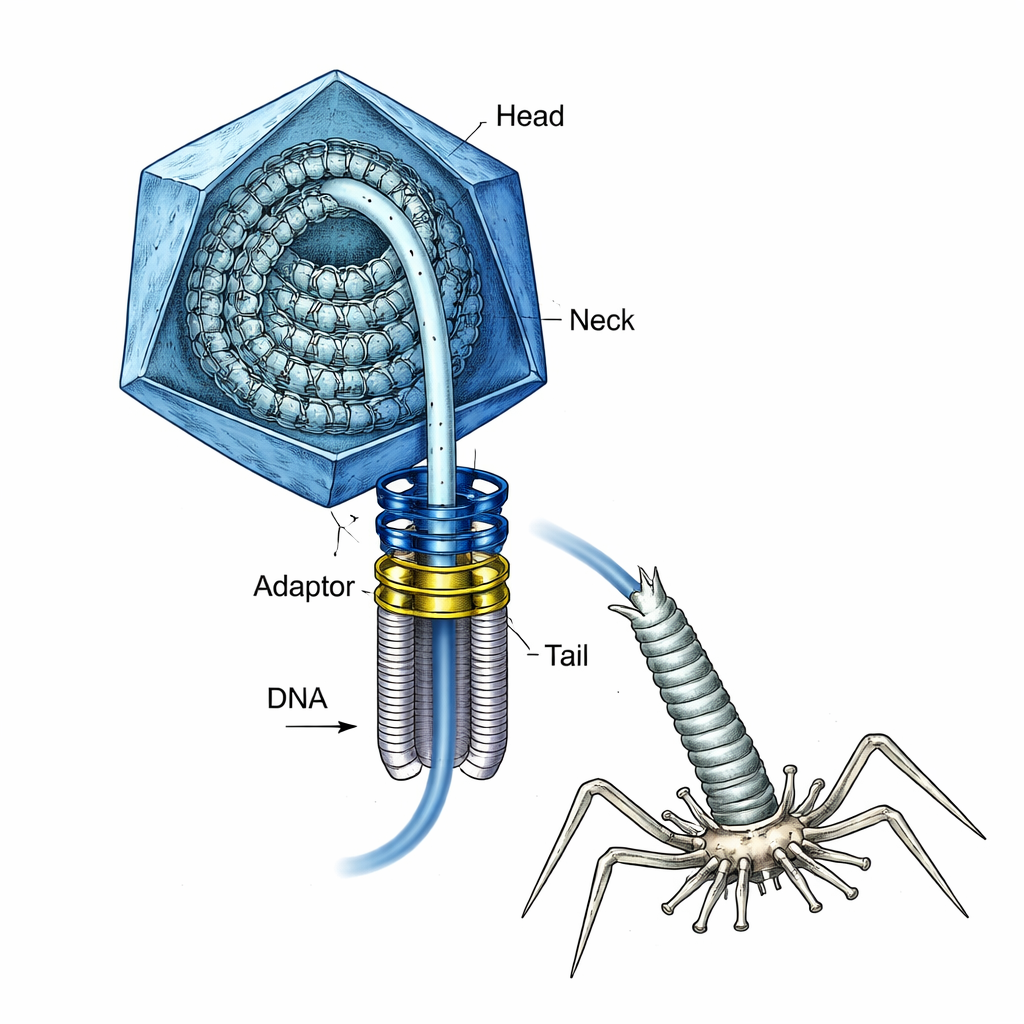
Viruset med en uppspänd fjäder inuti
T4 har länge varit en arbetsmyra inom molekylärbiologi och är också en modell för att bygga framtida vacciner och verktyg för genleverans. Under montering bygger viruset först ett tomt proteinskal, eller huvud, och en särskild ringformad ”portal” vid en spets. En kraftfull molekylär motor drar sedan in DNA:t i huvudet genom denna portal tills huvudet är "fullt." Vid den punkten måste motorn släppa, en hals och en svans måste fästas, och senare måste DNA:t injiceras i en bakterie—allt utan att det högtryckta DNA:t forceras ut i förtid. Hur viruset höll detta starkt belastade DNA säkert under dessa övergångar var inte väl förstått.
Återskapande av halsen i laboratoriet
Forskarlaget återskapade nyckelkomponenter av T4 i bakterier och blandade dem under kontrollerade former för att iaktta hur halsen—kopplingen mellan huvud och svans—monteras. Två virusproteiner, kallade gp13 och gp14, producerades separat. Ensamma flöt de som enhetsmolekyler, men tillsammans klickade de ihop sig i staplade ringar som bildar en central tunnel för DNA-passage. Till forskarnas förvåning dök ett tredje protein upp i dessa preparat: Hfq, ett välkänt bakteriellt protein som vanligtvis hjälper till att reglera RNA och genaktivitet i E. coli. Masspektrometri bekräftade att Hfq binder specifikt till gp14, vilket antyder att viruset lånar detta värdprotein som en del av sin hals.
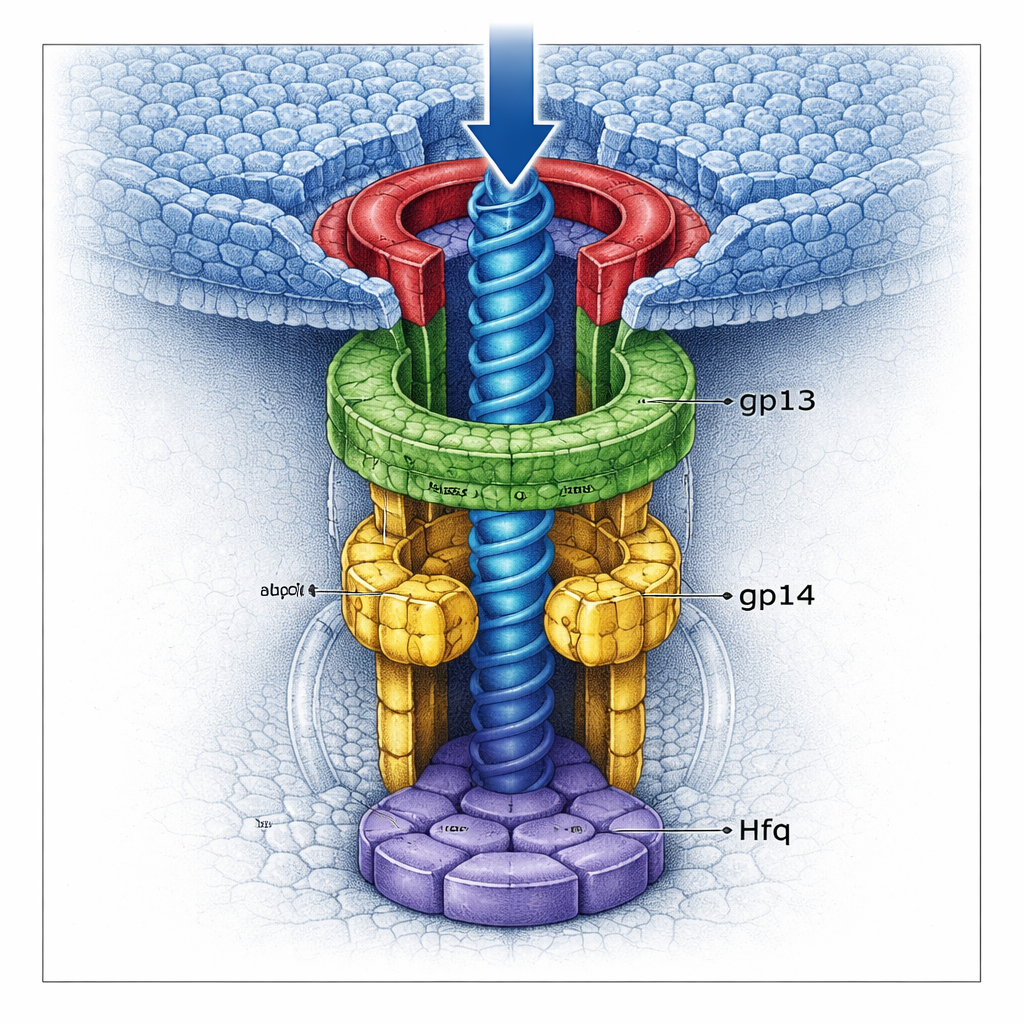
En dubbelgrind som låser in genomet
Med hjälp av högupplöst kryo-elektronmikroskopi visualiserade teamet flera varianter av halskomplexet i nästan atomär detalj. De fann att gp13 bildar en bred ring som anpassar sig till portalen, medan gp14 sitter under den som en hexamer och skapar en smalare kanal. Avgörande är att varje gp14-subenhet bidrar med en lång slinga som svänger in i mittpartiet av tunneln. Tillsammans bildar sex sådana ”stopp-slings” en tät grind som kan fånga den sista DNA-segmentet när det försöker lämna huvudet. Under gp14 monterar det kapade Hfq-proteinet sig också i en egen hexamer och tätar kanalens botten som en andra dörr. När Hfq är närvarande är gp13–gp14-strukturen mer komplett och stela, och de kombinerade grindarna drar ihop tunneln ännu mer, vilket kraftigt minskar risken för DNA-läckage.
Tajming, felsäkring och en lånad hjälpare
Studien visar också att detta system är mer än en statisk plugg; det är en omsorgsfullt koreograferad sekvens av formförändringar. När huvudet är fullt trycker det inre trycket portalen till en ny konformation som blottar bindningsytor för gp13. En förmonterad gp13–gp14–Hfq-hals dockar sedan på portalen. Gp13 böjer sig, svänger uppåt och låser fast vid både portalen och det yttre skalet, vilket väver fast halsen i huvudet. Under hela detta skede håller gp14:s stopp-slingor och Hfq-pluggen DNA:t på plats. Hfq spelar en andra roll som kvalitetskontroll: genom att ockupera viktiga ytor på gp14 förhindrar det att gp14 binder portalen i fel position, vilket annars skulle leda till felmontering av halsen. Först när den förbyggda svansen anländer bildar ett svanstippprotein, gp15, ett ännu starkare bindemedel med gp14, tränger undan Hfq och öppnar vägen för kontrollerad frisättning av DNA in i svansen.
Varför detta är viktigt bortom ett enda virus
Enkelt uttryckt använder T4 ett tvådörrars säkerhetslås för att hålla tillbaka en kraftfull DNA-"fjäder" medan det färdigställer resten av viruset. Den första dörren byggs av dess egna halsprotein, gp14, och den andra dörren lånas från värdens Hfq-protein, som viruset använder tillfälligt och sedan överger. Denna dubbelgrind säkerställer att nästan inget DNA går förlorat och att det färdiga viruset är fullt infektöst. Eftersom många stora virus packar sina genom under liknande extrema tryck och delar besläktad arkitektur, antyder arbetet att jämförbara grindmekanismer, och till och med tillfällig kapning av värdproteiner, kan vara utbredda. Att förstå dessa mekanismer kan vägleda utformningen av säkrare virala vektorer för medicin och peka på nya sätt att blockera skadliga virus genom att rikta in sig på deras genom-"lås."
Citering: Han, L., Mao, Q., Zhu, J. et al. Cryo-EM structures of bacteriophage T4 portal-neck assembly intermediates reveal a viral genome retention mechanism. Nat Commun 17, 1964 (2026). https://doi.org/10.1038/s41467-026-69107-7
Nyckelord: bakteriofag T4, viral montering, kryo-elektronmikroskopi, genompackning, värd–virusinteraktion