Clear Sky Science · sv
In situ-strukturer av portal-hals-stjärt-komplexet hos bakteriofag T4 belyser en mekanism för positionering av virusgenomet
Hur ett virus laddar sin genetiska fjäder
Bakteriofager — virus som infekterar bakterier — är bland naturens mest sofistikerade nanomaskiner. En av de mest välstuderade, bakteriofag T4, måste pressa sitt långa DNA-genom in i ett pyttelitet huvud och sedan skjuta in det i en bakterie på ett ögonblick. Den här studien visar, nästan atom för atom, hur T4 noggrant positionerar sitt DNA som en komprimerad fjäder inne i stjärten, redo att avfyras in i en ny värdcell utan att förlora så mycket som en enda genetisk “bokstav.” 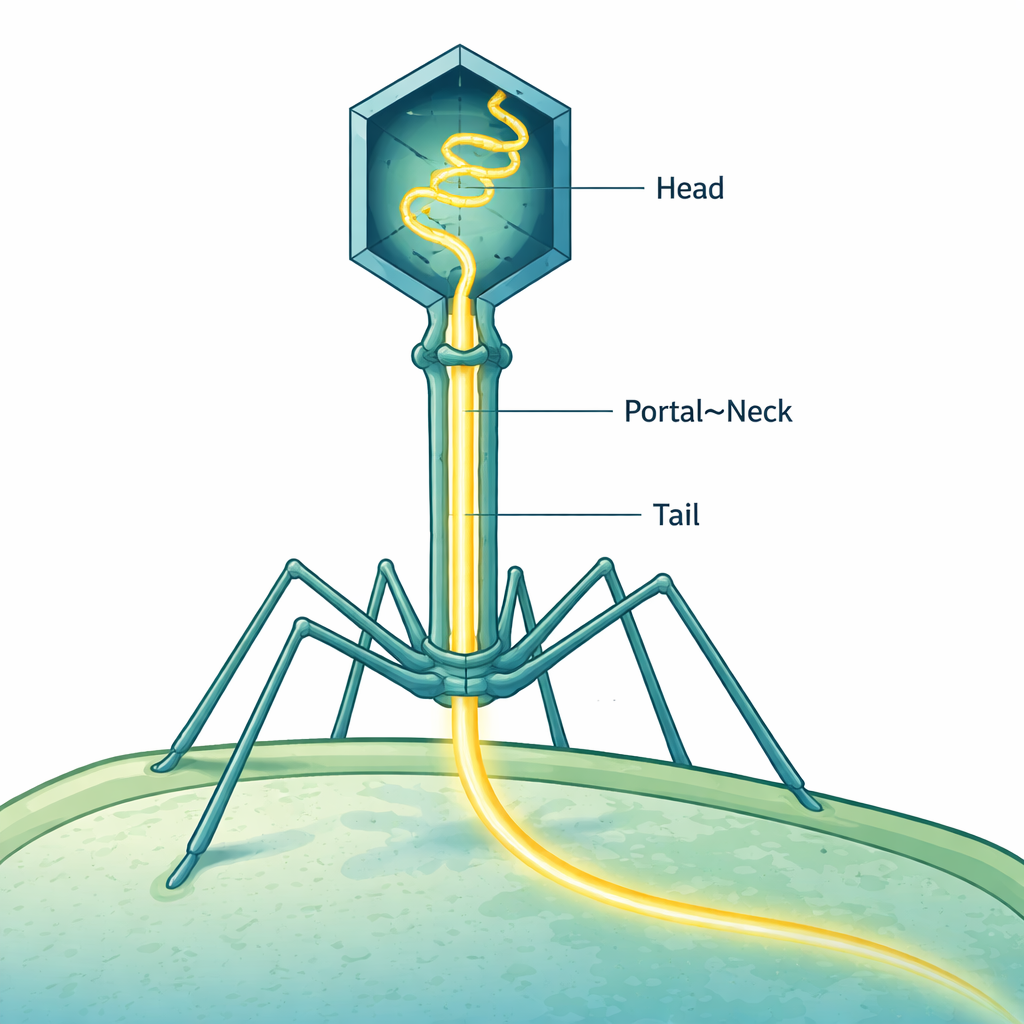
En högtryckshölje
Inuti fagets proteinskal pressas DNA:t till nästan kristalldensitet, vilket skapar ett inre tryck på ungefär 25–35 atmosfärer — liknande trycket i djuphavssänkor. Författarna använde högupplöst kryo-elektronmikroskopi för att visualisera vad som händer vid den särskilda ”porten” genom vilken DNA kommer in och går ut ur huvudet. De fann att när huvudet blir fullt ändrar den ringformade portalproteinet form från en flygande tefat-liknande struktur till en svampliknande form och förskjuts nedåt i förhållande till skalet. Denna tryckdrivna förskjutning verkar signalera att tillräckligt med DNA har paketerats, vilket utlöser att motorn som pumpade in DNA lossnar och blottar nya dockningsytor för nästa del av virusmaskineriet.
Bygger en låsande hals mellan huvud och stjärt
När DNA-huvudet är fullt monteras en halsstruktur mellan huvud och stjärt, som fungerar både som förbindelse och ventil. Två halsproteiner, kallade gp13 och gp14, bildar ringar under portalen. Gp13 svänger upp en del av sin struktur för att gripa portalen och når också ut till det omgivande skalet, binder samman huvud och hals tätt och erbjuder fästpunkter för dekorativa fibrer. Gp14, som sitter nedanför, bildar ursprungligen en dubbel ”genomport” tillsammans med ett värdprotein kallat Hfq och tätar effektivt utgångskanalen så att det högtryckta DNA:t inte läcker ut i förtid. I detta tillslutna tillstånd stoppas DNA:t nära halsen och hålls på plats medan resten av viruset färdigmonteras.
Stjärtdockning öppnar porten
Nästa steg är att fästa en förbyggd stjärt, som består av ett innerör omringat av en kontraktil hölje och avslutas i en komplex basplatta som känner igen bakterieytan. Överst på den här stjärten finns en ”stjärtterminator”-ring, gp15, och strax under den kapslar en annan ring, gp3, inneröret. När stjärten dockar mot halsen genomgår gp14 en dramatisk omarrangering: dess loopar som bildar porten roterar nedåt och klämmer fast vid gp15, medan en utdragen svans av gp14 sveper runt gp15 och bildar ett mycket stort, laddat gränssnitt. Dessa rörelser fördriver Hfq-stoppet och svänger gp14-looparna åt sidan, vilket förvandlar den tidigare stängda halsen till en helt öppen kanal som nu linjerar upp med stjärtens håliga rör.
DNA fångas av en molekylär måttstock
Med porten öppen spillr inte det högtryckta DNA:t fritt ut. Istället färdas det cirka 17 nanometer ned genom den nybildade portal–hals–stjärt-förbindelsen. Vid skarven med gp3 och toppen av stjärtröret möter det ”måttbandsproteinet” (TMP), ett långt spiralformat protein som ursprungligen fungerade som en måttstock för att bestämma stjärtens längd. TMP:s ände har DNA-bindande segment som tar tag i genomets spets. Fortsatt tryck från det packade huvudet skjuter sedan detta DNA–TMP-komplex vidare ner i stjärtröret, komprimerar TMP:s coiled-coil-segment som en fjäder och flyttar DNA-spetsen till botten av den andra ringen i stjärtröret. 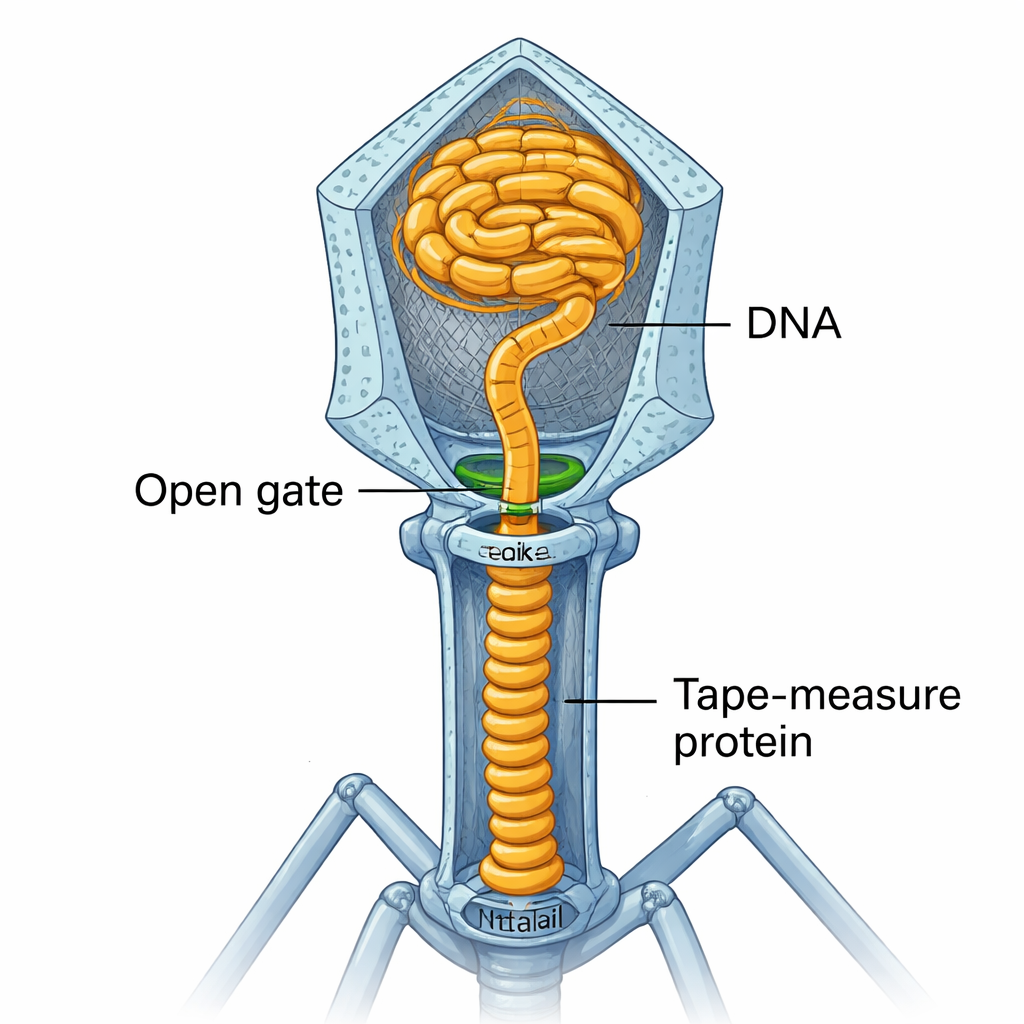
En fjäderuppspänd genom klar att avfyras
Dessa strukturella ögonblicksbilder visar att efter assemblage är faggenomet inte bara förvarat i huvudet; det är avsiktligt positionerat så att dess ledande ände är upphängd djupt inne i en intern tunnel som löper från huvudet, genom halsen och in i stjärten. DNA:t hålls där av det komprimerade måttbandsproteinet och en ”propp” vid basplattan, vilket upprätthåller ett metastabilt, fjäderuppspänt tillstånd. När basplattan känner av och låser fast vid en bakteriell receptor utlöser den förändringar som tar bort denna propp och tillåter det komprimerade DNA–TMP-komplexet att rusa framåt och styra genomet smidigt in i värdcellen. I korthet har viruset utvecklat ett tryckdrivet laddnings- och siktssystem som säkerställer snabb, komplett och pålitlig leverans av sitt genetiska last.
Citering: Fokine, A., Zhu, J., Klose, T. et al. In situ structures of the portal-neck-tail complex of bacteriophage T4 inform a viral genome positioning mechanism. Nat Commun 17, 1965 (2026). https://doi.org/10.1038/s41467-026-69106-8
Nyckelord: bakteriofag T4, packning av viralt DNA, kryoelektronmikroskopi, virusstruktur, faginfektionsmekanism