Clear Sky Science · sv
Strukturell grund för pauser under transkriptionsinitiering i Mycobacterium tuberculosis
Hur en bakteries genströmbrytare kan stanna upp
Mycobacterium tuberculosis, bakterien som orsakar tuberkulos, måste ständigt slå av och på gener för att överleva i kroppens hårda miljö. Arbetet som beskrivs här skymtar in i ett av de tidigaste stegen i denna genetiska reglering och fångar en flyktig ”paus” som uppstår just när cellen börjar läsa DNA till RNA. Att förstå denna paus hjälper oss förklara hur mikroben avgör om den ska fullfölja aktiveringen av en gen eller avbryta försöket — och kan så småningom blottlägga nya svaga punkter för antibiotika.
Att starta budskapet från DNA
I bakterier rör sig en stor proteinkomplex som kallas RNA-polymeras längs DNA för att tillverka RNA, det första steget mot att producera proteiner. För att börja samarbetar det med hjälpproteiner kända som sigmafaktorer som vägleder det till specifika startplatser på DNA och hjälper till att öppna en liten ”bubbla” i dubbelspiralen. För Mycobacterium tuberculosis är en sådan hjälpare, kallad sigma E, särskilt viktig när bakterien befinner sig under stress utanför sitt inre cellmembran. En annan faktor, CarD, hjälper till att stabilisera den öppna DNA-bubblan. Tillsammans bildar dessa aktörer ett initieringskomplex som gör de första byggstenarna av RNA innan det antingen förbinder sig till ett fullängdsmeddelande eller ger upp och släpper korta RNA-fragment.
En dold paus vid sex eller sju bokstäver lång
Tidigare biokemiska och enkelmolekylstudier hade antytt att RNA-polymeras ofta pausar mycket tidigt, när den nya RNA-strängen bara når sex eller sju byggstenar i längd. Men dessa pauser är extremt korta och svåra att se direkt, så inga högupplösta strukturer fanns tillgängliga. I denna studie använde författarna kryo-elektronmikroskopi för att frysa och visualisera flera versioner av initieringsmaskineriet från M. tuberculosis. De konstruerade DNA–RNA-stommar som fångar komplexet när RNA:t är sex eller sju enheter långt och löste strukturer för tre huvudsakliga tillstånd: två ”vanliga” initieringskomplex och ett distinkt pausat initieringskomplex.
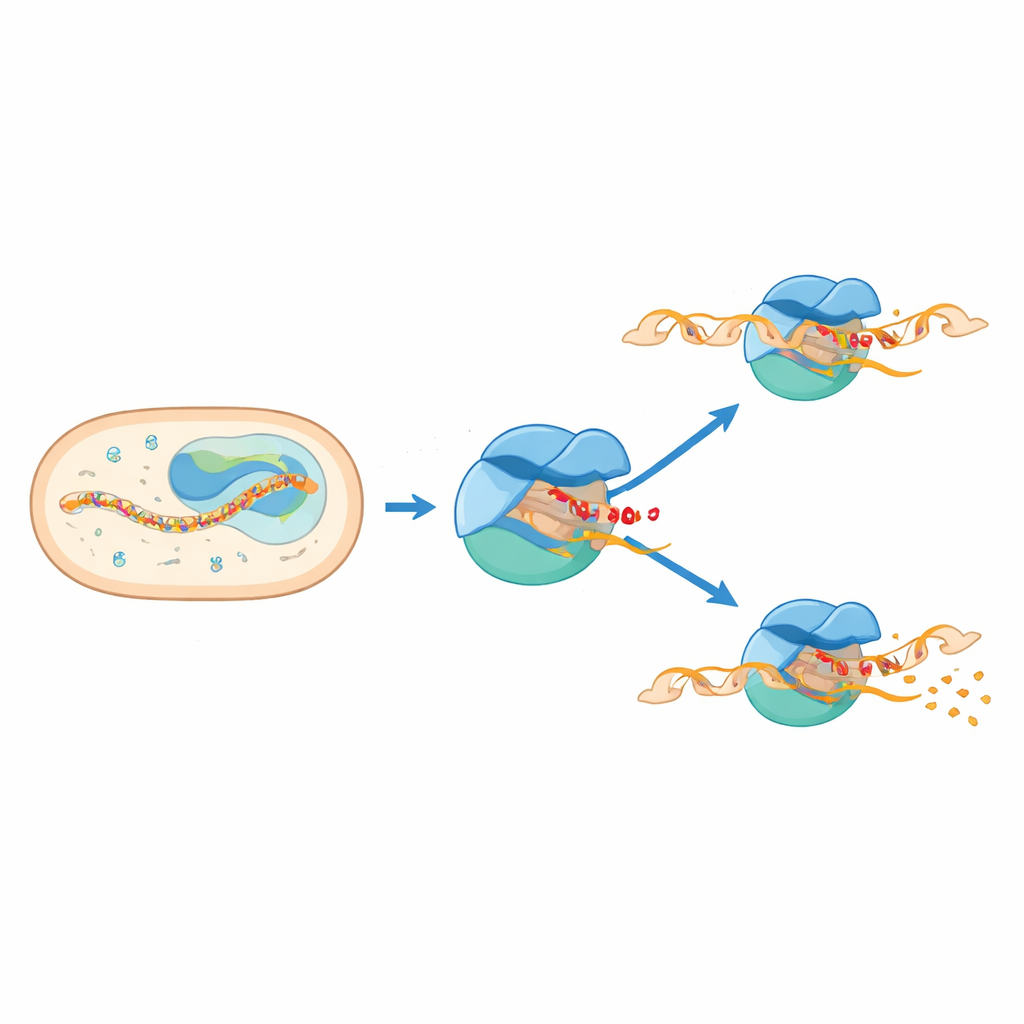
När två delar av maskineriet kolliderar
Strukturerna visar att pausen uppstår när två delar av maskineriet försöker inta samma utrymme. Ett flexibelt segment av sigma E, känt som 3.2-regionen, skjuter in i kanalen där det växande RNA:t måste passera för att lämna enzymet. När RNA:t förlängs till sex eller sju enheter kolliderar dess främre ände med den utstickande loopen. Den kollisionen tvingar en svängningsrörelse av en stor modul inom RNA-polymeraset och förvränger ett nyckelstrukturellt element kallat bridge-helix. Samtidigt dras DNA strax uppströms om den aktiva ytan inåt och delvis löses upp, vilket bildar en ”skrumpnad” och knäckt bubbla. Dessa sammankopplade rörelser låser komplexet i ett pausat, halvframflyttat tillstånd som lagrar mekanisk spänning.
En formförändrande hjälpare stadgar bubblan
CarD, den accessoarisk faktor, visar sig spela en mer mångsidig roll än man tidigare uppskattat. I det icke-pausade initieringskomplexet kilas CarD in i minorgrooven av en DNA-sträng vid bubbla-kanten och hjälper till att hålla bubblan öppen så att RNA-polymeraset kan börja syntesen. I det pausade komplexet skiftar CarD för att omfamna den motsatta, icke-mallsträngen av DNA och samarbetar med sigma E för att klämma den ihopskrumpna bubblan mer tätt. Biokemiska tester visar att CarD förstärker sigma E–beroende transkription och påverkar hur många RNA-molekyler som ackumuleras vid sex–sju-enhetsstadiet. Dessa fynd tyder på att CarD både stabiliserar det initiala öppna tillståndet och hjälper det pausade komplexet att undvika ett för tidigt kollaps.
En kontrollpunkt mellan misslyckande och åtagande
Genom att jämföra högupplösta strukturer bildade på delvis föröppnat DNA med lägre upplösta strukturer sammansatta på fullt matchat DNA visar författarna att samma grundläggande pausade former uppträder under mer naturliga förhållanden. De föreslår att kollisionen mellan det växande RNA:t och sigma 3.2-loopen skapar en energifylld kontrollpunkt vid sex till sju RNA-enheter. Från detta beredda tillstånd kan komplexet följa två huvudvägar: det kan släppa det korta RNA:t och återställa sig, ett abortivt försök, eller så kan det använda den lagrade spänningen för att bryta sig loss från promotorregionen och gå in i stabil, långvarig RNA-produktion. CarD:s ompositionering och sigmafaktorns försvagade grepp om uppströms DNA verkar styra detta beslut.
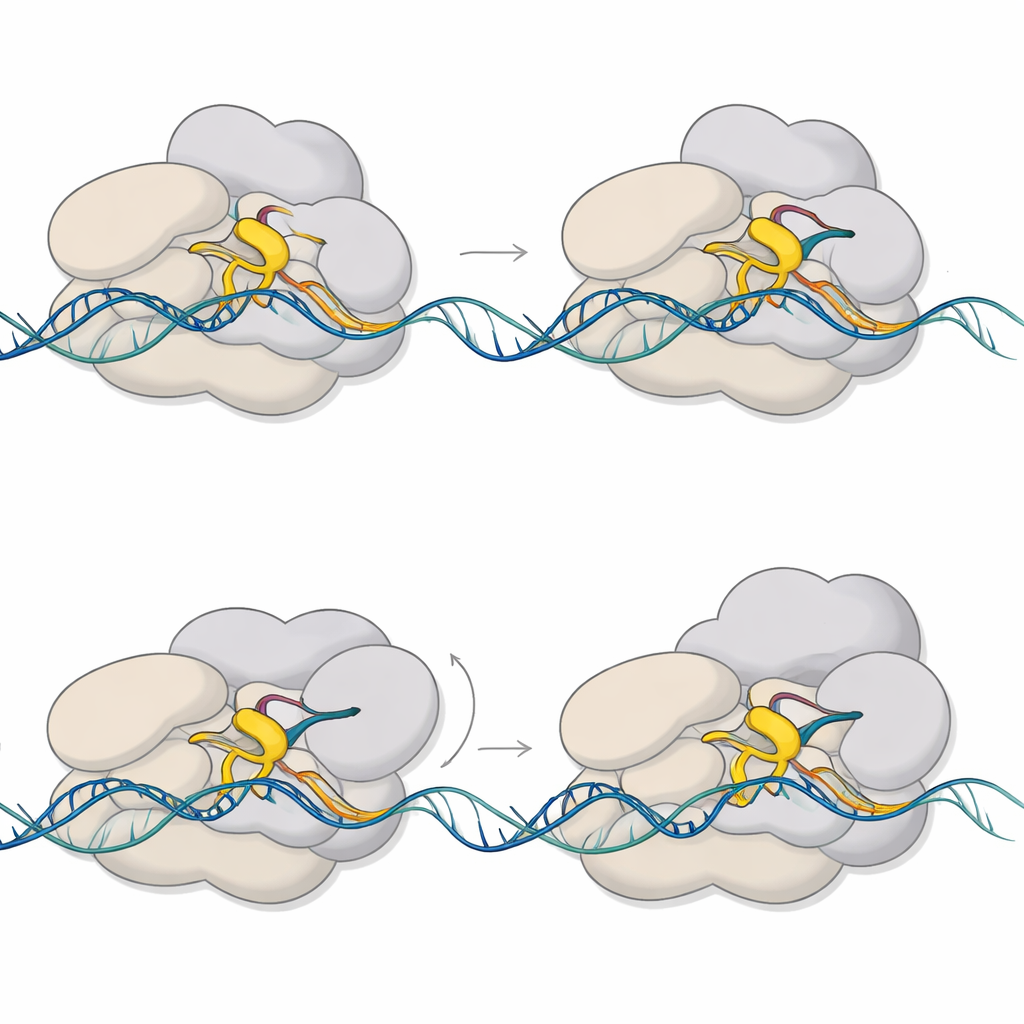
Varför detta är viktigt för tuberkulos
För en allmän läsare är huvudbudskapet att tuberkulosbakterien inte helt enkelt slår på gener som en lampa. I stället tvekar den vid en minimal RNA-längd och använder en kort mekanisk paus som en beslutsnod mellan att avbryta eller binda sig till full genaktivering. Detta arbete fångar den pausen i atomär detalj och visar hur en liten rörlig loop, en svängande kärna och en omformad DNA-bubbla tillsammans skapar en kontrollerbar kontrollpunkt. Eftersom sigma E och CarD är centrala för hur M. tuberculosis svarar på stress, skulle dessa insikter så småningom kunna hjälpa forskare att designa läkemedel som blockerar detta tidiga steg och försvagar bakteriens förmåga att anpassa sig och överleva.
Citering: Zheng, L., Xu, K. Structural basis of pausing during transcription initiation in mycobacterium tuberculosis. Nat Commun 17, 2197 (2026). https://doi.org/10.1038/s41467-026-69104-w
Nyckelord: initiering av transkription, RNA-polymeras pausering, Mycobacterium tuberculosis, sigmafaktorer, cryo-EM