Clear Sky Science · sv
scLong: en miljardparametrig grundmodell för att fånga långsiktig genkontext i enkelcells-transkriptomik
Lära datorer läsa cellernas dolda språk
Varje cell i din kropp rymmer en myllrande stad av gener som slås av och på i intrikata mönster. Modern enkelcells-RNA-sekvensering kan nu avlyssna varje enskild cell, men resultatet är en överväldigande flod av siffror. Denna artikel presenterar scLong, en massiv artificiell intelligensmodell utformad för att förstå dessa komplexa genaktivitetsmönster, inklusive svaga signaler som äldre metoder tenderar att ignorera. Målet är att hjälpa forskare förstå hur celler reagerar när gener stängs av, läkemedel tillförs eller sjukdomar tar fäste.
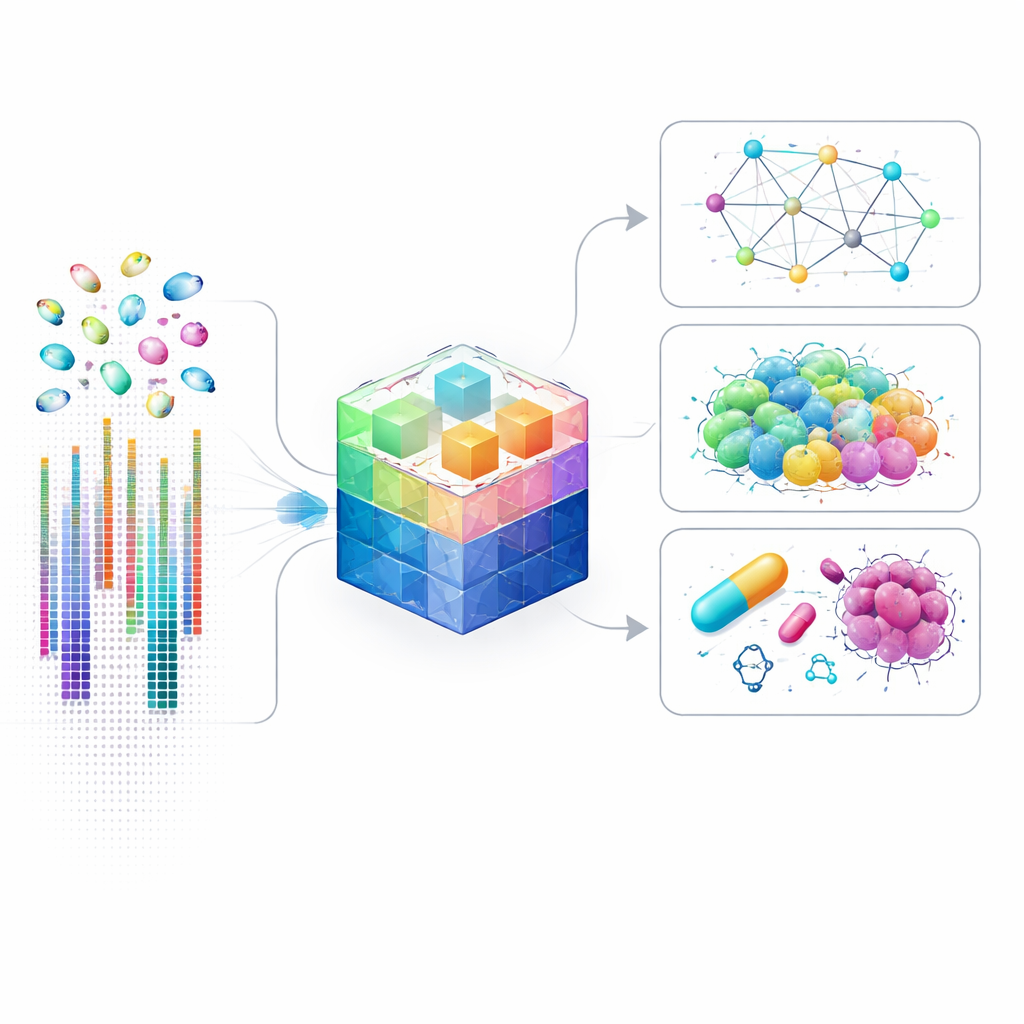
Varför genkartor på cellnivå är viktiga
Traditionella genstudier blandar ofta ihop miljontals celler, vilket jämnar ut sällsynta eller ovanliga celler. Enkelcellstekniker förändrade det genom att mäta genaktivitet i varje cell separat, vilket avslöjar dolda celltyper, subtil kommunikation mellan celler och detaljerade kontrollkretsar som bestämmer vad en cell kommer att göra. Att analysera denna typ av data är dock extremt utmanande: varje cell kan ha aktivitetsnivåer mätta för tiotusentals gener, många av dem knappt detekterbara. Befintliga AI-modeller förenklar problemet genom att fokusera endast på de mest högljudda generna, vilket snabbar upp beräkningarna men förbiser många subtila signaler som kan vara avgörande vid sjukdom, utveckling eller läkemedelsrespons.
En ny modell som lyssnar på varje gen
scLong tar sig an denna utmaning genom att skala upp i stället för att skära ner. Det är en miljardparametrig grundmodell tränad på genaktivitetsprofiler från cirka 48 miljoner humana celler över mer än 50 vävnader. Till skillnad från tidigare angreppssätt som uppmärksammar ett par tusen kraftigt aktiva gener, beaktar scLong ungefär 28 000 gener samtidigt, inklusive sådana som sällan eller svagt uttrycks. Den kombinerar två typer av information för varje gen: hur aktiv den är i en viss cell och vad som redan är känt om dess funktion från Gene Ontology, en stor expertgranskad katalog över geners roller och relationer. Ett specialiserat nätverk som arbetar på en graf av genkopplingar destillerar denna förkunskap till kompakta representationer som modellen kan använda tillsammans med de råa uttrycksvärdena.
Hur modellen balanserar kraft och effektivitet
Att undersöka varje gen i detalj är beräkningsmässigt dyrt, så scLong använder en smart tvåspårsdesign. Inom varje cell sorteras gener efter hur starkt de uttrycks. De mest aktiva generna, som ofta bär huvudbudskapet biologiskt, bearbetas genom en större, mer kraftfull uppmärksamhetsmodul. De tystare generna, inklusive låga och till och med nollmätningar, routas genom en mindre, lättare modul. Därefter sammanförs alla gener och passerar genom ett ytterligare uppmärksamhetslager som låter varje gen påverka varje annan. Denna design gör det möjligt för modellen att behålla billigare men ändå meningsfulla representationer för svaga signaler samtidigt som den reserverar mer kapacitet för de starkaste. Under förträning döljer systemet upprepade gånger en del av genaktivitetsvärdena och lär sig rekonstruera dem från den omgivande kontexten, vilket tvingar modellen att upptäcka mönstren som länkar generna till varandra.
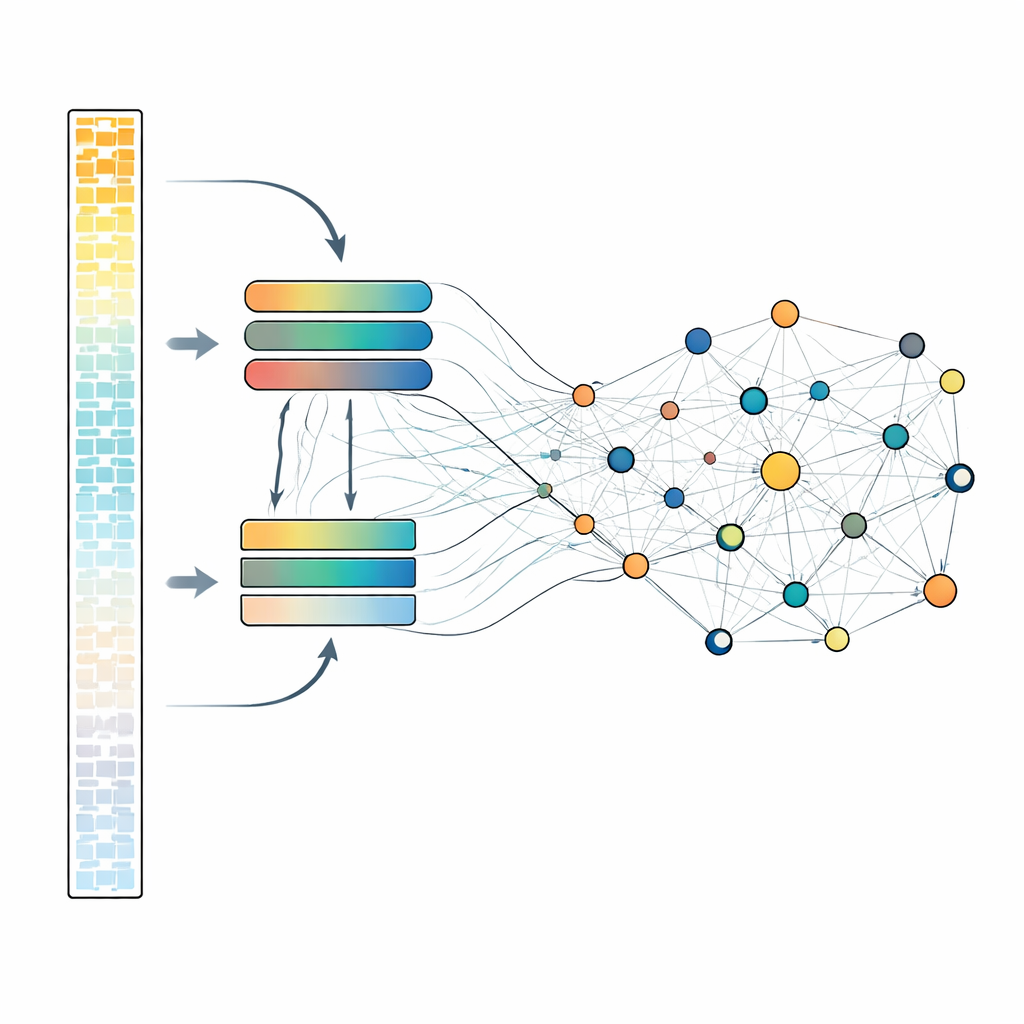
Tillämpning på verkliga problem
När den har tränats kan scLong anpassas till ett brett spektrum biologiska frågor. Författarna visar att den förutsäger hur genaktivitet kommer att ändras när specifika gener stängs av eller förändras, inklusive kombinationer av två gener som kan samverka. Den förutspår också hur celler reagerar när de exponeras för olika kemikalier, vilket är viktigt för läkemedelsupptäckt och säkerhetstester. I cancerstudier hjälper scLong att förutse hur tumörcellinjer kommer att reagera på enkla läkemedel och på läkemedelspairer som kan fungera bättre i kombination, och presterar ofta bättre än både specialiserade modeller och andra stora grundmodeller. Utöver prediktion kan scLong härleda nätverk av regulatoriska relationer mellan gener och kan hjälpa till att korrigera tekniska förvrängningar som uppstår när data samlas in på olika laboratorier eller med olika instrument.
Vad detta betyder för framtidens medicin och forskning
Enkelt uttryckt ger scLong forskare en högupplöst, kontextmedveten karta över genaktivitet inne i enskilda celler, en karta som inte kastar bort de tysta eller sällan använda generna. Genom att lära av miljontals celler och inkorporera befintlig biologisk kunskap erbjuder den mer precisa gissningar om hur celler kommer att reagera när gener störs, när nya läkemedel introduceras eller när sjukdomsprocesser utvecklas. Detta kan påskynda sökandet efter nya terapier, vägleda mer personligt anpassade behandlingsval och skärpa vår förståelse för hur komplexa gen nätverk styr hälsa och sjukdom. Även om modellen är stor och beräkningskrävande pekar den mot en framtid där kraftfulla, allmängiltiga AI-system fungerar som mångsidiga följeslagare för att utforska cellernas dolda mekanismer.
Citering: Bai, D., Mo, S., Zhang, R. et al. scLong: a billion-parameter foundation model for capturing long-range gene context in single-cell transcriptomics. Nat Commun 17, 2380 (2026). https://doi.org/10.1038/s41467-026-69102-y
Nyckelord: single-cell transcriptomics, foundation models, gene regulation, drug response prediction, gene expression