Clear Sky Science · sv
En kombinatorisk syntetisk strategi för att utveckla proteinkompletteringsmedel för genredigering riktade mot musens näthinna
Nytt hopp för behandling av ärftlig blindhet
Många former av ärftlig blindhet börjar med en enda felaktig gen i de ljuskänsliga cellerna längst bak i ögat. Moderna genredigeringsverktyg som CRISPR kan i princip rätta till dessa fel, men att få redigeringsmaskineriet säkert in i rätt celler har varit ett stort hinder. Denna studie beskriver ett nytt sätt att föra kraftfulla genredigerare direkt in i musnäthinnan med hjälp av särskilt utformade fettliknande partiklar, vilket öppnar för möjligheten till engångsbehandlingar som återställer synen hos personer med genetiska ögonsjukdomar.
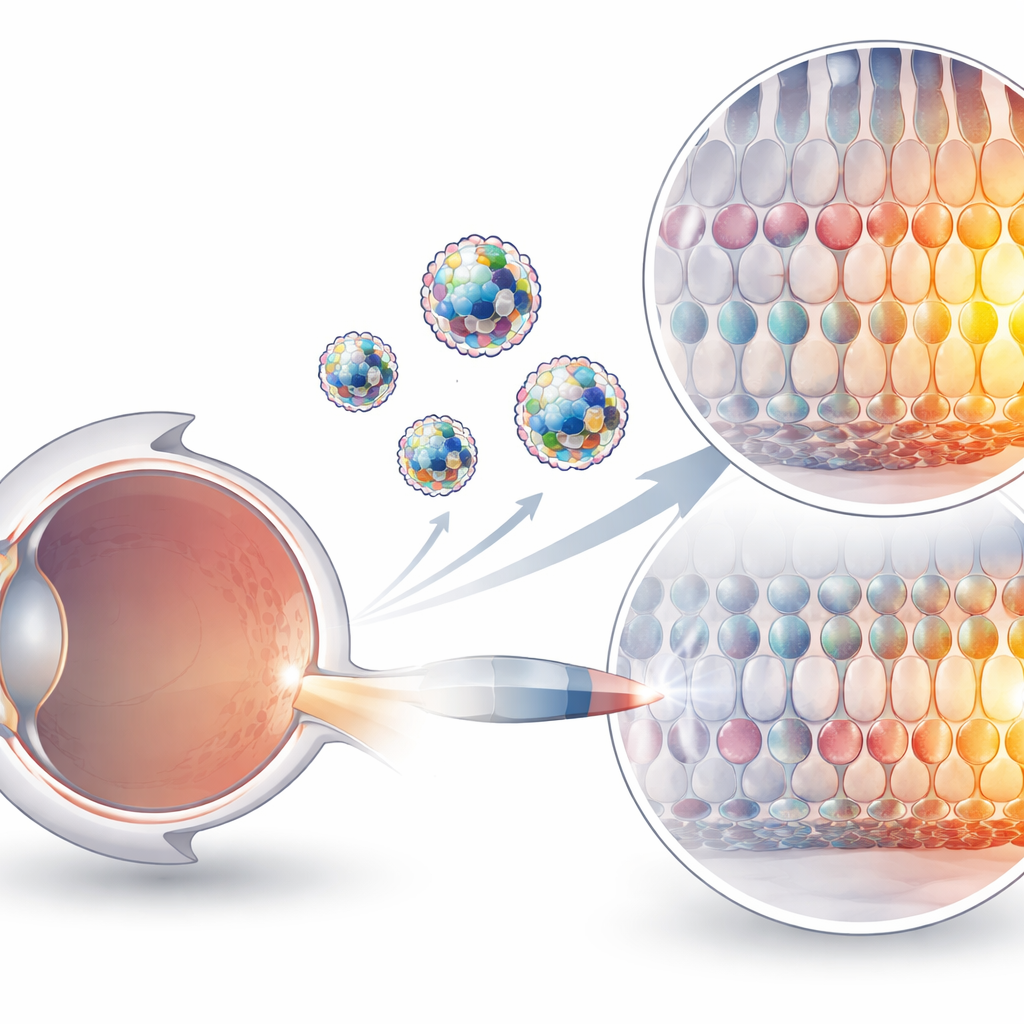
Varför det är så svårt att leverera genredigerare
CRISPR-baserade verktyg kan nu förändra enskilda DNA-bokstäver utan att klippa båda strängarna, en förbättring som gör dem attraktiva för behandling av genetiska sjukdomar. Men dessa verktyg är skrymmande protein–RNA-maskiner, elektriskt laddade och känsliga i kroppen. Nuvarande leveransmetoder förlitar sig till stor del på modifierade virus eller på partiklar som bär de genetiska ritningarna för redigeraren snarare än redigeraren själv. Virus kan framkalla immunreaktioner och har strikta storleksbegränsningar, medan leverans av budbärar-RNA fungerar mycket bra i levern men förblir ineffektivt i många andra vävnader, inklusive ögat. Att injicera förmonterade protein–RNA-komplex direkt är konceptuellt renare och säkrare, men de har saknat ett lämpligt fordon för att hjälpa dem passera cellmembran och nå sina mål.
En färginspirerad färja för proteiner
Forskarlaget började från en oväntad utgångspunkt: Coomassie Brilliant Blue, ett djupt blått färgämne som ofta används i biolaboratorier och redan godkänts för vissa ögonoperationer. Detta färgämne binder hårt till många olika proteiner. Teamet kopplade kemiskt Coomassie-"huvuden" till fettliknande "svansar" för att skapa en familj av nya molekyler kallade lipidoider. I vatten tenderar dessa lipidoider att klustra till partiklar, med de oljiga delarna begravda inuti och Coomassie-grupperna exponerade utåt där de kan gripa tag i proteiner. Genom att variera svansarnas längd, förgrening och laddning byggde forskarna flera dussin kandidatföreningar utformade för att binda genredigerande proteiner på ena sidan och interagera med cellmembran på den andra.
Test av proteinleverans till ögonceller
För att se vilka konstruktioner som faktiskt fungerade använde gruppen först ett enkelt testprotein kallat Cre-rekombinas som vänder en genetisk switch från grönt till rött eller rött till grönt fluorescens i konstruerade celler och möss. Flera Coomassie-lipidoider förde effektivt in Cre i odlade celler och gjorde stora andelar av cellerna från gröna till röda. När de injicerades under näthinnan hos rapportermöss utlöste utvalda föreningar påfallande färgförändringar både i pigmentlagret som stödjer synen och i de ljuskännande fotoreceptorerna, vilket visar att proteinerna nådde just de celler som påverkas vid många blinda sjukdomar. Dessa tidiga experiment visade också att subtila förändringar i lipidoidstrukturen kunde förskjuta vilka celttyper som riktades, vilket antyder att framtida varianter kan finjusteras för specifika näthinneskikt.
Förstärkt genredigering och återställd syn
Nästa steg var att lasta systemet med en adeninebasredigerare, en förfinad CRISPR-variant som kan rätta den specifika enkla nukleotidmutation som orsakar synförlust i rd12-möss, en modell för svår barndomsblindhet. Redigerarens protein–RNA-komplex trängde dåligt in i celler på egen hand. En lipidoid, kallad CBB11, förbättrade leveransen men tenderade att klumpa ihop sig i lösning. För att stabilisera den inbäddade forskarna CBB11 i små, väldefinierade liposomer—ihåliga sfärer gjorda av flera lipidsorter, inklusive kliniskt använda komponenter från mRNA-vacciner. I dessa formulationer grep CBB11 på liposomens yta tag i protein-delen av redigeraren, medan andra lipider hjälpte till att binda RNA-guiden, och skapade ett kooperativt skal som höll hela komplexet på partikelns yta.
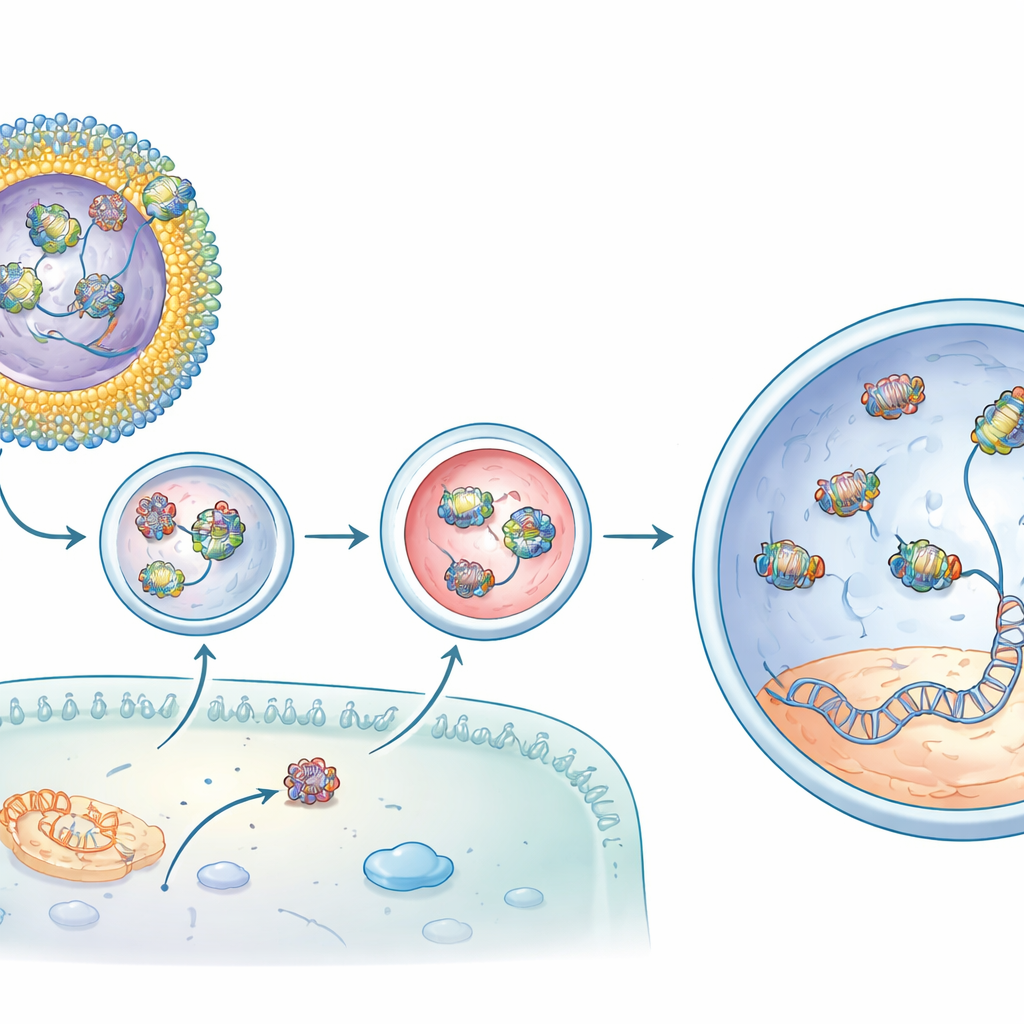
Från molekylär reparation till återställda ljussvar
När dessa CBB11-innehållande liposomer som bar basredigeraren injicerades under näthinnan hos rd12-möss var resultaten slående. Jämfört med redigerare injicerad ensam ökade den optimerade formuleringen den önskade DNA-korrigeringen i målgenen med långt mer än en tiopotens och producerade ännu högre nivåer av korrigerat budbärar-RNA. Kemisk analys visade återhämtning av det ljuskänsliga retinala pigment som saknas vid sjukdomen. Mest övertygande var att elektriska inspelningar från djurens ögon visade att deras stavceller återfick en stor del av sin förmåga att reagera på svagt ljus—upp till ungefär tre fjärdedelar av signalen hos en normal mus i de bästa fallen. Oönskade ändringar på andra ställen i genomet låg på bakgrundsnivåer, vilket tyder på att redigeringen var både potent och precis.
Vad detta kan betyda för framtida ögonbehandlingar
För en icke-specialist är huvudbudskapet att författarna har byggt en återanvändbar "skolbuss" för genredigerande proteiner som fungerar direkt i det levande ögat. Genom att dekorera säkra, vaccinliknande fettpartiklar med ett proteingripande färgämne skapade de ett system som kan fånga olika redigerare på sin yta, leverera dem in i näthinnans celler, korrigera sjukdomsframkallande mutationer och mätbart återställa synen hos möss efter en enda behandling. Även om mer arbete krävs för att fullt ut bedöma säkerheten, förbättra riktningen och anpassa metoden för mänsklig användning, pekar denna plattform mot framtida engångs-precisionsterapier för ärftliga retinala sjukdomar och möjligen andra genetiska tillstånd där noggrann, lokaliserad DNA-reparation kan göra skillnaden mellan blindhet och syn.
Citering: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Nyckelord: retinal genbehandling, CRISPR basredigering, liposomer, proteinleverans, ärftlig blindhet