Clear Sky Science · sv
Insikter i strukturen och regleringen av mänskliga TWIK-2
Varför denna lilla grind i våra celler spelar roll
Långt inne i våra celler styr mikroskopiska portar av protein flödet av laddade atomer, vilket formar hur nerver avfyrar, hur blodkärl drar ihop sig och hur vårt immunsystem reagerar. En sådan port, kallad TWIK-2, har kopplats till högt blodtryck i lungorna och skadlig inflammation, men fram tills nu visste forskare mycket lite om hur den är uppbyggd eller hur den kan kontrolleras med läkemedel. Denna studie avslöjar den detaljerade strukturen hos mänskliga TWIK-2, visar dess elektriska beteende och skisserar hur den kan riktas för att utveckla nya antiinflammatoriska läkemedel.
En tyst kanal med stora hälsoeffekter
TWIK-2 tillhör en stor familj av så kallade "läckande" kaliumkanaler som hjälper till att bestämma cellers vilopotential genom att låta kaliumjoner driva över cellmembranet. Medan andra medlemmar i denna familj, som TREK- och TASK-kanaler, har studerats intensivt och kopplats till smärta och sinnestillstånd, har TWIK-2 förblivit dunkel eftersom den är svår att registrera och uttrycks dåligt i standardlaboratoriesystem. Trots det har djur- och cellstudier knutit TWIK-2 till pulmonell hypertension, akut lungskada, hörselnedsättning och aktivering av ett immunkomplex kallat NLRP3-inflammasomen, vilket driver skadlig inflammation vid sepsis och andra sjukdomar. Att förstå hur TWIK-2 fungerar är därför viktigt både för grundläggande biologi och för utformning av riktade terapier.
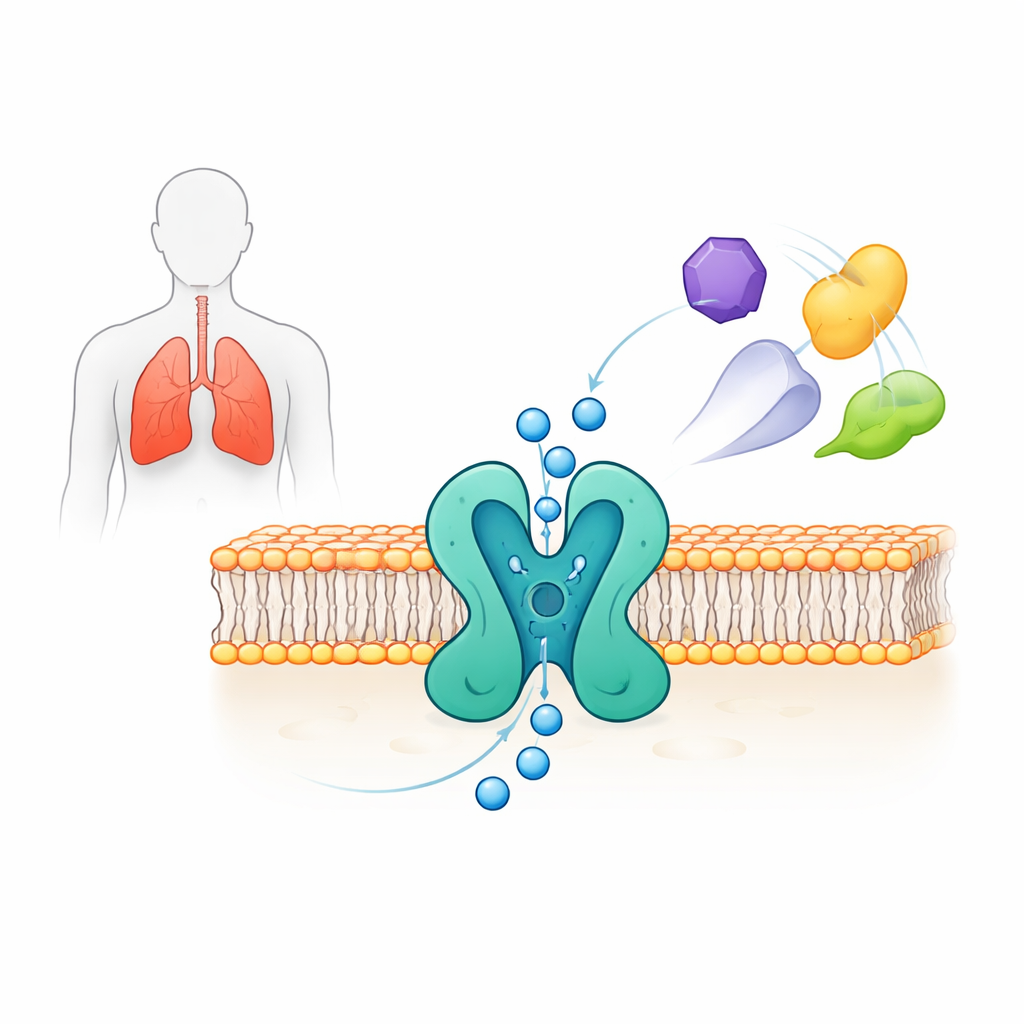
Att se porten i atomär detalj
Forskarna uttryckte fullängds mänsklig TWIK-2 i mänskliga cellinjer och använde single-particle kryoelektronmikroskopi för att bestämma dess tredimensionella struktur med en upplösning på ungefär 3,7 ångström. Kanalen bildar en tvådelad sammansättning som tillsammans skapar en central por för kaliumjoner att passera genom. Varje halva innehåller fyra membrangenomgående segment och två "porhelixar" som formar ett smalt område kallat selektivitetsfiltret, där kalium särskiljs från andra joner. Ovanför poren skapar två bågformade "lock"-strukturer två separata ingångsvägar för joner från utsidan av cellen. Strukturen avslöjar också subtila asymmetrier mellan de två sidorna av poren som ger TWIK-2 en pseudo-fyrdelad arrangemang, ett kännetecken för denna kanalfamilj.
Dolda lipider och en finjusterad jonväg
Längs jonledningsvägen kartlade teamet hur kaliumjoner rör sig från cellens inre, genom en hydrofob "manschett", upp genom selektivitetsfiltret och ut under locket. Den smalaste punkten är fortfarande tillräckligt bred för att kalium ska kunna resa i enkel fil. Även om proteinet renades utan tillsatta fettsyror visade kryo-EM-kartorna rörliknande täthet nära den nedre delen av poren och i sidofickor mellan helixar. Dessa representerar sannolikt lipider eller detergentsvansar som fastnat vid TWIK-2 under reningen, vilket antyder att naturliga membranfetter kan slå sig ner i dessa fåror och subtilt ändra formen på närliggande helixar. Sådana skiften, särskilt i en helix kallad M4 och i looparna kring selektivitetsfiltret, tros ställa in om kanalen är öppen, stängd eller någonstans däremellan.
Att pröva porten med mutationer och blockare
För att koppla struktur till funktion använde forskarna ett automatiserat patch‑clamp-system för att mäta strömmar från celler som uttryckte antingen normal TWIK-2 eller varianter med specifika aminosyror ändrade. De fann att TWIK-2 är starkt spänningsberoende men, olikt sin kusin TWIK-1, till stor del okänslig för förändringar i yttre surhetsgrad. Mutationer vid två konserverade treoniner i basen av selektivitetsfiltret gjorde att kanalen öppnade snabbare och förde mer ström, vilket tyder på att dessa platser fungerar som viktiga gångjärn som stabiliserar det stängda tillståndet. Förändringar vid ingången och utgången av poren påverkade hur snabbt kanalen slog på och av, vilket visar hur tätt kontrollerad jonvägen är. Teamet testade därefter fyra kända småmolekyler som modulerar besläktade kanaler. Två av dem, ML365 och NPBA, blockerade TWIK-2 kraftfullt, medan de andra saknade effekt. Genom att jämföra hur olika mutationer förändrade drogkänsligheten drar författarna slutsatsen att dessa föreningar sannolikt binder strax under selektivitetsfiltret och i närliggande håligheter, och att olika läkemedel använder överlappande men distinkta bindningslägen.
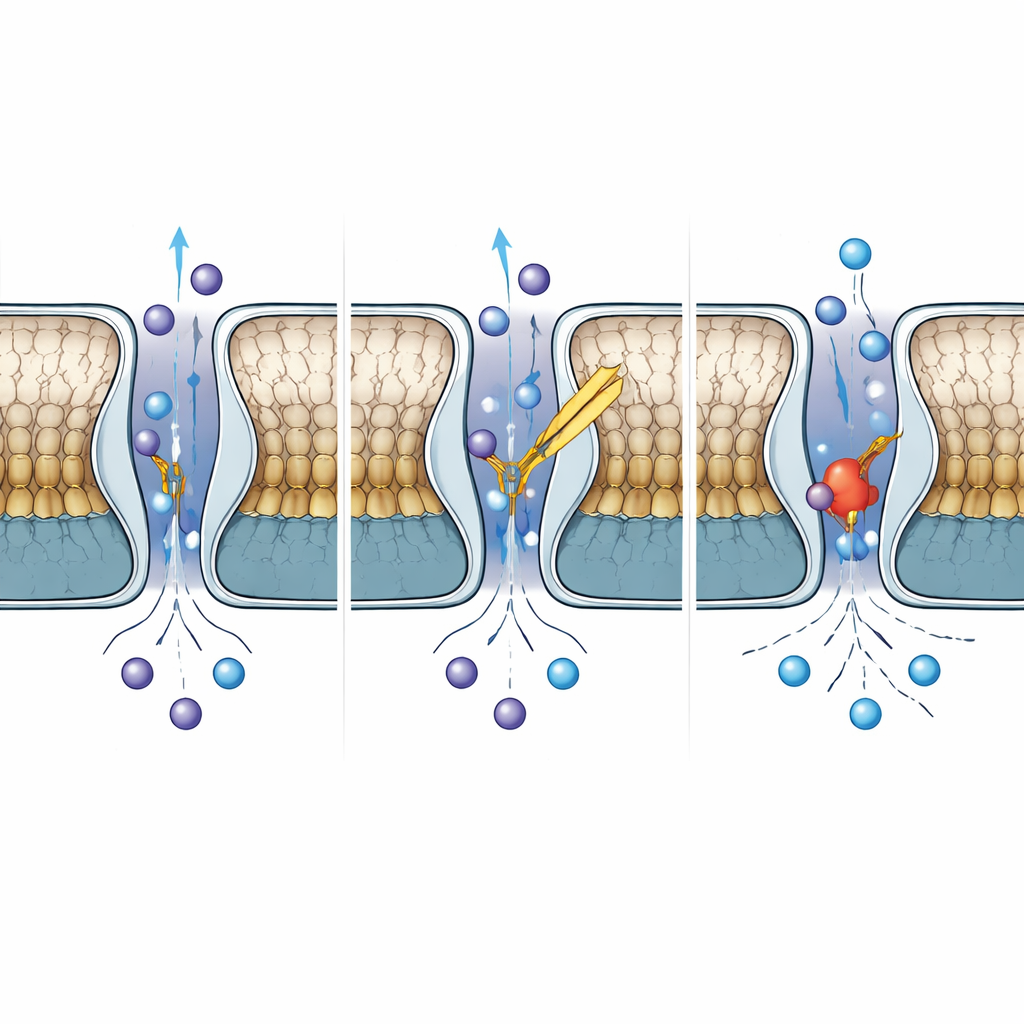
Hur TWIK-2 skiljer sig från sina närmaste släktingar
Även om TWIK-2 delar mer än hälften av sin sekvens med TWIK-1, avviker deras beteenden på viktiga sätt. När författarna jämförde TWIK-2 med publicerade TWIK-1-strukturer vid neutralt och surt pH, fann de att TWIK-2:s lockregion liknar den syra‑inhiberade formen av TWIK-1, men att dess selektivitetsfilter förblir arrangerat som den ledande, öppna formen. En enda histidin i TWIK-1, känd för att känna av protoner och svänga in i poren för att blockera jonflöde vid lågt pH, är ersatt av en tyrosin i TWIK-2. Även när teamet återinförde en histidin på denna position i TWIK-2 blev kanalen inte pH-känslig, vilket visar att pH‑kontroll i dessa kanaler bygger på ett bredare nätverk av rester och rörelser, inte bara en enda "strömbrytare"-aminosyra.
Från struktur till framtida terapier
Sammantaget ger detta arbete den första högupplösta bilden av mänskliga TWIK-2 och kartlägger hur specifika strukturella drag formar dess jonflöde, respons på spänning och känslighet för småmolekylära blockare. Upptäckten att befintliga föreningar kan selektivt hämma TWIK-2, kombinerat med en robust automatiserad screeningsplattform, öppnar dörren för storskaliga sökningar efter säkrare och mer potenta läkemedel. Eftersom TWIK-2‑aktivitet i immunceller har kopplats till okontrollerad inflammation, särskilt i lungorna, skulle sådana läkemedel kunna utgöra grunden för nya antiinflammatoriska behandlingar som verkar genom att varsamt "skruva ner" denna lilla men kraftfulla grind i cellmembranet.
Citering: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Nyckelord: TWIK-2 kaliumkanal, två-por-domän K2P-kanaler, cryo-EM jonkanalstruktur, modulatorer av kaliumkanaler, pulmonal inflammation