Clear Sky Science · sv
Kolonial rumslig enkelcellsproteomik och musmodeller kopplar mitokondriell dysfunktion till brist på dimeriskt IgA‑utsöndrande plasmaceller vid Crohns sjukdom
Varför tarmantikroppar är viktiga vid Crohns sjukdom
Crohns sjukdom är mest känd för smärtsamma skov av tarminflammation, men långt innan symtomen ökar kan subtila förändringar ske i hur immunsystemet skyddar tarmen. Denna studie ställer en enkel men viktig fråga: producerar personer med Crohns sjukdom i remission fortfarande rätt typ av antikroppar för att hålla tarmens mikrober i schack? Genom att kombinera patientprover, högupplöst vävnadsprofilering, metabola analyser och musmodeller upptäcker författarna en dold svaghet i tarmens antikroppsskydd som är kopplad till cellernas energiproduktion.
En skyddande beläggning som inte räcker till
Våra tarmar är beroende av en speciell antikropp kallad sekretoriskt IgA som utsöndras i slemhinnan. IgA, särskilt i dess ”dubbel” form kallad dimeriskt IgA, täcker bakterier och andra mikrober och hjälper till att hålla dem vid ytan snarare än djupt inne i vävnaden. I detta arbete undersökte forskarna kolonbiopsier, blod och avföring från personer med Crohns sjukdom i remission och från icke‑inflammerade kontroller. I kolonvävnaden hade Crohns‑patienter faktiskt fler B‑celler och antikroppsproducerande celler samt högre nivåer av IgA‑relaterade gener och proteiner. När teamet mätte IgA i avföring fann de ändå motsatsen till vad man kan vänta sig: sekretoriskt IgA i tarmlumen var signifikant minskat. 
Fast halvvägs: antikroppsproducerande celler som inte mognar helt
Cellerna som utsöndrar IgA—plasmaceller—mognar normalt genom definierade steg från aktiva, kortlivade föregångare till långtlevande specialister som producerar stora mängder dimeriskt IgA. Med rumslig enkelcellsproteomik, som kartlägger många proteiner på individuella celler i intakt vävnad, kunde författarna skilja omogna och fullt mogna plasmacellsundergrupper i kolon. Hos Crohns‑patienterna var tidiga plasmablasts och omogna plasmaceller utökade, medan de mest mogna plasmacellerna var reducerade. Biokemiska analyser bekräftade att kvoten dimeriskt mot monomert IgA var lägre i Crohns‑kolon, och varje antikroppsproducerande cell utsöndrade i genomsnitt mindre dimeriskt IgA. När teamet isolerade klassväxlade minnes‑B‑celler från kolon och drev dem att bli plasmaceller i kultur, kunde celler från Crohns‑patienter inte uppreglera viktiga mognadsmarkörer och producerade mindre total och dimerisk IgA, även om IgG‑produktionen i stort var normal. Detta tyder på ett inneboende block i mognadsprogrammet specifikt för IgA‑utsöndrande plasmaceller.
Energifabriker under belastning
För att förstå vad som driver detta block vände forskarna sig till cellmetabolism. De fann att plasmaceller i Crohns‑vävnad uttryckte högre nivåer av CD38, ett enzym på cellytan som förbrukar NAD+, ett centralt bränsle för mitokondriell energiproduktion. Gener som är involverade i mitokondriell oxidativ fosforylering—huvudvägen för cellernas ATP‑produktion från näringsämnen—var generellt nedreglerade i kolonvävnad från Crohns‑patienter, och plasmametabolitmönster var förenliga med ett skifte bort från effektiv mitokondrieandning. I ex vivo‑experiment konsumerade Crohns‑härledda plasmaceller lite glukos, frisatte mindre laktat och visade reducerat uttryck av mitokondriella energigen, vilket indikerar ett metaboliskt ”kvarvarande” eller försvagat tillstånd. 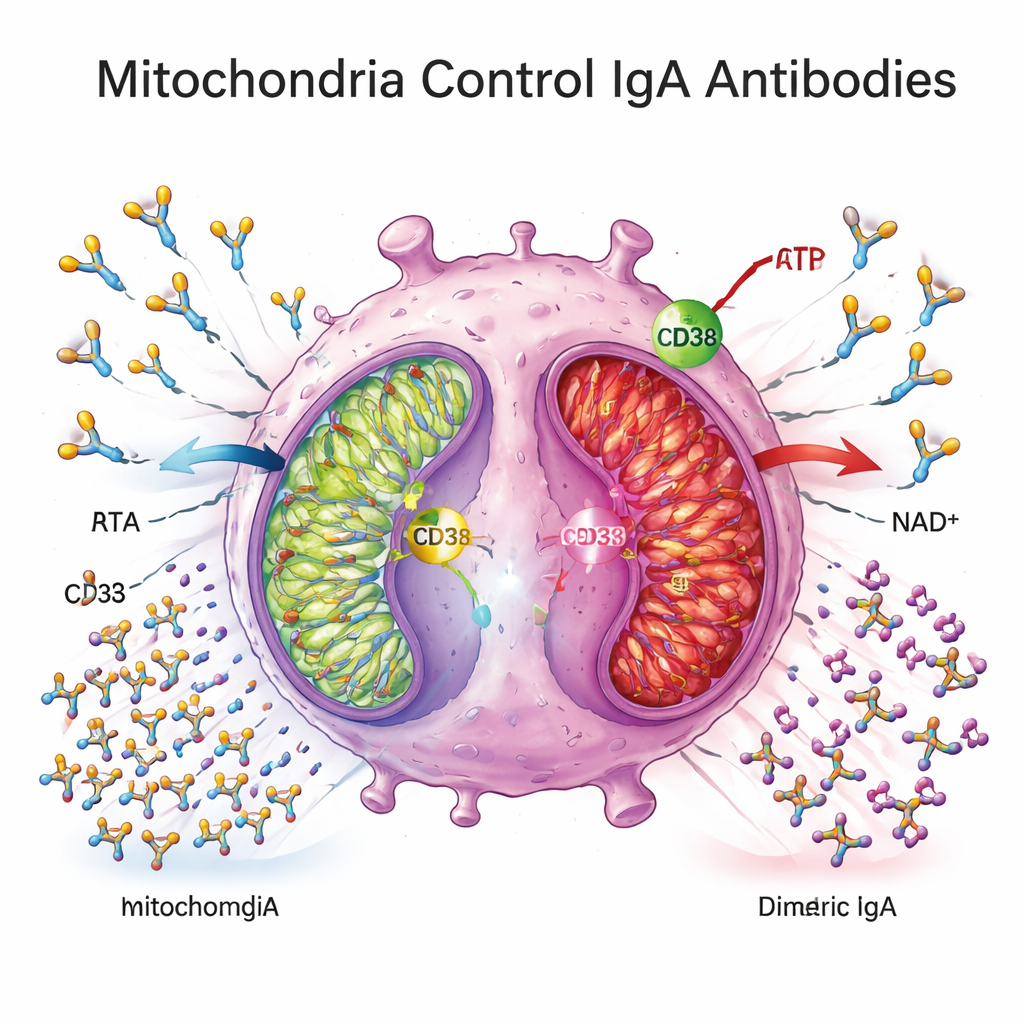
Ledtrådar från musmodeller och kost
Musmodeller gav ytterligare stöd. Möss som bar en definierad mitokondriell mutation som försämrar ATP‑producerande enzymkomplex V hade färre mogna plasmaceller i tarmassocierade lymfoida vävnader, reducerat uttryck av plasmacellsmarkörer i kolon och lägre nivåer av både monomert och dimeriskt IgA i kolonvävnad. Omvänt utvecklade friska möss som föddes på en glukosfri, proteinrik diet som förbättrar mitokondrieaktiviteten i kolon fler IgA‑producerande celler och högre fecalt IgA. Dessa kompletterande experiment knyter mitokondriell funktion direkt till plasmacellernas förmåga att mogna och upprätthålla en robust IgA‑barriär i tarmen.
Vad detta betyder för personer med Crohns sjukdom
Sammantaget målar studien upp en bild där Crohns sjukdom, även under klinisk remission, är förknippad med ett överflöd av omogna B‑linje‑celler i kolon och en brist på fullt mogna, energikrävande plasmaceller som utsöndrar dimeriskt IgA i slemmet. Tarmen kan se lugn ut, men dess antikroppsskydd är tunnare och mindre effektivt. Genom att koppla denna defekt till mitokondriell dysfunktion—möjligen delvis driven av ökad CD38‑aktivitet—tyder arbetet på att terapier inriktade på att återställa cellulär energimetabolism eller finjustera CD38‑signalering kan hjälpa till att bygga upp det mukosala IgA‑skyddet. För patienter väcker detta utsikten att framtida behandlingar inte bara kan dämpa inflammation när den uppstår, utan också stärka tarmens första försvarslinje av antikroppar för att förhindra att skov uppstår från början.
Citering: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Nyckelord: Crohns sjukdom, tarmantikroppar, IgA, mitokondrier, intestinalt immunförsvar