Clear Sky Science · sv
FidlTrack: högupplöst strukturmedveten single particle tracking löser intracellulär molekylär rörelse i organeller som känner av APP‑bearbetning
Att observera enskilda molekyler inne i levande celler
Inuti varje cell rör sig otaliga molekyler ständigt—de stöter ihop, binder och faller isär. Moderna mikroskop kan följa enskilda molekyler en i taget och lovar en detaljerad bild av hur livet fungerar på de minsta skalen. Men när många molekyler rör sig snabbt i trånga, slingrande utrymmen, till exempel i det endoplasmatiska nätverket eller mitokondrierna, blir deras banor intrasslade och lätta att misstolka. Denna artikel presenterar FidlTrack, ett nytt sätt att reda ut den trassligheten så att forskare kan lita på vad de ser när de spårar enskilda molekyler i realtid.
Varför det är så svårt att följa små rörelser
Single particle tracking fungerar genom att följa samma ljusa punkt över många bildrutor. På en relativt plan yta där molekyler rör sig långsamt och är åtskilda är detta hanterbart. Djupt inne i cellen diffunderar molekyler däremot mycket snabbare och trängs ihop i smala, slingrande rör och skivor. Mellan bildrutor kan samma punkt ha rört sig långt, och flera identiska punkter kan ligga inom räckhåll. Traditionell mjukvara måste ”gissa” vilken punkt i nästa ruta som är samma molekyl, och de gissningarna kan lätt bli fel. Värre är att korrekta och felaktiga banor kan likna varandra starkt, så det är svårt att veta vilka delar av datan som går att lita på.
Att utforma experiment för ärliga data
Forskarna byggde först en realistisk simulator som genererar "ground truth"-filmer av diffunderande molekyler, där de verkliga banorna är kända. De använde dessa syntetiska datamängder för att systematiskt testa hur nyckelfaktorer påverkar spårningspålitligheten: hur snabbt molekyler rör sig, hur många som syns i varje bild, hur ofta bilder tas och hur långt en molekyl tillåts hoppa mellan rutor. Utifrån detta skapade de kartor som visar vilka inställningar som maximerar andelen korrekt rekonstruerade rörelser i olika situationer. Kartorna visar att för långsamt rörliga molekyler vid måttliga densiteter kan spårning vara mycket tillförlitlig, men för snabbrörliga molekyler vid hög densitet ökar felen snabbt och att lägga till fler molekyler förbättrar inte längre den användbara informationen.
Upptäcka och ta bort tveksamma steg
Nästa steg tog teamet itu med en subtil men kraftfull idé: tvetydighet. En rörelse kallas tvetydig när mer än en möjlig nästa punkt ligger inom räckhåll, vilket tvingar algoritmen att välja mellan flera rimliga länkar. Med hjälp av sina simuleringar visade författarna att en stor andel av spårningsfelen uppstår från dessa tvetydiga steg. De definierade en Ambiguity Score som räknar hur ofta sådana situationer uppstår, och undersökte vad som händer om alla tvetydiga steg tas bort efter spårningen. Denna beskärning offrar en del data och förkortar banor, men höjer skarpt den övergripande tillförlitligheten i det som återstår och förbättrar uppskattningar av hur snabbt molekyler rör sig. När metoden tillämpades på verkliga filmer av en markör i det endoplasmatiska nätverket var tvetydigheten högre i trängda områden nära cellkärnan, och borttagning av tvetydiga länkar renade upp dessa områden utan att skada enklare regioner.
Låta cellens arkitektur styra spårningen
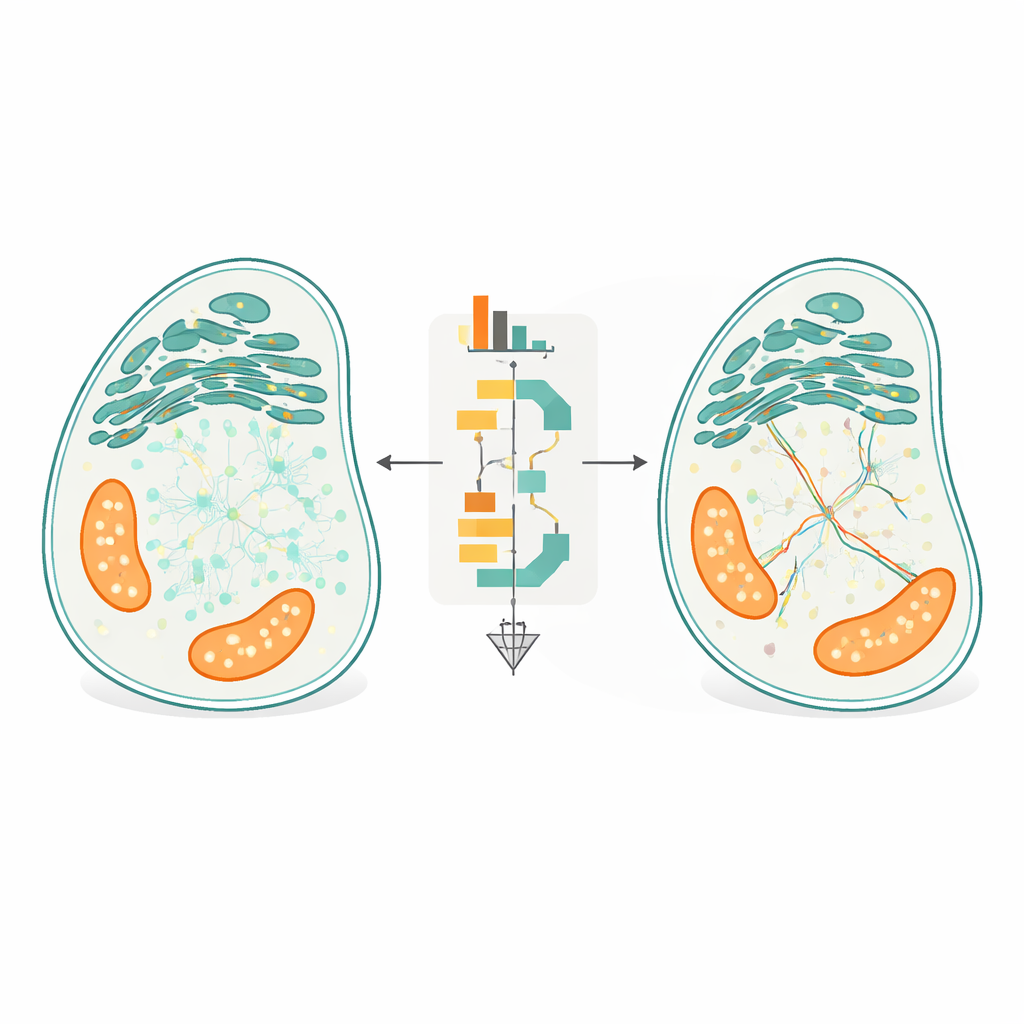
Den centrala nyheten i FidlTrack är "strukturmedveten" spårning. Istället för att behandla varje punkt som om den rörde sig i tomt rum använder metoden bilder av cellens interna arkitektur—som konturerna av endoplasmatiskt nätverk, mitokondrier eller smala neuronala utskott—för att begränsa var molekyler realistiskt kan förflytta sig. Organellbilden omvandlas till en graf av sammanhängande pixlar, och avstånd mäts längs denna graf snarare än i raka linjer genom rummet. Länkar som skulle kräva att en molekyl hoppar över ett gap mellan två separata tubuli kan därmed flaggas som omöjliga och avvisas. I simuleringar av tätt packade rör och i verkliga filmer av neuronala processer och organeller minskade denna strukturella medvetenhet tvetydiga kopplingar med upp till hälften och ökade mängden pålitlig, icke-tvetydig rörelsedata flera gånger om.
Avslöja dolda cellbeteenden och sjukdomsrelevanta händelser
Utrustade med dessa verktyg—optimerade inställningar, filtrering av tvetydighet och strukturmedvetenhet—återbesökte författarna flera biologiska frågeställningar som tidigare legat strax utanför räckhåll. I det endoplasmatiska nätverket kunde de tydligt följa hur proteiner rör sig när de engagerar sig med exit‑platser som kanaliserar gods mot Golgiapparaten, och skilja korta "fly-bys" från längre uppehåll. De fångade sällsynta ögonblick när det Alzheimer‑relaterade proteinet APP klyvs av enzymet BACE1, synligt som en plötslig övergång från långsam, membran‑bunden rörelse till snabbare fri diffusion. De följde också konstruerade antikroppsliknande molekyler i ER och drog slutsatser om när de bundit sitt mål respektive drivit fritt, utifrån förändringar i deras rörelse. I dessa olika fall återvann FidlTrack mer tillförlitliga banor och skärpte skillnader som standardspårning antingen suddade ut eller underskattade.
Vad detta betyder för framtidens cellbiologi
För icke‑specialister är huvudbudskapet att inte alla enskilda molekylspår är likvärdiga: vissa är tillförlitliga, andra missvisande, och hittills har det varit svårt att skilja dem åt. FidlTrack erbjuder ett praktiskt, öppen källkodssätt för att både mäta hur tillförlitlig en given datamängd är och förbättra den genom att finjustera experimentinställningar, ta bort tvetydiga steg och använda cellens egen geometri som vägledning. Detta gör det möjligt att med större säkerhet se hur molekyler navigerar cellens intrikata inre och att upptäcka sällsynta eller subtila händelser—från proteinsortering till sjukdomsrelevant bearbetning—that tidigare begravts i brus.
Citering: Parutto, P., Yuan, Y., Davì, V. et al. FidlTrack: high-fidelity structure-aware single particle tracking resolves intracellular molecular motion in organelles sensing APP processing. Nat Commun 17, 2639 (2026). https://doi.org/10.1038/s41467-026-69067-y
Nyckelord: single particle tracking, intracellulär dynamik, organelstruktur, proteinrörelse, Alzheimers sjukdom