Clear Sky Science · sv
FLASH-MM: snabb och skalbar differentieringsanalys på enkelcellsnivå med linjära mixade effekter-modeller
Varför små celler behöver stor datorhjälp
Modern biologi kan numera avläsa aktiviteten hos tusentals gener i hundratusentals enskilda celler samtidigt. Denna enkelcellsvy lovar skarpare insikter i hur våra kroppar bekämpar infektioner, skiljer sig mellan könen eller utvecklar sjukdom. Men att omvandla dessa enorma, röriga datamängder till pålitliga upptäckter går långsamt och kan, om det görs naivt, vilseleda. Denna artikel presenterar FLASH-MM, ett nytt sätt att bearbeta enkelcellsdata som håller statistiken korrekt samtidigt som beräkningarna blir tillräckligt snabba för dagens största studier.
Utmaningen med bullrig, trängd celldata
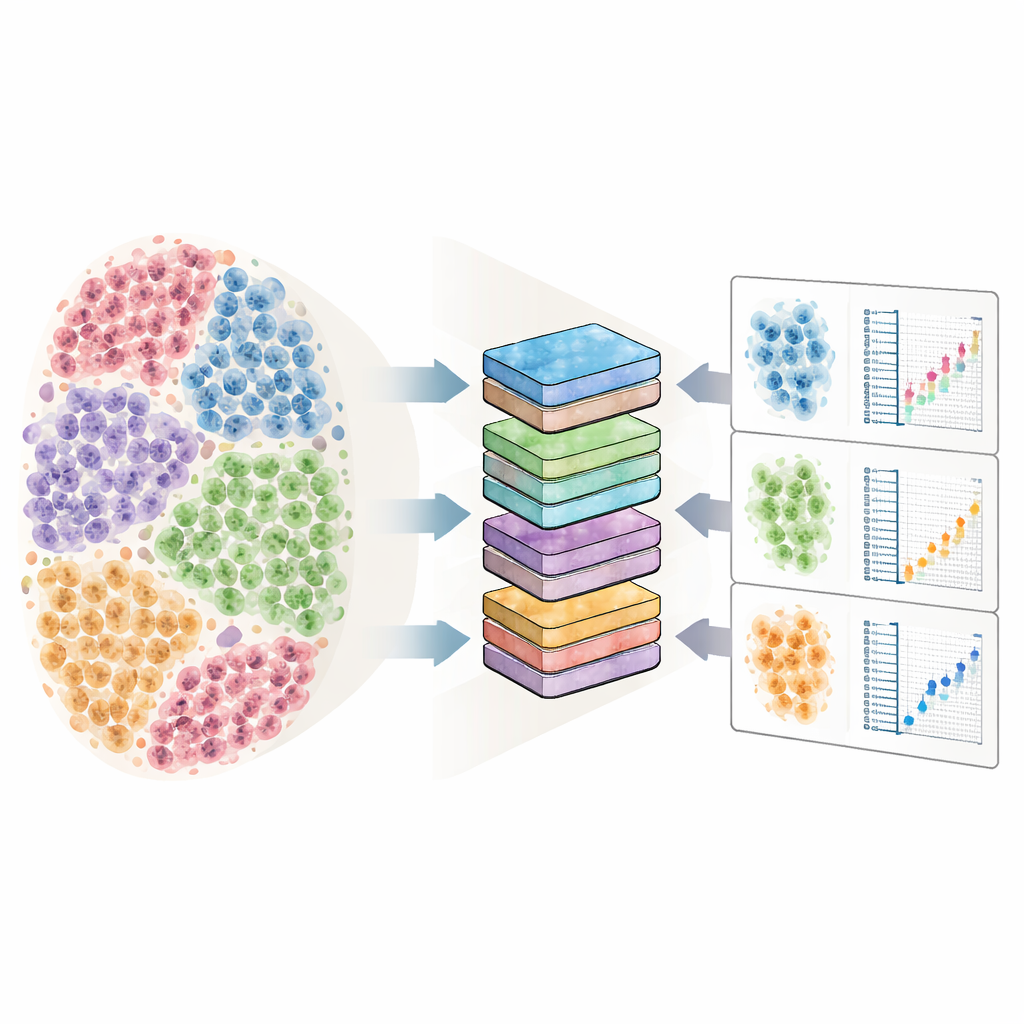
Single-cell RNA-sekvensering mäter vilka gener som är ”på” eller ”av” i varje cell, över många personer och tillstånd. Celler från samma person tenderar att likna varandra eftersom de delar gener och livshistoria, medan personer skiljer sig mycket åt sinsemellan. Det skapar en flerskiktsstruktur i datan: många celler inom varje person och många personer inom varje tillstånd, till exempel sjuk kontra frisk. Om dessa relationer ignoreras kan standardmetoder felaktigt märka tusentals gener som förändrade när de inte är det, helt enkelt för att de behandlar varje cell som en oberoende datapunkt. Samtidigt har enkelcellsdataset vuxit explosionsartat och inkluderar nu hundratals försökspersoner och upp till miljontals celler, vilket spänner konventionella statistiska verktyg bortom deras gränser både vad gäller tid och minne.
En smartare modellering av personer och celler
För att hantera dessa komplexiteter vänder sig statistiker ofta till linjära mixade effekter-modeller, som uttryckligen separerar konsekventa skillnader mellan tillstånd (till exempel tuberkulosstatus eller kön) från slumpmässiga skillnader mellan individer. I princip är dessa modeller idealiska för enkelcellsstudier eftersom de kan beakta både likheter bland celler från samma person och variation mellan personer. I praktiken saktar dock vida använda programvaror för dessa modeller ner eller går tomma på minne vid stora enkelcellsexperiment. Forskarna faller därför ofta tillbaka på genvägar, såsom att medelvärdesbilda räkningar över alla celler av samma typ inom varje person, vilket slänger bort mycket av den finfördelade cell-till-cell-information som gör enkelcellsdata så värdefulla.
Hur FLASH-MM snabbar upp tungt arbete
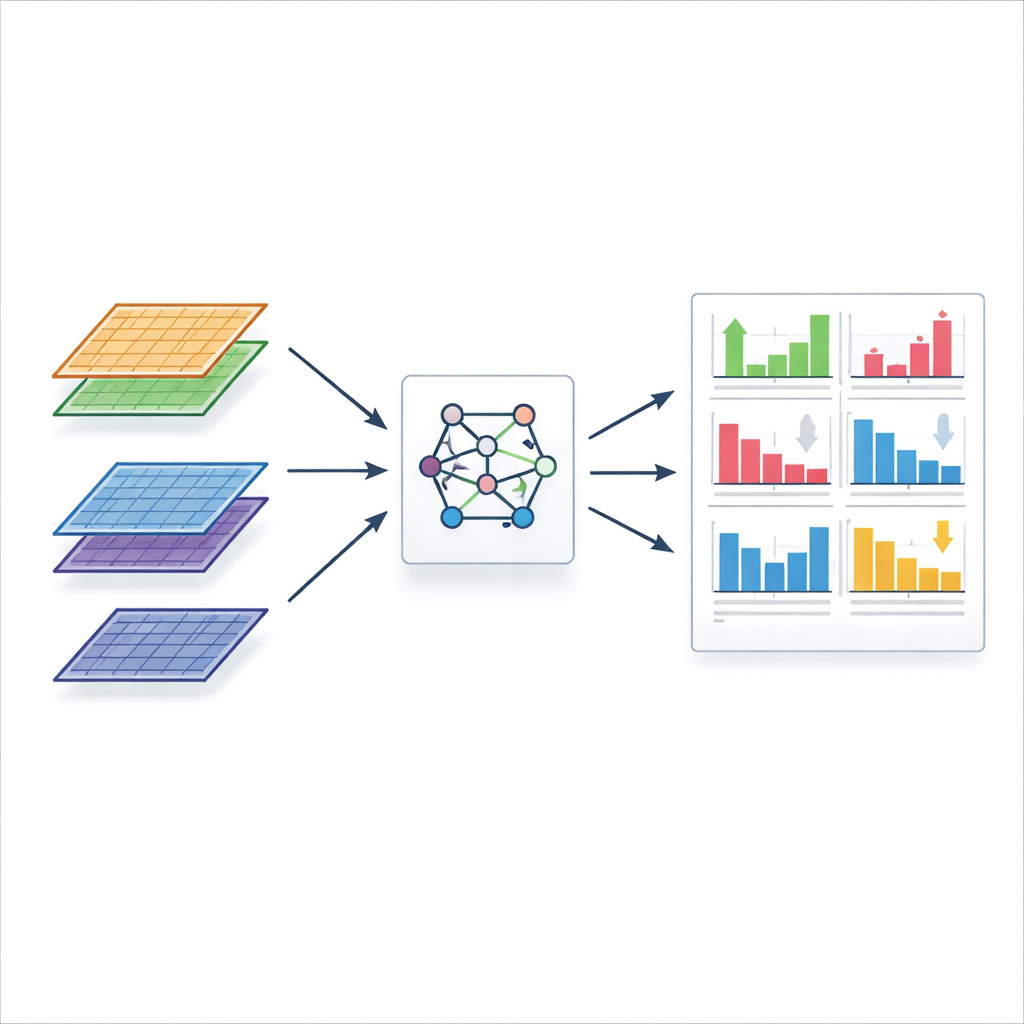
FLASH-MM behåller styrkorna hos mixade effekter-modeller samtidigt som det omkonstruerar hur beräkningarna utförs. Istället för att upprepade gånger gå igenom jättelika tabeller med cell-vid-gen-mätningar destillerar FLASH-MM först varje dataset till ett kompakt set summeringsvärden som fångar hur celler relaterar till kända egenskaper som bibliotekstorlek, celltyp, behandling eller donator. Kärnalgoritmen arbetar sedan endast med dessa mindre matriser, vilket krymper den beräkningsmässiga bördan från att skala med varje cell till att skala med det betydligt mindre antalet modellelement. Författarna finjusterar även hur modellens variabilitet representeras så att standardstatistiska test förblir giltiga, vilket möjliggör enkla t- och z-statistik för att bedöma både huvudeffekterna av intresse och det mervärde som kommer av att inkludera person-till-person-variation. Simuleringsstudier med realistiska artificiella data visar att FLASH-MM:s resultat överensstämmer med guldkornsprogramvara ner till flera decimaler, samtidigt som det körs ungefär 50 till 140 gånger snabbare och använder avsevärt mindre minne.
Att använda metoden i verklig vävnad
För att visa verklig nytta tillämpade teamet FLASH-MM på två krävande enkelcellsdataset. I en karta över mer än 27 000 friska mänskliga njurceller från 19 donatorer sökte FLASH-MM efter genaktivitetskillnader mellan manliga och kvinnliga donatorer inom varje celltyp, samtidigt som varje person behandlades som en slumpfaktor för att undvika överdrivet säkra resultat. Den starkaste könsrelaterade mönstret hittades i en specifik njurtubulcellstyp, där manliga celler gynnade signalvägar kopplade till syrahantering och blodtryck, medan kvinnliga celler visade berikning för signalering och receptoråtervinning. FLASH-MM slutförde denna analys på ungefär en minut, jämfört med nästan två timmar för ett standardverktyg. Metoden analyserade också ungefär en halv miljon minnes-T-celler från 259 personer i en tuberkuloskohort och identifierade gen- och vägsets kopplade till sjukdomsstatus i olika aktiverade T-cellstillstånd. Här blev FLASH-MM klar på under en och en halv timme, jämfört med mer än två dagar för den konventionella metoden.
Vad detta betyder för framtida cell-för-cell-studier
Ur ett populärvetenskapligt perspektiv är budskapet att vi nu kan utnyttja floden av enkelcellsdata bättre utan att ta genvägar. FLASH-MM håller reda på vilka celler som kom från vilken person och vilket tillstånd, så att upptäckta genförändringar sannolikt bättre speglar verklig biologi snarare än sampling- eller batch-effekter. Samtidigt gör dess slimmade beräkningar det möjligt att analysera hundratusentals celler på vanliga datorer, vilket öppnar för mer ambitiösa studier av subtila sjukdomssignaler, könsskillnader och sällsynta celltillstånd. Eftersom tillvägagångssättet är generellt och finns tillgängligt både i R och Python kan det utvidgas till nyare teknologier som spatial genkartering och multilager-molekylära mätningar, och hjälpa forskare att omvandla stora cellnivå-dataset till robusta, kliniskt relevanta insikter.
Citering: Xu, C., Pouyabahar, D., Voisin, V. et al. FLASH-MM: fast and scalable single-cell differential expression analysis using linear mixed-effects models. Nat Commun 17, 2384 (2026). https://doi.org/10.1038/s41467-026-69063-2
Nyckelord: single-cell RNA sequencing, differentiell uttrycksanalys, linjära mixade effekter-modeller, statistisk genomik, beräkningsbiologi