Clear Sky Science · sv
Tenascin C+ myofibroblaster förvärrar vaskulär neointimal hyperplasi genom spridning av nerv-makrofaginteraktioner hos möss
När blodkärl läker på fel sätt
Åtgärder som öppnar upp tilltäppta artärer, såsom ballongvidgning (angioplasti) och bypass-operation, räddar otaliga liv. De lämnar dock ofta ett dolt problem efter sig: med tiden kan det behandlade kärlet ärrväxa inåt, smalna av igen och utsätta patienten för risk. Denna studie i möss avslöjar en oväntad trevägskommunikation mellan stödjeceller, nerver och immunceller i kärlväggen som driver denna skadliga överläkning, och lyfter fram ett protein kallat tenascin C som ett lovande mål för att bryta cykeln.
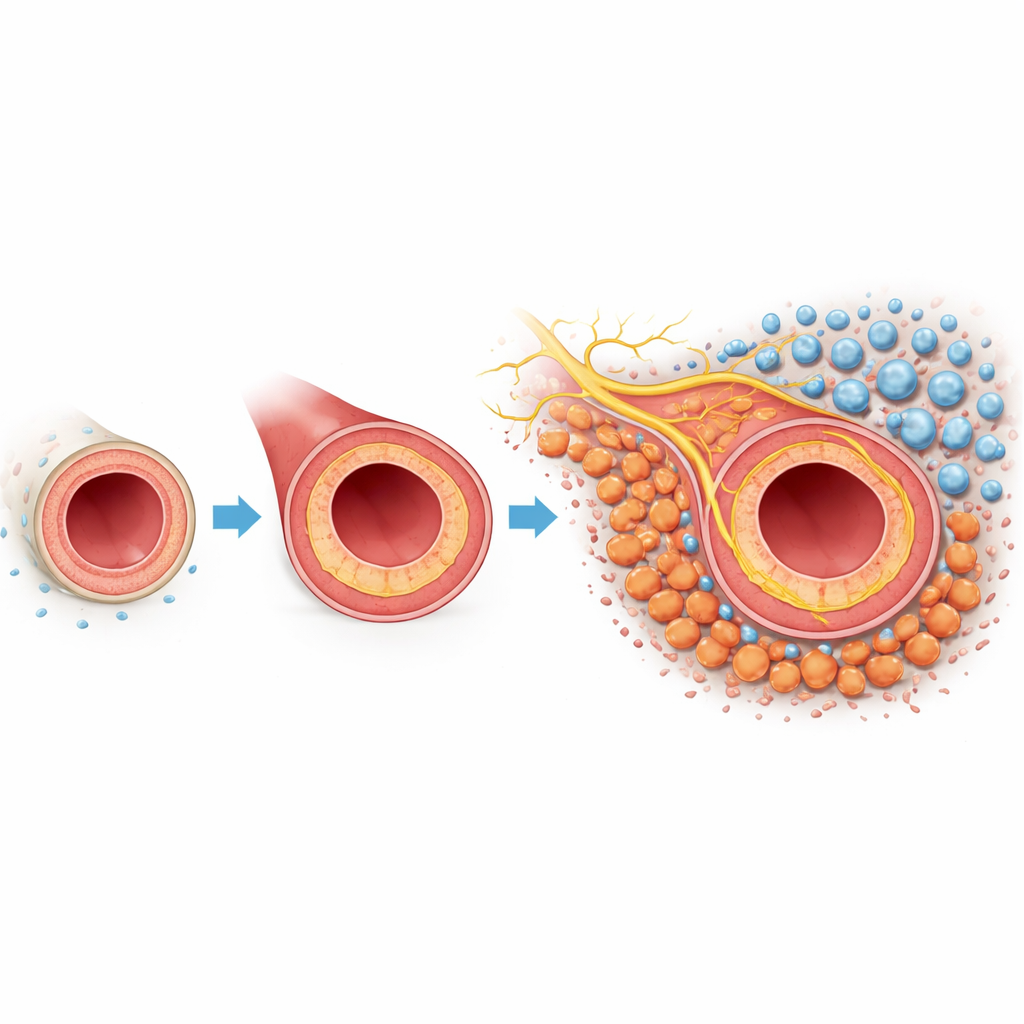
Närmare titt på problematisk ärrbildning i artärer
När en artär skadas eller manipuleras under operation kan det inre skiktet växa tillbaka för aggressivt. Denna inåtvända tillväxt, kallad neointimal hyperplasi, förtjockar kärlväggen och minskar kanalen där blodet flyter. Det yttersta lagret av kärlet, adventitian, innehåller fibroblaster—stödjeceller som normalt upprätthåller kärlets struktur. I denna musemodell, där karotisartären delvis bands för att efterlikna skada, använde forskarna enkelcellsgenetisk profilering och spatial kartläggning för att katalogisera varje huvudcellstyp som är involverad. De fann att fibroblaster var särskilt talrika och ändrade sitt beteende dramatiskt efter skada, vilket tyder på att dessa celler kan vara centrala aktörer i ärrsvaret.
Framväxten av ärrbildande tenascin C-celler
Genom att granska fibroblastpopulationen närmare upptäckte teamet en distinkt undergrupp som bara framträdde efter skada. Dessa celler bar kännetecken för myofibroblaster—höga nivåer av kontraktilt protein α-smooth muscle actin och en annan markör kallad periostin—vilket signalerar att de växlat till ett ärrbildande läge. Avgörande nog producerade denna undergrupp också stora mängder tenascin C, ett matrixprotein som normalt är sällsynt i friska vuxna vävnader men rikligt förekommer vid sjukdom och vävnadsreparation. Laboratorieexperiment visade att exponering av normala adventitiala fibroblaster för transformeringstillväxtfaktor beta eller extra tenascin C drev dem att bli dessa tenascin C–positiva myofibroblaster. Cellerna utsöndrade sedan ännu mer tenascin C och skapade en självförstärkande loop via ett specifikt ytreceptorpar, integrin αvβ1, som stadigt utvidgade den ärrbildande populationen.
Nerver och immunceller flyttar in i grannskapet
Berättelsen slutade inte med ärrbildningen. Med hjälp av 3D-bildtagning av hela preparat och spatial transkriptomik observerade forskarna att de tenascin C–rika myofibroblasterna klustrade sig nära utvuxande nervfibrer och immunceller kallade makrofager i det yttre kärllagret. Skadade artärer visade täta, trassliga sensoriska nerver och fler synapsliknande strukturer än normalt, både i möss och i humana artärprover med neointimal hyperplasi. Makrofager i dessa områden uppvisade en inflammatorisk signatur och producerade molekyler såsom IL-1β och TGF-β1 som ytterligare kan driva ärrbildning. Tillsammans målade data upp en bild av en omorganiserad mikro-miljö där ärrbildande celler, nerver och makrofager fysiskt blandas och påverkar varandra.
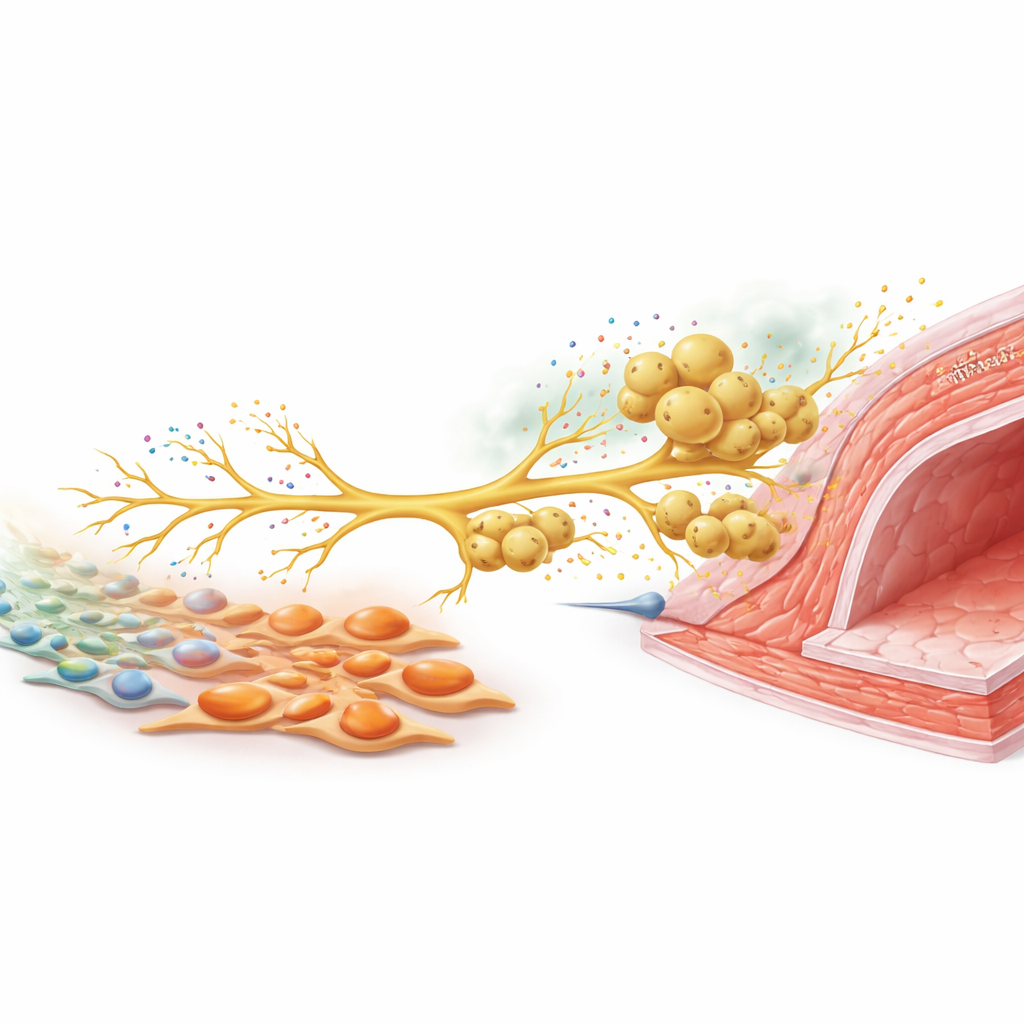
En nervsignal som kallar in fler försvarare
För att förstå hur dessa celltyper kommunicerar fokuserade teamet på sensoriska nerver som känner av skadliga stimuli. I cellkultur ökade tenascin C–rika myofibroblaster utväxten av nervfibrer från dorsalrotsganglie-neuroner. Hos skadade möss ökade dessa sensoriska neuroner produktionen av CCL2, en kemisk signal välkänd för att locka makrofager. När neuroner och makrofager odlades tillsammans migrerade makrofager längs växande nervefibrer, ungefär som de gjorde runt artärer in vivo. Tystnad av CCL2 i neuroner minskade kraftigt makrofagrekryteringen. I djur minskade både nedskärning av sensorisk nervaktivitet med ett toxin och selektiv deletion av tenascin C endast i fibroblaster nervdensiteten, CCL2-nivåerna, makrofagansamlingen och i slutändan förtjockningen av kärlväggen. Kombinationen av båda interventionerna gav ingen ytterligare nytta, vilket tyder på att de verkar längs samma signalväg.
Varför denna nya väg är betydelsefull
Tillsammans avslöjar fynden en ond cirkel: skada får fibroblaster att bli tenascin C–producerande myofibroblaster; dessa celler omformar matrixen och stimulerar sensoriska nerver; aktiverade nerver frigör CCL2, vilket lockar makrofager; och makrofager utsöndrar inflammatoriska och fibrotiska faktorer som förvärrar ärrbildningen och förtränger artären. Genom att identifiera tenascin C och dess efterföljande nerv–makrofag-axel som centrala drivkrafter i denna loop föreslår arbetet att behandlingar som riktar sig mot detta protein eller dess signalpartners kan hjälpa till att hålla reparerade artärer öppna längre, och därigenom ge patienter mer bestående skydd efter kardiovaskulära ingrepp.
Citering: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Nyckelord: neointimal hyperplasi, tenascin C, vaskulär ombyggnad, sensoriska nerver, makrofaginflammation