Clear Sky Science · sv
Paclitaxel driver expansion av TREM2+ makrofager som förklarar dess sämre terapeutiska effekt jämfört med Nab-paclitaxel
Varför denna studie är viktig
Många kvinnor med bröstcancer får cellgifter som tillhör taxanklassen, oftast paclitaxel eller en nyare variant bunden till små albuminpartiklar, kallad nab‑paclitaxel. Läkare har länge misstänkt att den nyare läkemedelsformen ofta fungerar bättre, men orsakerna var oklara. Den här studien granskar både patientdata och djurförsök och visar att standardpaclitaxel oavsiktligt kan hjälpa cancer att sprida sig till lungorna genom att omforma kroppens immunceller, och pekar ut ett sätt att blockera denna skadliga bieffekt.
Två snarlika läkemedel, två olika utfall
Forskarna jämförde först den verkliga effekten av paclitaxel och nab‑paclitaxel i tusentals kvinnor med bröstcancer. Genom att slå samman resultat från 17 kliniska studier med totalt 6 486 patienter fann de att nab‑paclitaxel gav högre tumörkrympningsfrekvenser och fler fullständiga försvinnanden av cancer i bröstet och närliggande lymfkörtlar före operation. Denna fördel var särskilt uttalad hos patienter som behandlats efter att tidigare terapier misslyckats. Ändå gavs båda läkemedlen i liknande doser och är designade för att angripa delande cancerceller på liknande sätt, vilket antyder att något utöver direkt tumördödande skiljer dem åt.
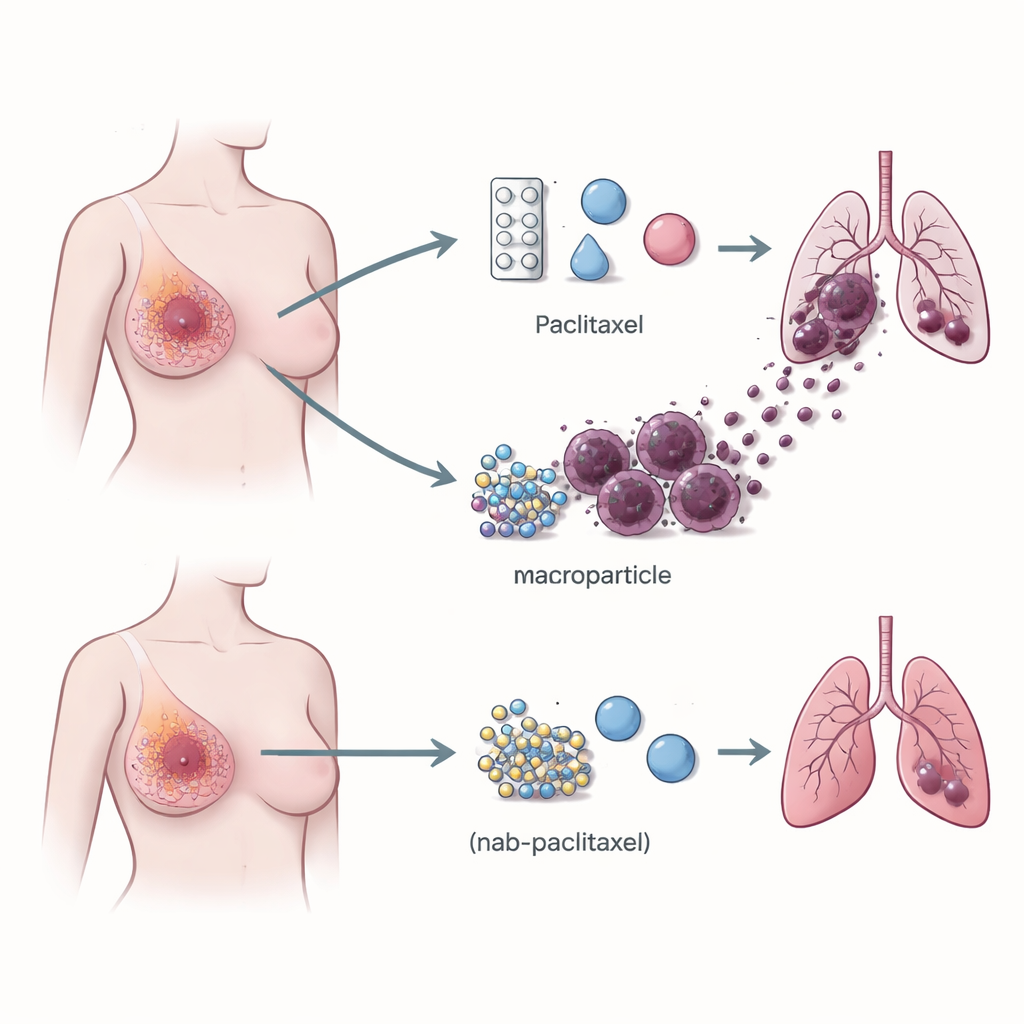
Immunceller som hjälper cancer att resa
Uppmärksamheten vändes mot tumörens immiljö — blandningen av vita blodkroppar som antingen kan bekämpa cancer eller, förvånansvärt ofta, hjälpa den att växa. Med hjälp av enkelcells‑RNA‑sekvensering, som läser genaktiviteten i tusentals enskilda celler, jämförde teamet tumörer från patienter behandlade med paclitaxel respektive nab‑paclitaxel. De fann att paclitaxelbehandlade tumörer innehöll betydligt fler makrofager som bär en receptor kallad TREM2 på ytan. Dessa TREM2‑positiva makrofager var rikliga vid tumörernas kanter och var mycket vanligare hos patienter som senare utvecklade lungmetastaser än hos dem vars cancer stannade kvar lokalt. Mönstret bekräftades i större patientgrupper och i musmodeller, vilket etablerar en stark koppling mellan denna makrofagtyp och risken för spridning.
När behandling krymper tumörer men gynnar spridning
I möss med brösttumörer gjorde paclitaxel vad det ska: det bromsade eller krympte primärtumörerna. Samtidigt ökade det antalet cancerfoci i lungorna och ökade förekomsten av TREM2‑positiva makrofager i tumörer och i blodomloppet. Nab‑paclitaxel, däremot, minskade tumörstorleken utan att driva på lungmetastasering eller expansion av dessa makrofager, trots att det var lika effektivt för att krympa huvudtumören. När genen för TREM2 togs bort i möss, eller när TREM2 minskades med antisens‑oligonukleotider (korta DNA‑bitar som tystar specifika gener), krympte paclitaxel fortfarande primärtumörerna men förlorade till stor del sin förmåga att främja lung‑spridning. Detta visar att TREM2‑bärande makrofager inte bara är förbipasserande; de är nödvändiga medverkande i paclitaxel‑driven metastasering.
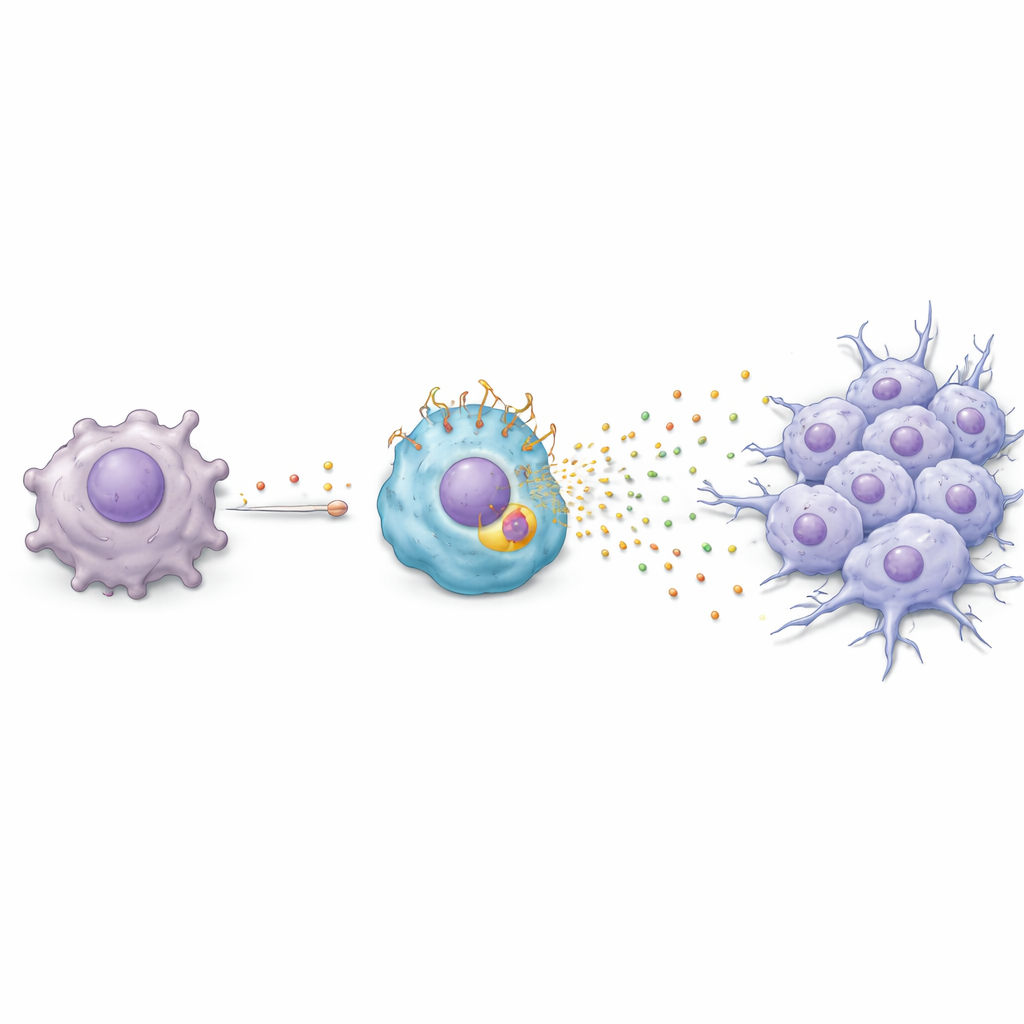
En kemisk kedjereaktion från tumör till immuncell
Teamet undersökte sedan hur paclitaxel orsakar att makrofager antar detta skadliga, TREM2‑rika tillstånd. De upptäckte en kedjereaktion: paclitaxel får cancerceller att slå på en stressresponsgen kallad ATF3, vilket i sin tur ökar produktionen av en tillväxtfaktor kallad FGF2. Cancercellerna frisätter därefter FGF2 i sin omgivning där den påverkar närliggande makrofager. I dessa makrofager aktiverar FGF2 en annan regulator, EGR1, som höjer TREM2‑nivåerna. När TREM2 är högt börjar makrofagerna utsöndra en blandning av proteiner — inklusive Serpin E1, HGF, CCL3 och CXCL2 — som driver cancerceller att anta en mer rörlig, invasiv form känd som epitelial‑mesenkymal transition. I laboratoriediskar och i möss gjorde denna kemiska tvärkommunikation tumörceller mer benägna att migrera och invadera, viktiga steg på vägen mot metastasering.
Att göra ett tveeggat svärd till ett säkrare verktyg
Ur ett populärvetenskapligt perspektiv är huvudbudskapet att paclitaxel kan fungera som ett tveeggat svärd: medan det attackerar tumörer instruerar det också vissa immunceller att hjälpa cancern att flytta till avlägsna organ. Nab‑paclitaxel verkar undvika att utlösa denna specifika immuna missriktning. Den uppmuntrande nyheten är att blockering av TREM2 — eller delar av FGF2–EGR1–TREM2‑signalvägen — kan skilja paclitaxels tumörkrympande fördelar från dess metastas‑främjande risker i djurmodeller. Om liknande strategier visar sig vara säkra och effektiva hos människor, kan läkare kanske fortsätta använda ett välkänt, allmänt tillgängligt cellgift samtidigt som man dämpar dess benägenhet att uppmuntra cancerspridning, vilket kan leda till bättre långsiktiga resultat för patienterna.
Citering: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Nyckelord: bröstcancer, paclitaxel, tumörmikromiljö, makrofager, metastas