Clear Sky Science · sv
Pålitlig ombyggnad av antikroppsinteraktomet inne i cellen
Göra antikroppar till små verktyg inne i våra celler
Antikroppar är välkända som blodomloppets precisa vapen som hittar virus och andra hot. Men i många sjukdomar, inklusive Alzheimers, Parkinsons och vissa cancerformer, sker huvuddramatiken inne i cellerna — dit vanliga antikroppar sällan når eller fungerar väl. Den här studien visar hur man systematiskt kan bygga om befintliga antikroppar till mindre ”intrabodies” som fungerar pålitligt inne i levande humana celler, vilket öppnar dörren för nya diagnostiska verktyg, forskningsmetoder och potentiellt framtida terapier som verkar direkt i sjukdomsprocessernas centrum.
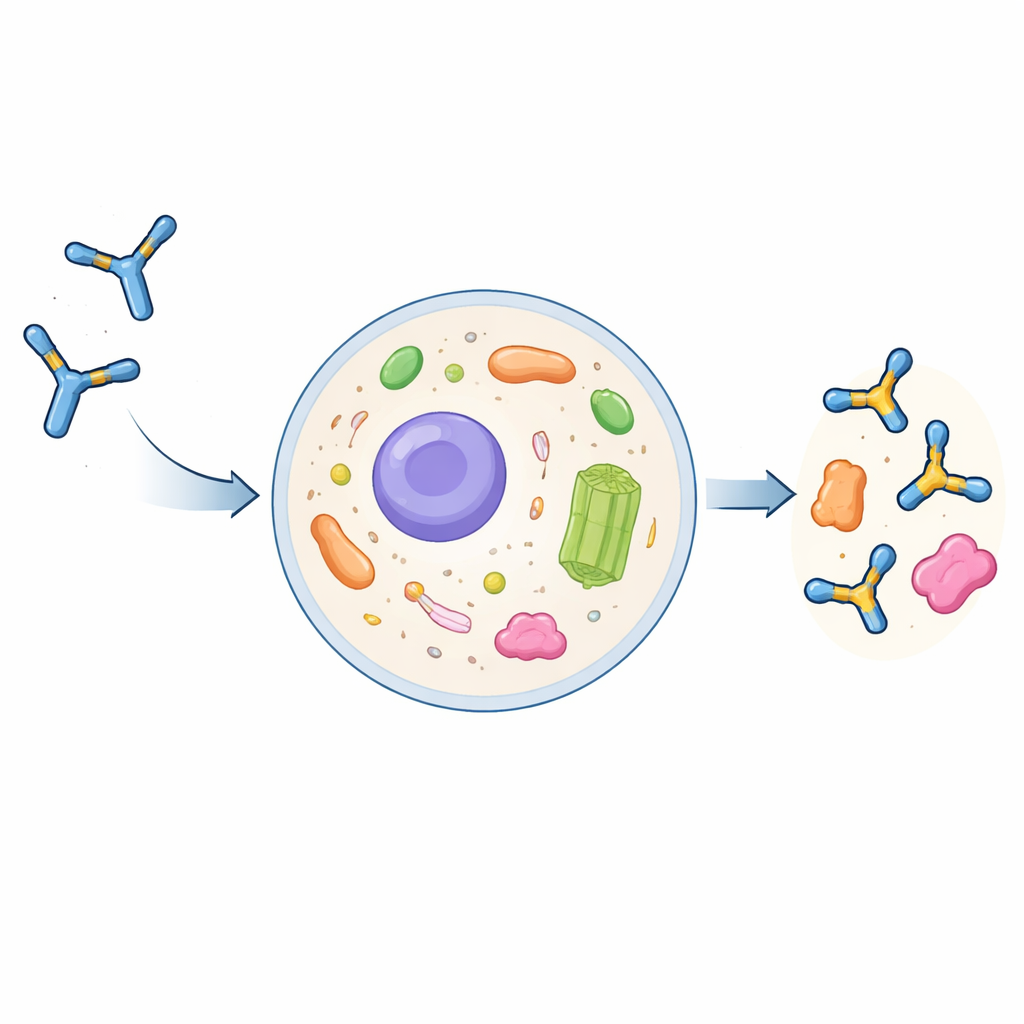
Varför vanliga antikroppar har svårt inne i celler
Fullstora antikroppar är stora, Y‑formade proteiner som utvecklats för att verka utanför cellerna. De monteras och kemiskt modifieras i cellens sekretoriska väg och släpps sedan ut i blodomloppet. Om de tas upp av celler hamnar de oftast i nedbrytningskompartment snarare än i cellens vätskehaltiga inre, cytoplasman. Forskare kan skära ner antikroppar till deras väsentliga igenkänningsdelar, så kallade single‑chain variable fragments (scFvs), och uttrycka dessa som intrabodies inne i celler. Dessa intrabodies tenderar emellertid ofta att klumpa ihop sig, bli olösliga och förlora förmågan att binda sina mål. Hittills har det saknats ett generellt, pålitligt recept för att förvandla en konventionell antikropp till en väluppförd intrabody.
Att hitta designreglerna för lösliga intrabodies
Forskarna började med att mäta hur väl 45 olika intrabodies höll sig lösta när de producerades i humana celler. De jämförde systematiskt många proteinegenskaper — såsom total hydrofobicitet, förutspådd strukturkvalitet och egenskaper hos bindningslooparna — för att se vilka som bäst förklarade om en intrabody förblev löslig. En enkel faktor framstod tydligt: nettoladdningen vid nära‑fysiologiskt pH. Intrabodies med starkt negativ nettoladdning var mycket mer benägna att förbli lösliga, medan de med neutral eller positiv laddning tenderade att aggregera. Andra sofistikerade prediktorer, inklusive strukturkonfidenspoäng från AlphaFold‑systemet, korrelerade inte med löslighet. Detta gjorde det möjligt för teamet att bygga en praktisk, laddningsbaserad modell som kan uppskatta hur stor del av en intrabody som kommer att finnas i den lösliga fraktionen av ett cellextrakt.
Omkonstruera länkar och domäner för bättre beteende
Med denna insikt fokuserade teamet på egenskaper som enkelt kunde justeras utan att störa hur en intrabody känner igen sitt mål. Ett nyckelelement är den korta peptid‑”länkaren” som kopplar de två variabla domänerna. De flesta befintliga konstruktioner använder neutrala länkar som inte ändrar laddning. Genom att byta in negativt laddade aminosyror på dessa positioner kunde forskarna sänka intrabodyns totala laddning, vilket dramatiskt förbättrade lösligheten samtidigt som bindningen till målet bevarades. De upptäckte också att ordningen på de variabla domänerna (om den tunga delen eller den lätta delen kommer först) och specifika ramverkspositioner utanför bindningslooparna påverkar hur lätt proteinet veckas och håller sig löst. Att välja en domänordning som skyddar mer sköra regioner och införa omsorgsfullt placerade laddningsändrande mutationer ökade prestandan ytterligare.
Använda artificiell intelligens för att bygga intrabodies i stor skala
För att gå bortom en‑och‑en‑trial‑and‑error kombinerade författarna sina enkla laddningsregler med avancerad proteindesignmjukvara baserad på djupinlärning. Med utgångspunkt i kända antikroppskonturer använde de en ”inverse folding”‑metod för att föreslå nya sekvenser som fortfarande skulle anta önskad form men ha ytegenskaper — särskilt laddningsmönster — som gynnar stabilitet och löslighet. De begränsade förändringar i de viktiga bindningslooparna för att bevara igenkänning, samtidigt som algoritmen fick omdesigna omkringliggande ytor. Tester visade att många av dessa AI‑styrda intrabodies inte bara var mycket lösliga utan också mer termiskt stabila än mänskligt designade varianter, och de bibehöll förmågan att binda sjukdomsrelevanta mål såsom felveckat SOD1, p53, α‑synuklein och andra proteiner kopplade till neurodegeneration.
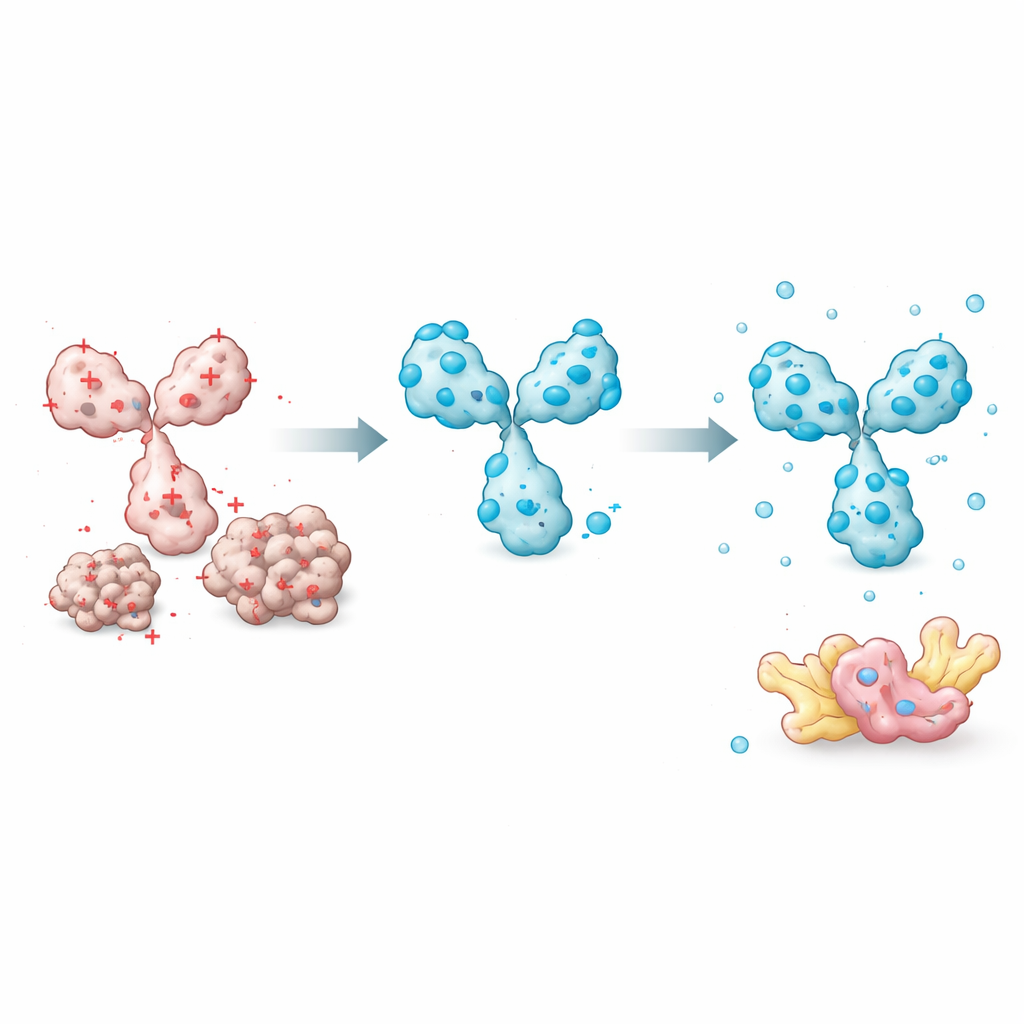
Bygga ett bibliotek av inne‑i‑cellen proteinfångare
Genom att tillämpa dessa regler och verktyg i stor skala omformaterade teamet beräkningsmässigt 672 antikroppar till intrabodies som förutspåddes fungera bra inne i celler. Dessa konstruerade molekyler täcker mer än 60 olika intracellulära mål, inklusive proteiner involverade i Alzheimers, Parkinsons och Huntingtons sjukdomar, liksom cancerrelaterade faktorer och post‑translationella modifieringar som fosforylering och acetylering. I experiment lyckades utvalda intrabodies fånga upp specifika sjukdomsassocierade proteiformer, såsom muterat SOD1 eller specifika former av α‑synuklein, samtidigt som de ignorerade normala varianter. Alla sekvenser släpps öppet, och författarna tillhandahåller ett webbverktyg som låter andra uppskatta intrabody‑löslighet från sekvens med samma laddningsbaserade modell.
Vad detta betyder för framtida läkemedel och forskning
I praktiska termer förvandlar detta arbete den stora befintliga samlingen av antikroppar — många redan studerade i kliniska sammanhang — till en verktygslåda som på ett tillförlitligt sätt kan anpassas för användning inne i celler. Genom att följa en enkel uppsättning designregler kan forskare nu skapa intrabodies som sannolikt fungerar vid första försöket, vilket sparar tid och kostnader. För en lekmannapublik är huvudbudskapet att forskare har funnit ett enkelt sätt att ”omkoppla” våra bästa proteindetektorer så att de fungerar i den trånga inre miljön i levande celler, där många sjukdomar tar sin början. Detta kan påskynda utvecklingen av nya metoder för att spåra, studera och så småningom behandla tillstånd som drivs av felveckade eller funktionsstörda proteiner.
Citering: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Nyckelord: intrabodies, antikroppskonstruktion, proteinslöslighet, neurodegenerativ sjukdom, artificiell intelligens inom biologi