Clear Sky Science · sv
In vivo dubbel RNA‑Seq avslöjar viktiga effektorfaktorer för epitelbarriärens uppluckring av en extracellulär patogen
Hur vissa mikrober smyger förbi våra cellulära stängsel
Våra organ är täckta av tätt packade celler som fungerar som väggar och håller blod, mikrober och toxiner där de hör hemma. Ändå lyckas vissa mikrober ändå slingra sig mellan dessa celler och sprida sig i kroppen. Denna studie visar i detalj hur bakterien som orsakar leptospiros, en allvarlig sjukdom globalt, tyst når organ som levern och njurarna och sedan använder ett smart knep med kalcium inne i våra celler för att bända upp dessa skyddande barriärer.
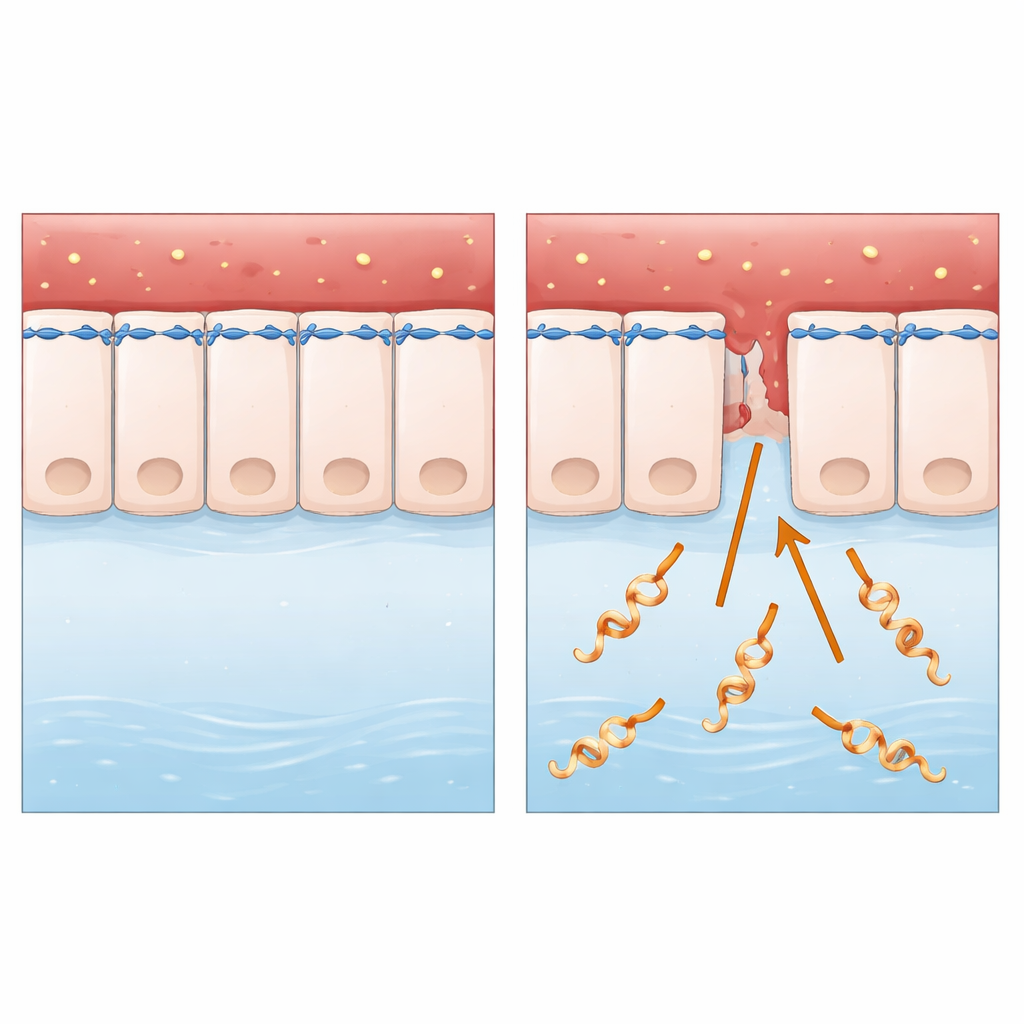
En smygande angripare i djur- och människovävnader
Forskningen fokuserar på Leptospira interrogans, en spiralformad bakterie som sprids främst från djur till människor via förorenat vatten eller jord. Efter inträde genom små hudsår eller slemhinnor färdas den via blodomloppet och kan utlösa svår sjukdom, inklusive lever‑ och njursvikt samt inre blödningar. Till skillnad från många välstuderade mikrober lever Leptospira utanför celler och saknar några av de klassiska ”molekylära vapnen” som forskare normalt letar efter. Det gjorde den till ett idealiskt fall för att ställa en grundläggande fråga: hur tar en till synes enkel, fritt levande bakterie sig så effektivt över intakta cellager?
Att iaktta värd‑ och mikrobgener tala samtidigt
För att fånga infektionsprocessen i en levande organism använde teamet dubbel RNA‑sekvensering i marsvin, en modell för akut leptospiros. Denna metod läser av vilka gener som är påslagna eller avstängda i både värd och patogen samtidigt. Forskarna infekterade marsvin och samlade in lever‑ och njurvävnad efter en och tre dagar. Tidigt, trots höga bakteriemängder, förändrade djurens celler knappt sin genaktivitet, vilket antyder att Leptospira initialt glider under immunförsvarets radar. Vid dag tre visade sig dock båda organen reagera kraftigt, särskilt levern: gener kopplade till inflammation, cell‑cell‑förbindelser och cellernas interna skelett förändrades markant, vilket pekar på en aktiv omformning av vävnadsbarriärerna.
Att bryta den cellulära blixtlåset från utsidan in
Cellager förseglas av tighta junctions och adherensjunctions, som länkar grannceller och förankrar dem till en ring av aktin och myosin — samma proteinpar som hjälper muskler att dra ihop sig. Mikroskopi av humana epitelceller infekterade med Leptospira visade att deras form ändrades, glipor öppnades mellan celler och viktiga junction‑proteiner försvagades eller hamnade fel. Viktigt är att cellerna inte dog, vilket betyder att barriären demonterades snarare än förstördes. Forskarna såg också tecken på stress i cellernas proteinveckningsfabriker, men att blockera denna stress återställde inte junctions, vilket pekade mot en annan syndabock.
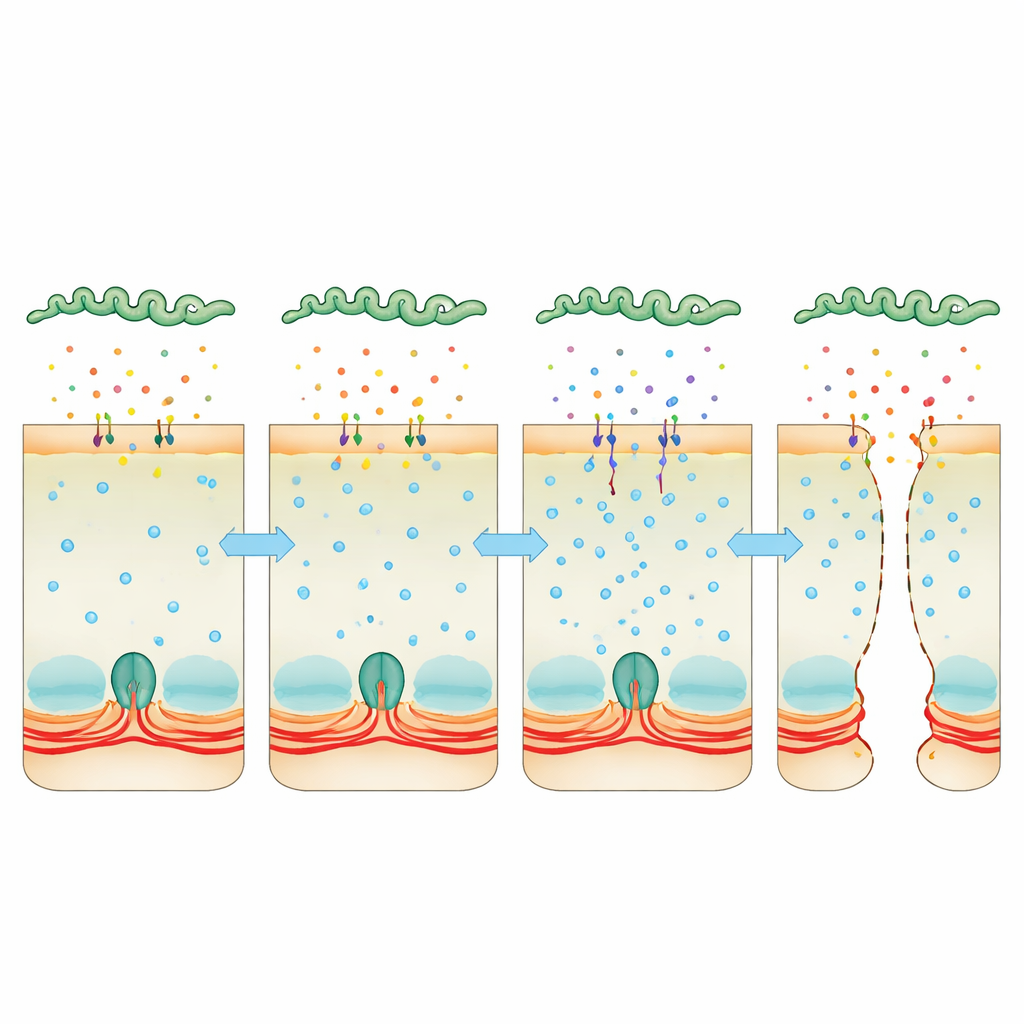
Kapande av kalcium som en dold kofot
Uppmärksamheten riktades mot kalcium, en universell signal inne i celler som kan dra åt eller slappna av aktin‑myosin‑ringen. Infekterade celler ackumulerade mer kalcium, och detta kopplades till ökad aktivitet av myosin light chain‑kinas, ett enzym som får den kontraktila ringen att dra i junctions. När teamet använde en förening som fångar upp kalcium, eller läkemedel som hämmar kalmodulin eller detta kinas, höll sig cellagren mer intakta och bakterierna hade svårare att pressa sig igenom. Samtidigt visade djupsekvensering av bakteriellt RNA att Leptospira inne i värden kraftigt ökar produktionen av två ”virulens‑modifierande” proteiner som liknar toxiner. Dessa proteiner utsöndras i omgivningen, fäster vid värdceller och påträffas inne i dem. När bakterier saknade ett eller båda dessa proteiner var de mycket mindre kapabla att passera cellager eller orsaka dödlig sjukdom, och deras utsöndrade vätska ökade inte längre kalciumnivåerna eller demonterade junctions lika effektivt.
Vad detta betyder för sjukdom och framtida försvar
Tillsammans målar resultaten upp en tydlig bild. Efter att ha smugit in i kroppen nästan omärkt börjar Leptospira utsöndra toxinliknande virulens‑modifierande proteiner. Dessa proteiner binder till epitelceller och rubbar kalciumbalansen inuti, vilket i sin tur aktiverar en kontraktil väg som drar isär det cellulära ”blixtlås” som håller grannceller ihop. När tighta och adherensjunctions luckras upp uppstår mikroskopiska glipor som tillåter bakterierna att passera mellan celler, kolonisera organ och utlösa svår sjukdom. Genom att peka ut denna kalciumdrivna mekanism och de bakteriella proteinerna bakom den öppnar studien en väg mot nya strategier — såsom att blockera dessa proteiner eller deras signalslinga — för att stärka våra cellulära stängsel och begränsa spridningen av leptospiros och möjligen andra infektioner som utnyttjar liknande taktik.
Citering: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Nyckelord: leptospiros, epitelbarriär, kalciumsignalering, bakterietoxiner, värd–patogen‑interaktioner