Clear Sky Science · sv
Supercharging-förbättrad nDIA-MS möjliggör global profilering av läkemedelsinducerade förändringar i proteomets löslighet
Varför proteiners beteende spelar roll bortom enkla mängdmässiga förändringar
Läkemedel kan påverka inte bara hur mycket av ett protein en cell producerar, utan också var proteinet befinner sig och om det flyter fritt eller klumpar ihop sig på cellulära strukturer. Dessa förändringar i ”var” och ”hur” proteiner existerar inuti celler är nära kopplade till sjukdomar som cancer och neurodegeneration, men de är svåra att mäta i stor skala. Denna studie presenterar ett snabbt, kraftfullt sätt att skanna tusentals mänskliga proteiner samtidigt för att se hur deras löslighet – om de är i ett fritt eller mer fastnat tillstånd – förändras när celler utsätts för två ofta använda experimentella läkemedel.
Ett snabbare, skarpare sätt att studera proteiner
Författarna bygger vidare på en kärnteknik i modern biologi: masspektrometri, en metod som väger och räknar proteinfragment. Standardmetoder är redan mycket bra på att berätta hur mycket av varje protein som finns, men de har svårare att avslöja förändringar i proteiners tillstånd, såsom att flytta ut på DNA eller in i täta samlingar. Här förfinar forskarna en variant av masspektrometri kallad narrow-window data-independent acquisition (nDIA-MS). Genom att tillsätta små kemiska hjälpmedel, kallade supercharging-reagenser, till vätskan som för peptider genom instrumentet ökar de de elektriska laddningarna på dessa fragment och förstärker signalen avsevärt.
Efter att ha testat två vanliga supercharging-tillsatser, dimetylsulfoxid (DMSO) och m-nitrobenzylalkohol (mNBA), finner de att 3% DMSO ger den största totala signalförstärkningen och det högsta antalet detekterade proteiner, medan mNBA är bättre på att öka antalet och laddningen hos individuella peptidfragment. Med den optimerade uppställningen kan teamet identifiera cirka 9 600 humana proteiner från bara en mikrogram av en standardcell‑digest i ett 15-minuterslopp – en anmärkningsvärd kombination av hastighet och djup för rutinexperiment. Denna prestanda banar väg för att använda nDIA-MS inte bara för att räkna proteiner, utan för att undersöka hur deras fysiska tillstånd svarar på stress.
Att omvandla löslighet till en avläsning av cellulära förändringar
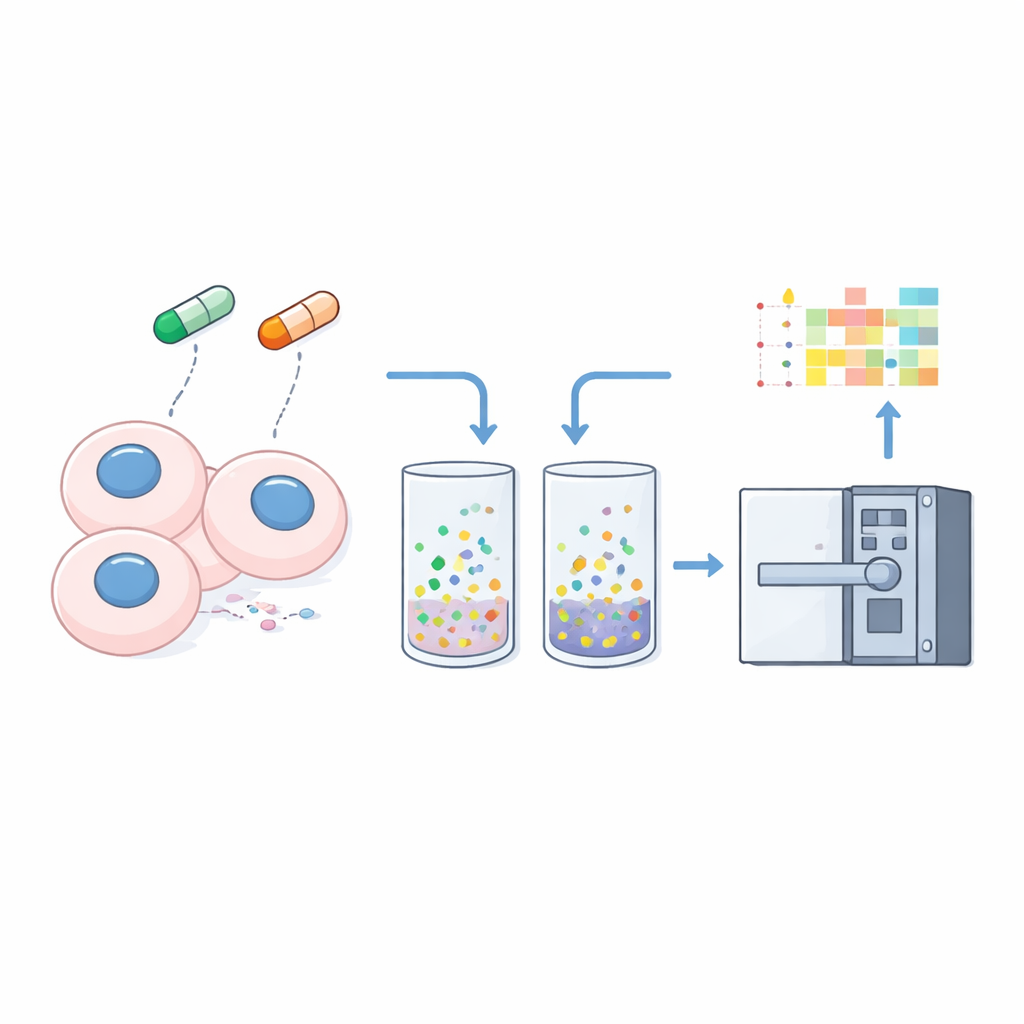
För att omvandla löslighet till en mätbar signal förbehandlar forskarna cellerna försiktigt med ett milt rengöringsmedel som extraherar fritt lösliga proteiner och lämnar kvar material som är hårt bundet till DNA, membran eller andra strukturer. De analyserar både helcelllysatet och detta ”olösliga” pellet från tre cancercellinjer med den optimerade nDIA-MS-metoden. Genom att jämföra varje proteins abundans i pelletet i förhållande till helcellsprovet beräknar de ett enkelt ”olöslighetskvot” – högre värden tyder på starkare association med cellulära strukturer, lägre värden tyder på ett mer lösligt, fritt tillstånd.
Teamet utsätter sedan cellerna i bara en timme för två läkemedel: MG132, en proteasomhämmare som förhindrar att celler bryter ner oönskade proteiner, och ML‑792, en hämmare av SUMO‑aktivering som stör ett viktigt proteinsättningssystem. Den korta exponeringen är avsiktlig; den syftar till att fånga snabba, tidiga förändringar i proteiners beteende innan genuttrycksändringar hunnit slå igenom fullt ut. Även inom detta korta fönster kan de kvantifiera förändringar i löslighet och abundans för 8 694 proteiner och bekräfta att deras fractionering tydligt separerar klassiska lösliga proteiner, som tubulin, från kromatinbundna proteiner, som histoner.
Läkemedel som omformar cellens proteinlandskap
MG132 och ML‑792 orsakar omfattande men distinkta omstruktureringar av proteiners löslighet. MG132 gör över tusen proteiner mer olösliga och mer än sexhundra mer lösliga över de tre cellinjerna. Många påverkade proteiner befinner sig i korsningen mellan kvalitetskontroll av proteiner, DNA‑skaderespons, genreglering och autofagi – cellens självstädningssystem. Till exempel blir komponenter av proteasom‑aktiverarkomplexet och adaptrar som hjälper till att märka felaktiga proteiner mindre lösliga, vilket antyder att när nedbrytningen blockeras så fastnar nyckelfaktorer för kvalitetskontroll själva på strukturer såsom kromatin eller cellulära membran. Autofagiproteiner och aktörer i skaderesponsen, inklusive stressregulatorn HSF1, skiftar också mot mer olösliga, kondensatliknande tillstånd, i linje med bildning av nukleära stresskroppar.
ML‑792, däremot, riktar sig starkt mot proteiner som är involverade i transkription och i SUMO‑systemet självt. Hundratals proteiner blir antingen mer olösliga eller mer lösliga när SUMO‑aktivering blockeras, och kärn‑SUMO‑proteiner flyttar in i den lösliga poolen, som förväntat. Studien framhäver slående beteenden: underenheter av RNA‑polymeras III blir mer olösliga, vilket tyder på förändrad nukleär import eller kromatinbindning; viktiga repressorer associerade med nukleära kroppar, såsom SP100 och DAXX, blir mer lösliga, vilket indikerar att SUMO‑markeringar hjälper till att hålla dem sequesterade i dessa kompartment. När båda läkemedlen appliceras ensamma eller i följd visar vissa proteiner, inklusive NAB2, SMAD2 och RB1, koordinerade eller till och med motsatta löslighetsförändringar, vilket avslöjar ett nyanserat samspel mellan ubiquitin‑ och SUMO‑märkningssystemen i kontrollen av proteinlokalisering.
Vad detta betyder för framtida läkemedelsforskning
För icke‑specialister är huvudbudskapet att proteiner inte bara ändrar mängd när celler utsätts för stress eller läkemedelsbehandling; de rör sig också, kondenserar och ändrar hur hårt de är bundna till cellulära strukturer. Detta arbete levererar ett högfrekvent, proteomöverblickande sätt att observera dessa förflyttningar. Genom att kombinera ett finjusterat masspektrometri‑arbetsflöde med en enkel jämförelse mellan lösligt och olösligt visar författarna att vanliga experimentella läkemedel snabbt omorganiserar det interna proteinlandskapet på sätt som standardmätningar av abundans skulle missa. Metoden öppnar dörren för att kartlägga hur kandidatläkemedel omformar proteintillstånd genom hela cellen, vilket hjälper forskare att upptäcka oväntade mål, stressvägar och svagheter som kan vara avgörande för att förstå både terapeutisk verkan och biverkningar.
Citering: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Nyckelord: proteomets löslighet, masspektrometri, proteasomhämmaren MG132, SUMOylationshämmaren ML-792, proteiners tillståndsövergångar