Clear Sky Science · sv
Konstruerad intern arkitektur hos kärn-skal-lipidnanopartiklar främjar effektiv mRNA-frisättning från endosomer
Varför denna nya leveransmetod spelar roll
Många av de mest spännande nya läkemedlen, från COVID-19-vacciner till experimentella cancerbehandlingar, bygger på budbärar-RNA, eller mRNA. Men det finns ett seglivat problem: när dessa känsliga strängar väl kommer in i våra celler fastnar och förstörs de flesta i små inre säckar som kallas endosomer. Denna studie introducerar en smart omdesign av de små fettbubblorna, kända som lipidnanopartiklar, som bär mRNA. Genom att omorganisera deras inre struktur runt en solid guldkärna förbättrar forskarna dramatiskt hur mycket mRNA som slipper ut i cellens arbetsyta, där det faktiskt kan tillverka användbara proteiner.
Ge de små kurirerna en bättre kroppslayout
Dagens mRNA-vacciner och -terapier förlitar sig mest på mjuka, klumpformade partiklar gjorda av en blandning fetter som omsluter mRNA. I teorin bör särskilda ”joniserbara” fetter i dessa partiklar bli positivt laddade i det sura inre i endosomer och riva upp endosomalmembranet, vilket frigör mRNA. I praktiken neutraliserar mRNA:s negativa laddning mycket av denna effekt, så endast cirka 2 procent av det levererade mRNA når någonsin cellens proteinproducerande maskineri. Författarna ställde en enkel men kraftfull fråga: i stället för att bara ändra fettens kemi, vad händer om man omkonstruerar partikelns inre arkitektur för att kontrollera var mRNA och lipider ligger i förhållande till varandra?
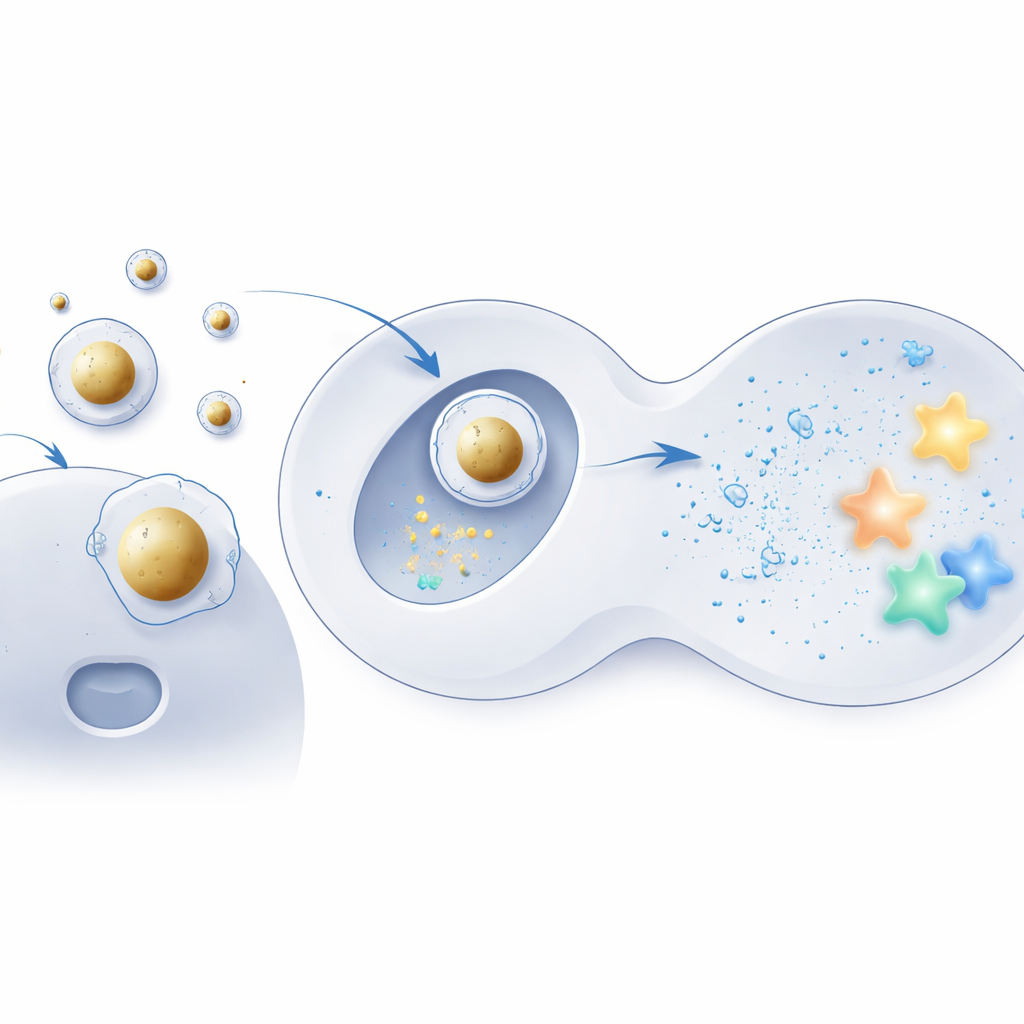
Bygga ett guldcentrerat leveransskal
För att testa idén använde teamet små guldsfärer som styva kärnor och belade dem med samma joniserbara lipider som används i konventionella formuleringar. Det negativt laddade mRNA kondenserades först på dessa kärnor, och först därefter sveptes byggnadsverket in i en välkänd blandning av hjälpfetter och stabiliserande molekyler, vilket skapade en ordnad kärn–skal-struktur. Elektronmikroskopi och datorsimuleringar visade att dessa ”Au‑LNPs” var mycket enhetliga, termodynamiskt stabila och behöll sin form väl i vattenliknande, kroppslika förhållanden. Viktigt är att deras övergripande fettkomposition förblev densamma som hos standardpartiklar, vilket isolerar intern struktur — inte ingredienser — som den avgörande förändringen.
Hur ett omarrangerat inre ökar flykten
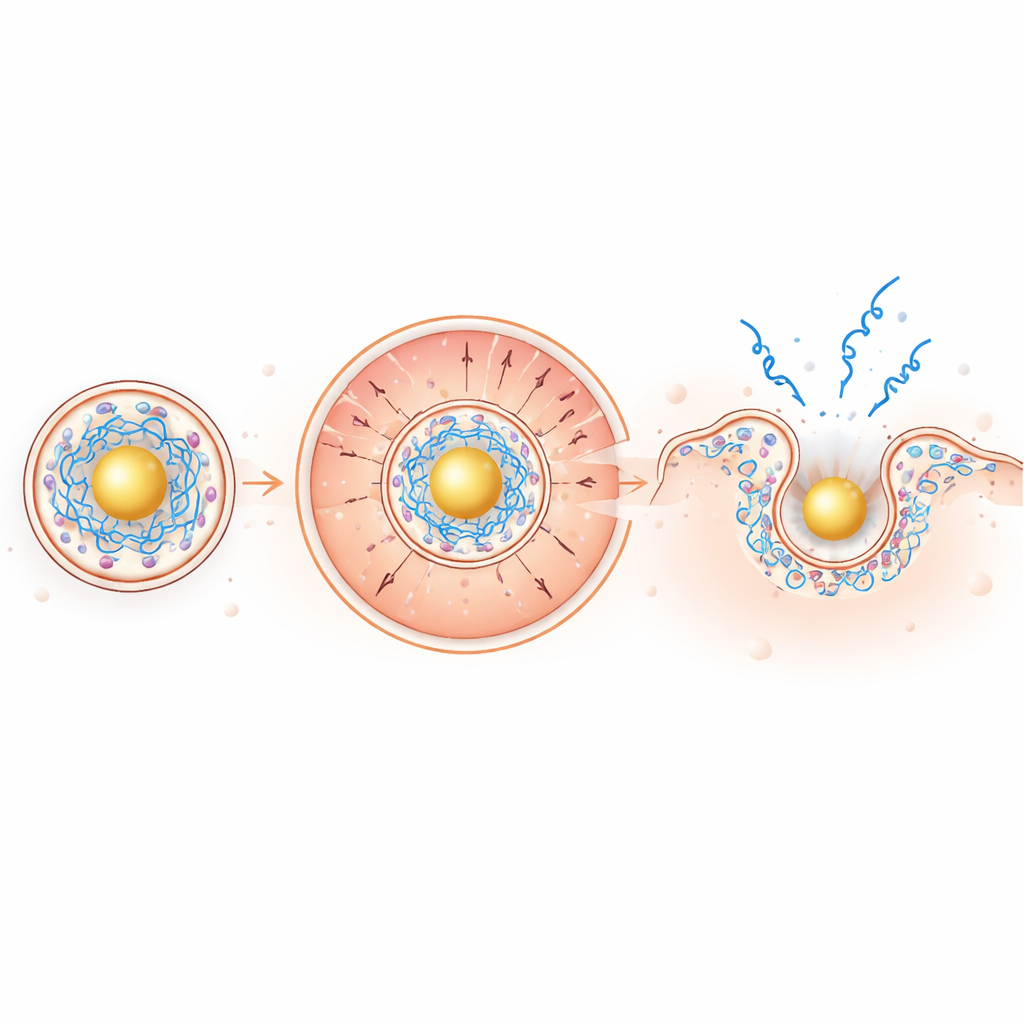
I det lätt sura endosomala miljön blir guldbaserade kärnan starkt positiv, vilket drar det negativt laddade mRNA:t inåt samtidigt som de positivt laddade joniserbara lipiderna pressas utåt mot det omgivande membranet. Denna laddningsdrivna segregation koncentrerar membranstörande lipider precis där de behövs. I tester på modellmembran och i röda blodkroppar var de nya partiklarna mer effektiva på att perforera membran vid låg pH samtidigt som de var inaktiva vid neutralt pH, en önskvärd säkerhetsaspekt. I levande celler visade avbildning av fluorescerande mRNA ungefär en dubblering i endosomal flykt och en häpnadsväckande ~100-faldig ökning i hur långt mRNA spreds genom cytoplasman jämfört med konventionella partiklar.
Från odlingsskålar till möss: starkare signaler och starkare skydd
Dessa fysiska fördelar översattes till verkliga biologiska vinster. Över flera celltyper gav guldkärnepartiklarna mycket högre produktion av rapportproteiner än standardformuleringar, särskilt vid låga doser. I möss ökade de mRNA-styrda proteinutbytet upp till fem- till sjufaldigt efter injektioner i muskel eller i vener, utan att förändra var i kroppen partiklarna tenderade att ansamlas. När de användes för att leverera ett SARS‑CoV‑2 spike-mRNA-vaccin fördubblade de omkonstruerade partiklarna ungefär antikroppsnivåerna efter första dosen och ökade dem ytterligare efter en boosterdos, samtidigt som de också frambringade mer potenta virusneutraliserande antikroppar. I en utmanande modell för trippelnegativ bröstcancer krympte mRNA-cancervacciner som levererades av de nya partiklarna tumörer mer effektivt, sänkte tumöraktivitetssignaler och förlängde betydligt överlevnaden.
Säkerhet och en väg mot framtida läkemedel
Trots att de använder guld i kärnan verkade partiklarna väl tolererade i möss. Kroppsvikter, inflammationsmarkörer och vävnadsundersökningar visade ingen allvarlig toxicitet, och guldnivåerna i organ sjönk tillbaka mot baslinjen inom två dagar. Författarna understryker att guld huvudsakligen tjänar som ett proof-of-concept-stomme: samma interna designprincip kan tillämpas på andra säkra eller biologiskt nedbrytbara material. Huvudbudskapet för icke-specialister är att hur vi packar mRNA inuti dess lilla bärare kan vara lika viktigt som vad vi packar det med. Genom att ge lipidnanopartiklar en mer disciplinerad intern layout erbjuder detta arbete ett nytt sätt att övervinna en långvarig flaskhals i mRNA-leverans — att låsa upp mer effektiva vacciner och terapier inom infektionssjukdomar, cancer och bortom.
Citering: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Nyckelord: mRNA-leverans, lipidnanopartiklar, endosomal flykt, nanomedicin, RNA-vacciner