Clear Sky Science · sv
FGF13 fungerar som en regulator av ERK/aerob glykolys-axeln i det inflammatoriska tillståndet vid sepsisinducerad lungskada
Varför denna studie är viktig för patienter med allvarliga infektioner
Sepsis är en livshotande komplikation av infektion som kan få lungorna att svikta inom några timmar, vilket gör att patienterna blir beroende av respirator och har hög dödlighet. Denna studie undersöker ett lite känt protein inne i våra celler, kallat FGF13, och visar hur det bidrar till den okontrollerade inflammationen och det höga energibehovet som allvarligt skadar lungorna vid sepsis. Genom att kartlägga denna dolda styrningskrets pekar arbetet på nya läkemedelsmål som kan dämpa stormen i lungorna utan att stänga av kroppens hela immunsystem.
En dold aktör i lungskada vid sepsis
Forskarnas första steg var att jämföra lungvävnad från septiska möss och mänskliga patienter med vävnad från icke-septiska kontroller. De undersökte en familj molekyler som kallas fibroblasttillväxtfaktorer, vilka bidrar till att upprätthålla lungan. Bland dessa stack FGF13 ut: dess nivåer var markant lägre i lungorna hos septiska patienter och djur. När teamet kartlade var FGF13 fanns, fann de det främst inne i två nyckelcellstyper: endotelceller, som bildar blodkärlens inre beklädnad, och makrofager, immunceller som känner av och förstärker inflammation. I septiska lungor var FGF13-positiva endotelceller och makrofager kraftigt reducerade, vilket antyder att förändringar i detta protein kan vara kopplade till svår lungskada.
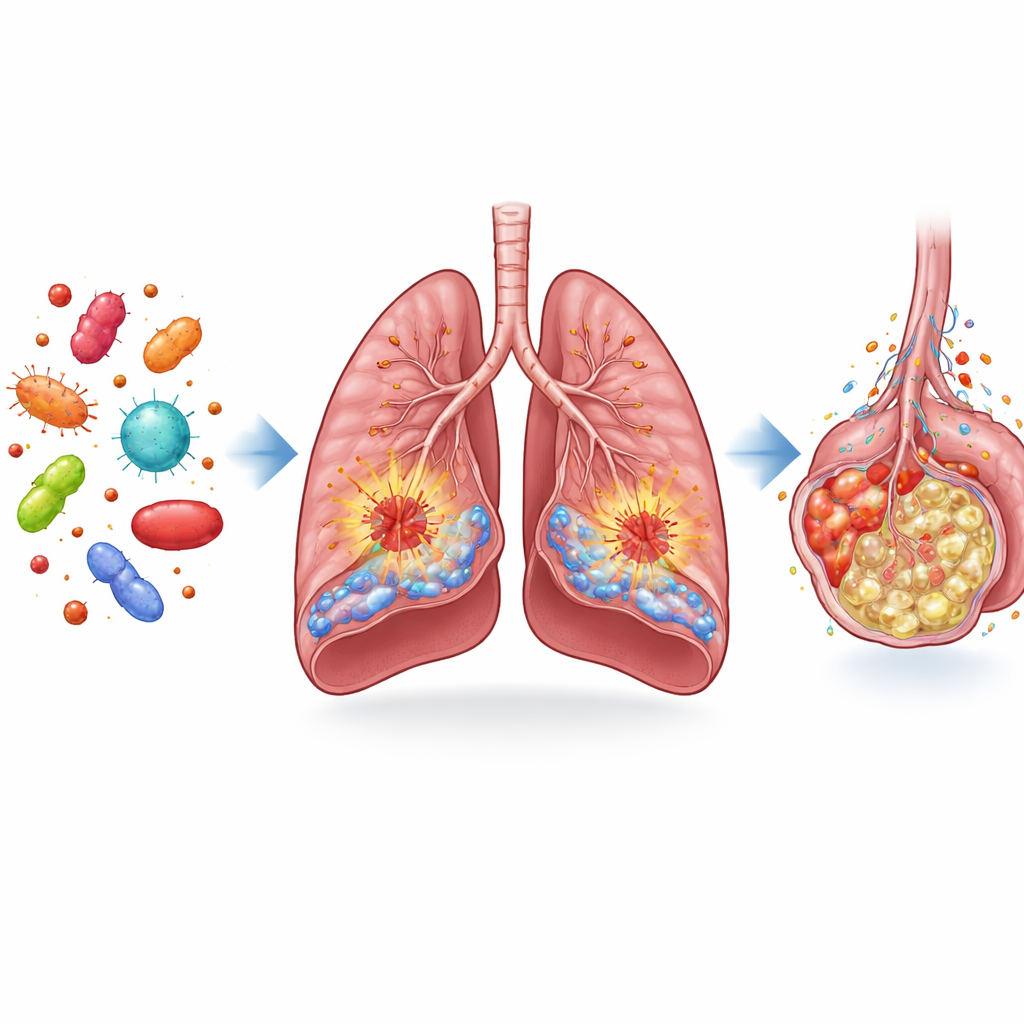
Hur FGF13 förvandlar lungens försvarare till skadeframkallare
För att testa vad FGF13 faktiskt gör använde teamet genetiska verktyg i möss för att antingen ta bort det från specifika celler eller tvinga dessa celler att producera mer av det. När FGF13 togs bort endast i endotelceller hade septiska möss mindre läckande, svullna lungor, färre invaderande immunceller och bättre överlevnad. Motsatsen inträffade när endotelceller konstruerades för att överproducera FGF13: lungödem, blödningar och ansamling av inflammatoriska celler förvärrades. En liknande bild framträdde i makrofager. Möss som saknade FGF13 i dessa immunceller visade svagare inflammatoriska svar och mindre lungskada, medan makrofager tvingade att producera extra FGF13 släppte ut fler inflammatoriska molekyler och förvärrade skadan. I cellkultur gjorde sänkt FGF13 blodkärlsceller och makrofager mindre klibbiga, mindre inflammerade och mindre giftiga för sina grannar.
Inflammerade celler växlar till ett sockerslukande läge
Inflammerade celler, likt cancerceller, skiftar ofta sin energistrategi: i stället för att långsamt förbränna bränsle med syre, bryter de snabbt ner socker i en process kallad aerob glykolys och bildar mjölksyra. Författarna fann att FGF13 starkt uppmuntrar detta skifte. I septiska möss som saknade FGF13 i antingen endotelceller eller makrofager var blodets laktatnivåer lägre. I odlingar tog celler med reducerat FGF13 upp mindre glukos och producerade mindre laktat efter inflammatorisk stimulering, medan celler med extra FGF13 visade förbättrad glykolys. När forskarna blockerade glykolys med ett läkemedel dämpades till stor del den inflammationsfrämjande effekten av överskott av FGF13, vilket kopplar molekylens skadliga roll direkt till detta sockerförbränningsprogram.
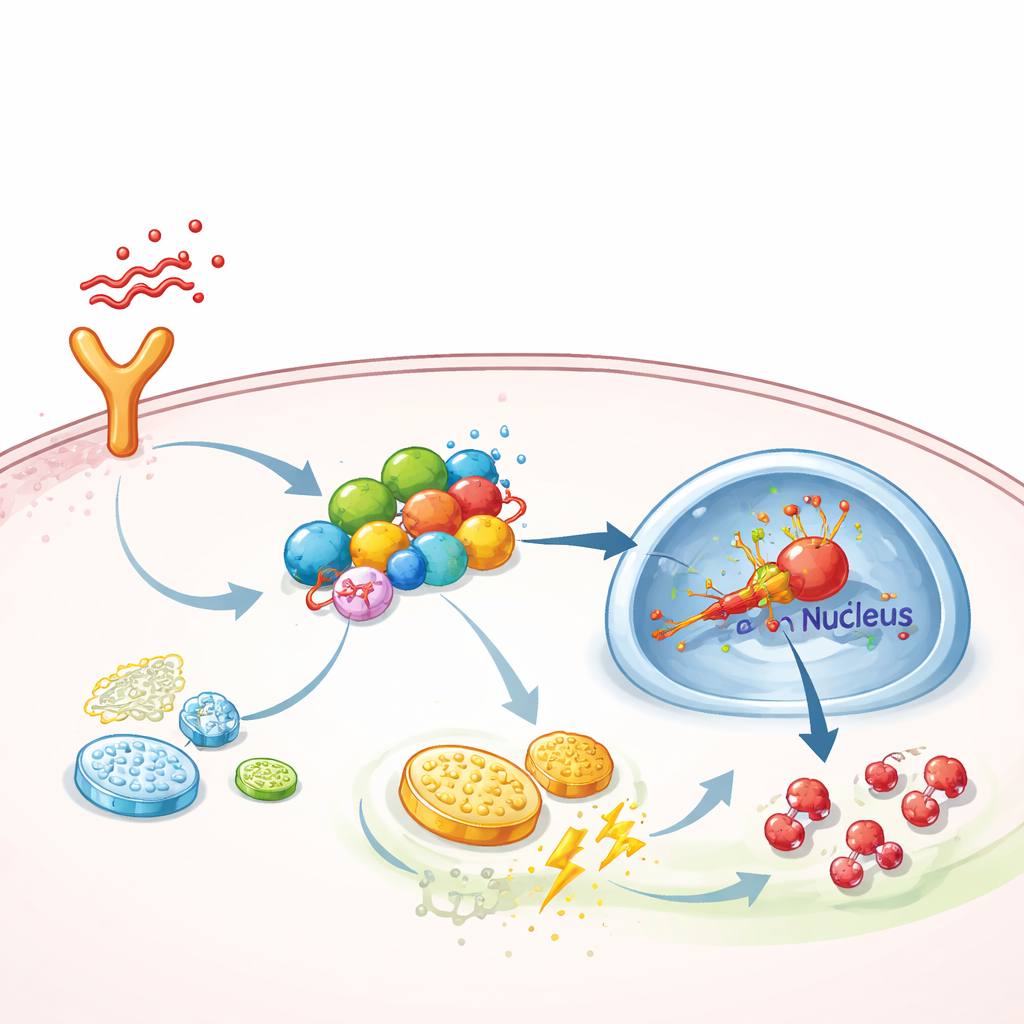
En molekylär ställning som förstärker inflammatorisk signalering
För att gå djupare undrade teamet hur FGF13 skjuter celler mot denna högväxlande ämnesomsättning. De upptäckte att FGF13 fysiskt binder till flera signalproteiner som bildar en kedja från ytreceptorer till cellkärnan — specifikt TAK1–MEK–ERK-vägen, som är känd för att aktivera en huvudregulator av lågsyresvar kallad HIF-1α. FGF13 fungerar som ett slags ställning som håller dessa komponenter samman så att signaler går mer effektivt. När FGF13 minskades sjönk aktiveringen av ERK och HIF-1α, och glykolysen avstannade; när FGF13 ökade blev vägen hyperaktiv. Överuttryck av HIF-1α i möss utplånade den skyddande effekten av att ta bort FGF13, medan en selektiv ERK-hämmare, SCH772984, neutraliserade skadorna orsakade av FGF13-överproduktion och förbättrade lungtillståndet hos septiska djur.
Vad detta betyder för framtida sepsisbemötande
För en lekmannaläsare är huvudbudskapet att sepsisinducerad lungskada inte bara är slumpmässig vävnadsförstörelse; den drivs av en specifik molekylär krets inne i endotelceller och makrofager. FGF13 sitter i centrum av denna krets och hjälper till att bygga ett signaleringsnav som tvingar celler in i ett sockerslukande, starkt inflammatoriskt tillstånd. Även om FGF13-nivåerna sjunker under sepsis — troligen som en del av en bredare stressreaktion — visar denna studie att det kvarvarande proteinet fortfarande är en potent skadeorsak. Genom att blockera antingen FGF13:s signaleringspartners eller det glykolytiska skifte det främjar kan det bli möjligt att minska lungsvullnad, läckage och inflammation utan att förlama kroppens förmåga att bekämpa infektion. Detta arbete belyser därmed FGF13 och ERK–HIF‑1α–glykolys-axeln som lovande ledtrådar för att utveckla mer precisa, säkrare behandlingar av sepsisrelaterat lungsvikt.
Citering: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Nyckelord: sepsisinducerad lungskada, FGF13, endothelial inflammation, aerob glykolys, ERK-signalering