Clear Sky Science · sv
Kombinerad målinriktad och epigenetisk terapi förbättrar antitumör immunitet genom att stabilisera GATA6-beroende MHCI-uttryck i pancreatiskt ductalt adenokarcinom
Varför denna forskning är viktig för bukspottkörtelcancer
Pancreatiskt ductalt adenokarcinom är en av de mest dödliga cancerformerna, till stor del eftersom den undviker immunförsvaret och är resistent mot de flesta läkemedel. Denna studie avslöjar ett särskilt tumörcellstillstånd, drivet av en gen som heter GATA6, som gör bukspottkörtelceller mer synliga för immunangrepp. Författarna visar också hur kombinationen av två typer av läkemedel kan bevara detta sårbara tillstånd och öka mördande T-cellers förmåga att attackera tumörer i experimentella modeller.
Ett tumörcellstillstånd som inbjuder immunförsvaret
Alla bukspottkörtelcancerceller beter sig inte likadant. Vissa bibehåller en mer ordnad, epitel-lik identitet, medan andra övergår mot ett mer rörligt, aggressivt, mesenkymalt liknande tillstånd. Transkriptionsfaktorn GATA6 hjälper till att upprätthålla den epiteliala identiteten och är kopplad till bättre utfall hos patienter. I stora patientkohorter innehöll tumörer med höga GATA6-nivåer fler immunceller, inklusive CD8 ”mördande” T‑celler, än tumörer med lite eller inget GATA6. Med avancerad spatial bildteknik på mänskliga tumörprover fann forskarna att GATA6-positiva cancerceller oftare låg intill CD8 T‑celler och uppvisade högre nivåer av en molekyl som kallas MHCI, som fungerar som en flagga som visar T‑celler vad som finns inne i cellen. Dessa observationer antyder att GATA6 markerar en tumörcellspopulation som naturligt är mer synlig för immunförsvaret. 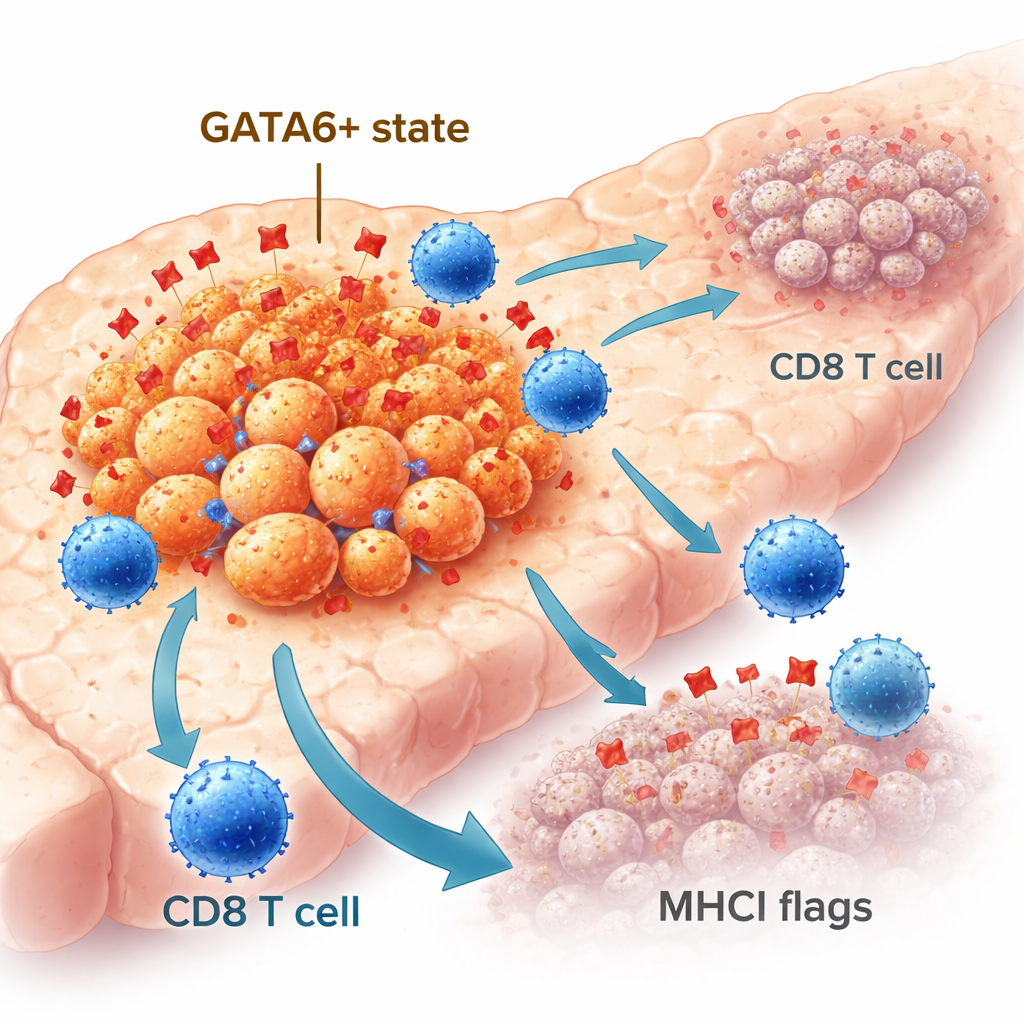
Målinriktad terapi som ökar tumörsynlighet — men med en kostnad
Nästa fråga var om målinriktade läkemedel kunde förstärka denna synlighet ytterligare. Forskarna fokuserade på MEK-hämmare, en läkemedelsklass som blockerar en tillväxtsignalväg som ofta är aktiv i bukspottkörtelcancer. I musbaserade pankreascellinjer och i tumörer odlade i möss samt i patientderiverade xenograftmodeller ökade MEK‑hämning MHCI på ytan av GATA6-höga tumörceller, vilket gjorde dem potentiellt bättre måltavlor för T‑celler. När tumörer med hög GATA6 behandlades med MEK‑hämmare i möss, bromsades tumörtillväxten, MHCI ökade och fler CD8 T‑celler med cytotoxiska molekyler trängde in i tumörerna. Att blockera GATA6 direkt, antingen genom gen‑knockout eller genom snabb nedbrytning av proteinet, upphävde denna MEK‑hämmarinducerade ökning av MHCI och den därpå följande tumörkontrollen, vilket visar att GATA6 är nödvändigt för denna gynnsamma effekt.
Hur tumörer anpassar sig: glider in i ett svårare att döda tillstånd
Berättelsen får dock en twist. Långtidsbehandling med MEK‑hämmare drev många tumörceller att skifta från det GATA6‑positiva epiteliala tillståndet till ett mer mesenkymalt, GATA6‑lågt tillstånd som förknippas med behandlingsresistens. I både musmodeller och patientderiverade xenograft visade MEK‑hämmarbehandlade tumörer så småningom färre GATA6‑positiva celler, fler markörer för epitel‑till‑mesenkymal övergång och i stort sett mindre hållbar nytta. Fastän enskilda GATA6‑positiva celler fortfarande uppreglerade MHCI som svar på läkemedlet, begränsade den minskade storleken på denna population den övergripande förbättringen i tumörantigenpresentation, vilket hjälper till att förklara varför MEK‑hämmare ensamma har varit besvikande i kliniska prövningar för bukspottkörtelcancer.
Epigenetiska läkemedel som håller tumörer i det sårbara tillståndet
För att motverka denna adaptiva flykt vände sig forskarna till histon‑deacetylas‑hämmare, eller HDAC‑hämmare, en klass epigenetiska läkemedel kända för att påverka cellidentitet och immun‑synlighet. I cellkulturer och musmodeller återställde kombinationen av MEK‑hämmare och klass I HDAC‑hämmare såsom domatinostat GATA6‑uttryck som undertryckts av MEK‑hämmning, reverserade tecken på epitel‑till‑mesenkymal övergång och ökade ytterligare MHCI‑nivåerna på tumörceller. Viktigt är att denna kombinationsterapi ledde till starkare infiltration och aktivering av CD8 T‑celler samt mer tumörcellsdöd i ortotopa mustumörer och i en genetiskt modifierad musmodell som noggrant efterliknar mänsklig bukspottkörtelcancer. Utdelningsförsök där CD8 T‑celler avlägsnades eliminerade stora delar av vinsten, vilket bekräftar att kombinationen till stor del verkar genom att stärka de mördande T‑cellerna.
Mot smartare kombinationsterapier för en svår cancer
Sammantaget föreslår studien en strategi där målinriktad MEK‑hämning och epigenetisk HDAC‑hämning används tillsammans för att stabilisera ett GATA6‑drivet tumörcellstillstånd som är rikt på MHCI och därmed väl igenkännbart för immunförsvaret. Genom både att öka antalet GATA6‑positiva celler och att förstärka deras MHCI‑”flaggor” främjar kombinationen djupare CD8 T‑cellsinfiltration, starkare cytotoxisk aktivitet och längre överlevnad i aggressiva musmodeller av bukspottkörtelcancer. Även om HDAC‑hämmare kan ha betydande biverkningar och arbetet är prekliniskt, pekar denna forskning mot framtida behandlingsstrategier som kan para ihop signalvägsriktade läkemedel och noggrant utvalda epigenetiska modifierare för att göra pankreastumörer mer sårbara för kroppens egna immunförsvar. 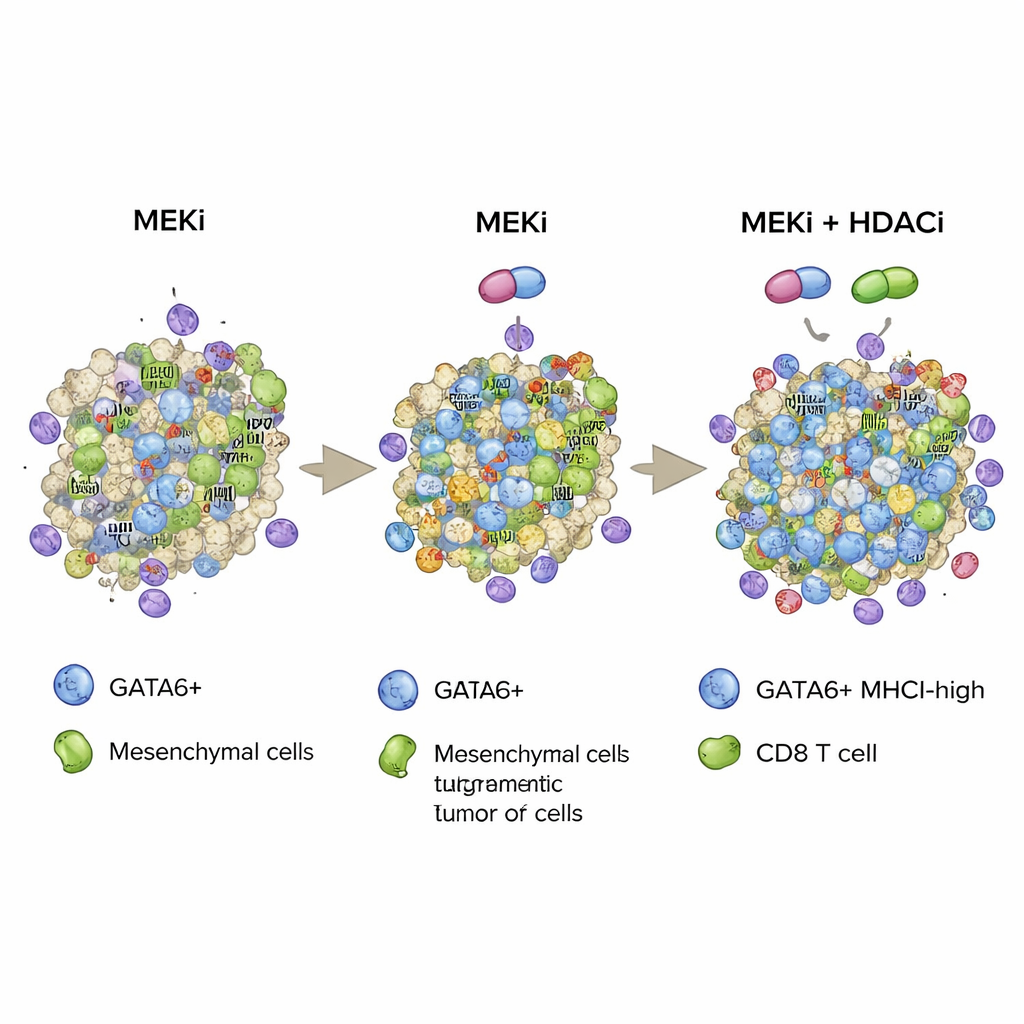
Citering: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Nyckelord: bukspottkörtelcancer, tumörimmunitet, GATA6, MEK-hämmare, HDAC-hämmare