Clear Sky Science · sv
Multikomponent synergistisk immobilisering via in situ- och dynamiska utbytesstrategier för konstruktion av hierarkiska biofarmaceutika
Varför det är viktigt att bygga smartare läkemedel
Många av dagens mest kraftfulla läkemedel är stora, ömtåliga biologiska molekyler som proteiner och enzymer. De kan bekämpa cancer, döda skadliga bakterier och påskynda läkning, men de skadas lätt och är svåra att leverera till rätt plats i kroppen. Denna artikel beskriver ett nytt sätt att ”packa” flera av dessa känsliga komponenter tillsammans inuti ett skyddande, svampliknande material, så att de kan verka i sekvens med större kraft och färre biverkningar.
Förvandla en kristall till ett molekylärt flerfamiljshus
Forskarna utgår från ett särskilt poröst material byggt av metalljoner och små organiska byggstenar. Det beter sig lite som ett pyttelitet, flexibelt flerfamiljshus fullt av rum och korridorer. De visar att denna ram, kallad ett zeolitliknande pyrimidinramverk, kan växa runt proteiner så att proteinerna slutar upp skyddade inuti kristallen. Denna ”in situ”-infångning krossar eller inaktiverar inte proteinerna, och noggranna bilder bekräftar att de är jämnt fördelade genom hela inredningen, ungefär som hyresgäster på varje våning i ett hus.
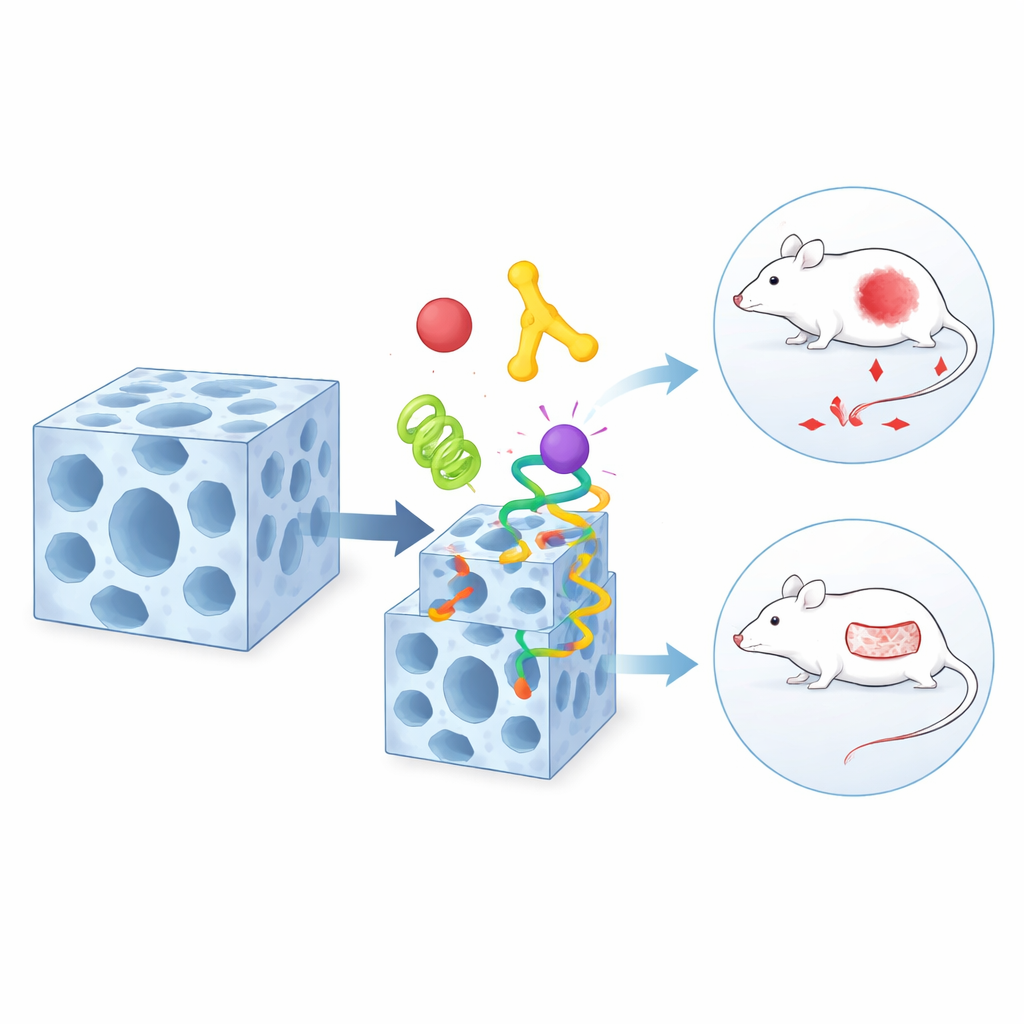
En formföränderlig värd för ytdekoration
Samma material har en överraskande andra förmåga: det kan reversibelt ändra sin inre struktur när det utsätts för vissa lösningsmedel eller vatten. Under denna skonsamma formförändring lossnar vissa kemiska bindningar i ramverket och återbildas sedan. Teamet upptäckte att särskilda kemiska grupper på proteinytor — som de som finns i vissa aminosyror — kan utnyttja detta ögonblick av svaghet. De konkurrerar tillfälligt med ramverkets ursprungliga byggstenar och glider in i nybildade ”defekter” nära ytan. Som ett resultat förankras ett lager proteiner främst på kristallens utsida, medan de inre förblir på plats. Denna dynamiska utbytesprocess låter forskarna bestämma vilka komponenter som bor djupt inuti och vilka som dekorerar det yttre skalet.
Design av enzymatiska löpande band
Med både inner- och ytutrymmen under kontroll bygger författarna små enzymatiska ”löpande band”. I ett exempel låses ett enzym som omvandlar socker till en reaktiv biprodukt inuti ramverket, medan ett andra enzym som säkert bryter ner denna biprodukt fästs nära ytan. Denna in–ut-ordning får reaktionen att gå snabbare och mer effektivt än mer traditionella kärna–skalförslag eller slumpmässiga blandningar av enzymer. Eftersom de yttre enzymerna är lättare för molekyler att nå, och den skadliga intermediären snabbt avlägsnas, förblir systemet aktivt över många cykler och tål bättre värme, hårda förhållanden och upprepad användning.
Smarta anti-cancer- och antibakteriella paket
Den verkliga styrkan i denna metod syns när den appliceras inom medicin. Teamet kombinerar ett tumörtargeterande protein, ett glukosätande enzym och ett vanligt cytostatika i en enda, lagerförd partikel. Targetkomponenten på ytan styr partikeln till cancercellerna, enzymet tömmer deras energiförråd genom att konsumera lokalt socker, och småmolekyl-läkemedlet levererar ett ytterligare dödande slag. I möss med mänskliga tumörtransplanterade vävnader krymper detta tremannapaket tumörer mycket effektivare än någon av komponenterna ensam eller enklare arrangerade blandningar. I en separat design anpassar författarna ramverket för infekterade hudsår genom att placera en antibakteriell peptid och ett vävnadsomformande enzym i olika regioner av samma bärare. I råttmodeller minskar dessa partiklar infektionen kraftigt och påskyndar slutning av svårläkta sår jämfört med konventionella behandlingar.

Hur detta arbete för medicinen framåt
För en icke-specialist är huvudbudskapet att denna studie förvandlar en enda porös kristall till ett programmerbart hem för många typer av terapeutiska molekyler. Genom att bestämma vem som bor inuti, vem som sitter på ytan och i vilken proportion kan forskarna orkestrera stegvisa behandlingar — först rikta in, sedan attackera, sedan reparera — inom ett enda litet objekt. Denna strategi skyddar inte bara ömtåliga biologiska läkemedel utan låter dem också hjälpa varandra, vilket leder till starkare, mer precisa anti-cancer- och antibakteriella terapier. Samma designprinciper skulle kunna anpassas till många framtida ”smarta läkemedel” som behöver flera komponenter att samarbeta på rätt plats vid rätt tidpunkt.
Citering: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Nyckelord: metall-organiska ramverk, enzymimmobilisering, cancernanomedicin, sårläkning, leverans av biofarmaceutika