Clear Sky Science · sv
Extracellulär matris medierar klustring av cirkulerande tumörceller vid metastasering av trippelnegativ bröstcancer
Hur avvikande bröstcancerceller går ihop i blodomloppet
När bröstcancer sprider sig beror det ofta på att lösa cancerceller tar sig ut i blodomloppet och anropar tumörer i avlägsna organ. Denna studie ställer en förvillande enkel fråga med stora konsekvenser: hur lyckas de mest aggressiva bröstcancercellerna, som förlorat sitt vanliga ”kardborreband” för att hålla ihop, ändå resa som tajta kluster — och varför gör det dem så dödliga?
En klibbig sockerhinna som ersätter klassiskt cellklister
Författarna fokuserar på trippelnegativ bröstcancer (TNBC), en särskilt aggressiv form som ofta släpper ut cirkulerande tumörceller (CTC) i blodet. I många cancerformer är CTC-kluster mycket mer benägna att bilda metastaser än enskilda celler. Vanligtvis hålls sådana kluster samman av epiteliala adherensföreningar — speciella proteinkomplex som fungerar som molekylära nit mellan närliggande celler. Men TNBC-celler förlorar ofta dessa föreningsproteiner, vilket skapar ett paradoxalt problem: utan det vanliga klistret, vad håller deras kluster intakta? Genom att gräva i stora cancerngendatabaser fann forskarna att TNBC-tumörer är berikade för gener som är involverade i cellens yttre ställning, den så kallade extracellulära matrisen. En framstående gen, HAS2, kodar för ett enzym som producerar hyaluronan (HA), en lång, sockrig polymer som täcker celler. Höga nivåer av HAS2 och HA var starkt kopplade till aggressiva, metastatiska tumördrag.
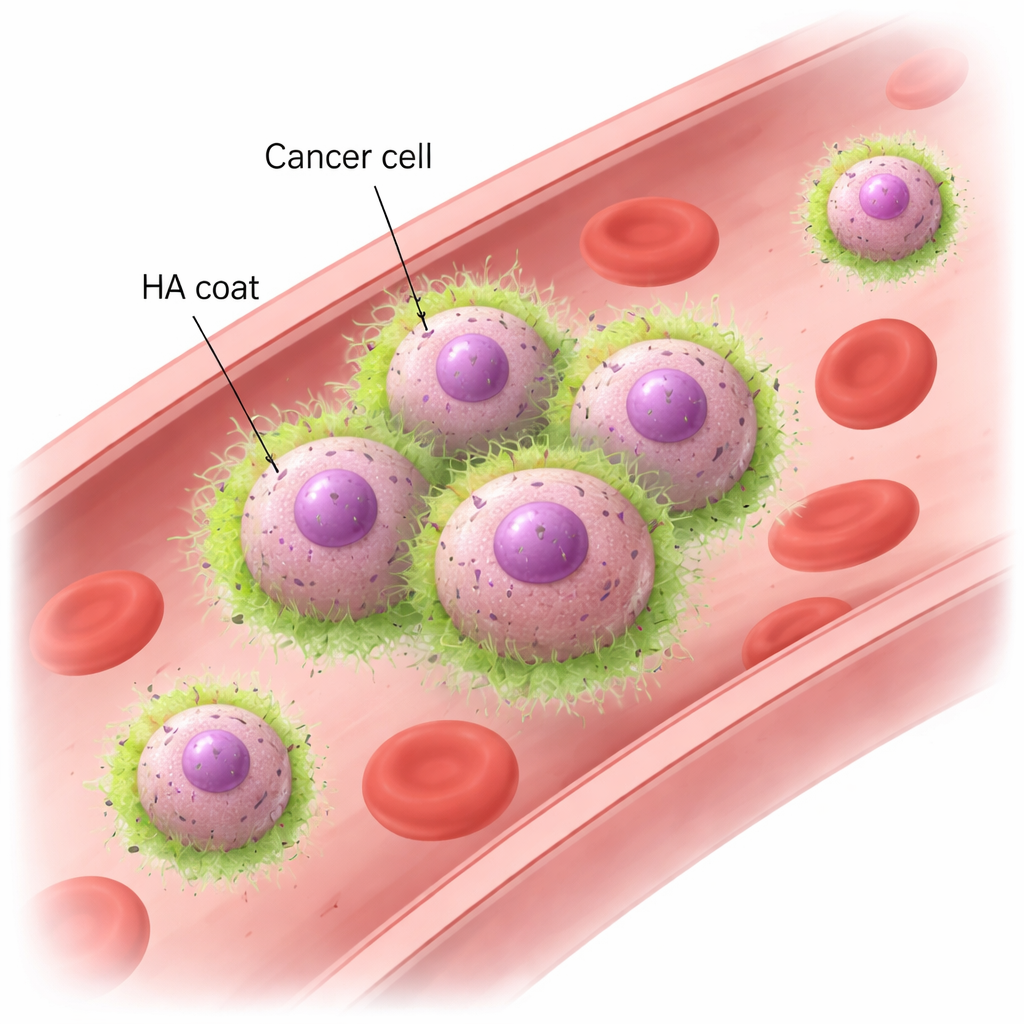
Hyaluronan och CD44: ett nytt sätt för celler att hålla händer
Med musmodeller och mänskliga bröstcancercellinjer visade teamet att metastatiska TNBC-celler snabbt bildar kluster när de utsätts för virvlande vätska som efterliknar blodflödet. Dessa kluster förblir intakta även under krafter liknande dem i riktiga blodkärl, medan mindre aggressiva bröstcancerceller faller isär och driver iväg som enskilda celler. Mikroskopi avslöjade att de metastatiska cellerna är inbäddade i en HA-"hätta" som koncentreras just där celler rör vid varandra. Att ta bort HA med enzymer eller att sänka HAS2 gjorde att cellerna förlorade sin förmåga att klustra under flöde, även om de fortfarande kunde sedimentera ihop när de fick ligga ostörda. Den viktiga partnern på cellsidan är CD44, en vanlig ytreceptor som binder HA. Celler utan CD44 kunde inte längre behålla HA på sin yta eller bilda kluster. Omvänt fick icke-klustrande celler som konstruerades för att producera både HAS2 och CD44 en robust förmåga att klustra. Dessa experiment visade att HA som interagerar med CD44 är både nödvändigt och tillräckligt för att få cancerceller att hålla ihop i snabbt rörligt blod.
Små utskott och mekaniska lås bygger starka kluster
Högupplösande avbildning kartlade den fysiska koreografin för hur kluster bildas. Enskilda TNBC-celler skjuter ut många tunna, aktinbaserade membranutskott — som känseltrådar — besatta med CD44 och spetsade med HA. När två celler driver nära varandra möts dessa känseltrådar först och bildar initiala HA–CD44-bryggor. Med tiden glider utskotten längs varandra, drar hela cellkropparna närmare tills breda områden av membranen ligger nästan sida vid sida. Denna process liknar hur normala epitelceller bygger adherensföreningar, men här drivs den av en flexibel sockerhinna istället för styva proteinkedjor. När kontaktzonen mognar går en annan uppsättning strukturer in: desmosomer, robusta föreningar som länkar cellmembran till det inre skelettet. Desmosomala proteiner ansamlas först efter att HA-baserad kontakt etablerats och fungerar som mekaniska ”lås” som hjälper klustren att stå emot de rivande krafter som blodflödet ger. När desmosomkomponenter reducerades bildades kluster men gick sönder vid högre skjuvspänning.
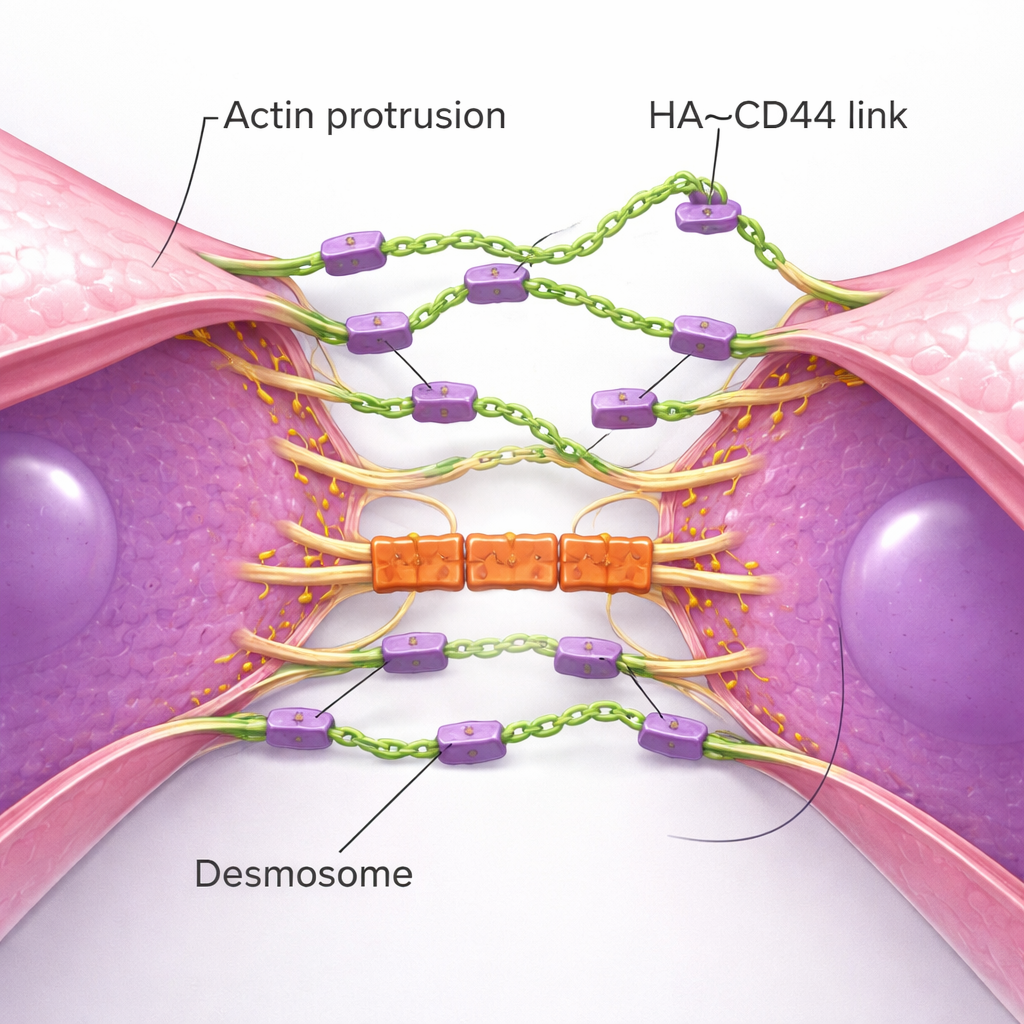
Varför klustring betyder något för överlevnad och metastasering
Det HA-baserade klustringssystemet visade sig vara mer än ett sätt att hålla ihop; det ökade direkt överlevnaden. Under långvarigt simulerat blodflöde uppvisade HA-rika kluster mycket lägre nivåer av skadliga reaktiva syreföreningar och avsevärt mindre celldöd än HA-borttagna enskilda celler. I musmodeller producerade TNBC-celler utan HAS2 betydligt färre CTC, bildade endast små kluster och gav dramatiskt färre lungmetastaser — trots att deras primärtumörer växte lika bra. När färdigbildade kluster av kontroll- och HAS2-defekta celler injicerades i möss var de HA-fattiga cellerna mycket mindre benägna att framgångsrikt kolonisera lungorna. Dessutom kunde HA-täckta CTC ”rekrytera” andra celler — både cancerceller utan HA och normala immunceller som neutrofiler — in i blandade kluster, förutsatt att dessa partners uttryckte CD44. Patientblodprover från kvinnor med metastaserande TNBC visade samma mönster: CTC bar ofta en HA-hinna, med HA berikat vid kontaktpunkter mellan tumörceller och mellan tumör- och icke-tumörceller.
Vad detta betyder för patienter och framtida terapier
För en icke-specialist är huvudpoängen att några av de dödligaste bröstcancercellerna inte reser ensamma utan som små, samarbetande team hållna ihop av en sockrig yttre hinna och dess receptor, snarare än av de klassiska cell–cell-"nitarna" som finns i normala vävnader. Denna HA–CD44-baserade mekanism hjälper tumörceller att överleva det hårda blodflödet, slå sig samman med varandra och med stödjande blodceller, och mer effektivt anlägga nya tumörer i avlägsna organ. Att rikta in sig på HA-produktion (till exempel genom att hämma HAS2) eller blockera dess interaktion med CD44 skulle i princip kunna försvaga dessa kluster och göra det svårare för TNBC att metastasera, vilket erbjuder en ny angreppspunkt för framtida anti-metastatiska behandlingar.
Citering: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Nyckelord: trippelnegativ bröstcancer, cirkulerande tumörceller, hyaluronan, CD44, metastas