Clear Sky Science · sv
Escherichia coli främjar metastasering av kolorektal cancer genom att upprätthålla enhancer–promotor-loopar genom frisättning av neutrofila extracellulära nät
Tarmbakterier och cancerns hemliga motorväg
Kolorektal cancer är ofta dödlig inte på grund av den ursprungliga tumören i tarmen, utan eftersom cancerceller sprider sig till levern och etablerar sig där. Denna studie avslöjar en oväntad medhjälpare i den resan: en vanlig tarmbakterie, Escherichia coli. Genom att följa händelsekedjan från bakterier i tarmen till aggressiva tumörer i levern visar forskarna hur mikrober, immunceller och DNA-arkitekturen inne i cancerceller kan samverka för att driva metastasering — och pekar på nya sätt att bryta denna kedja.
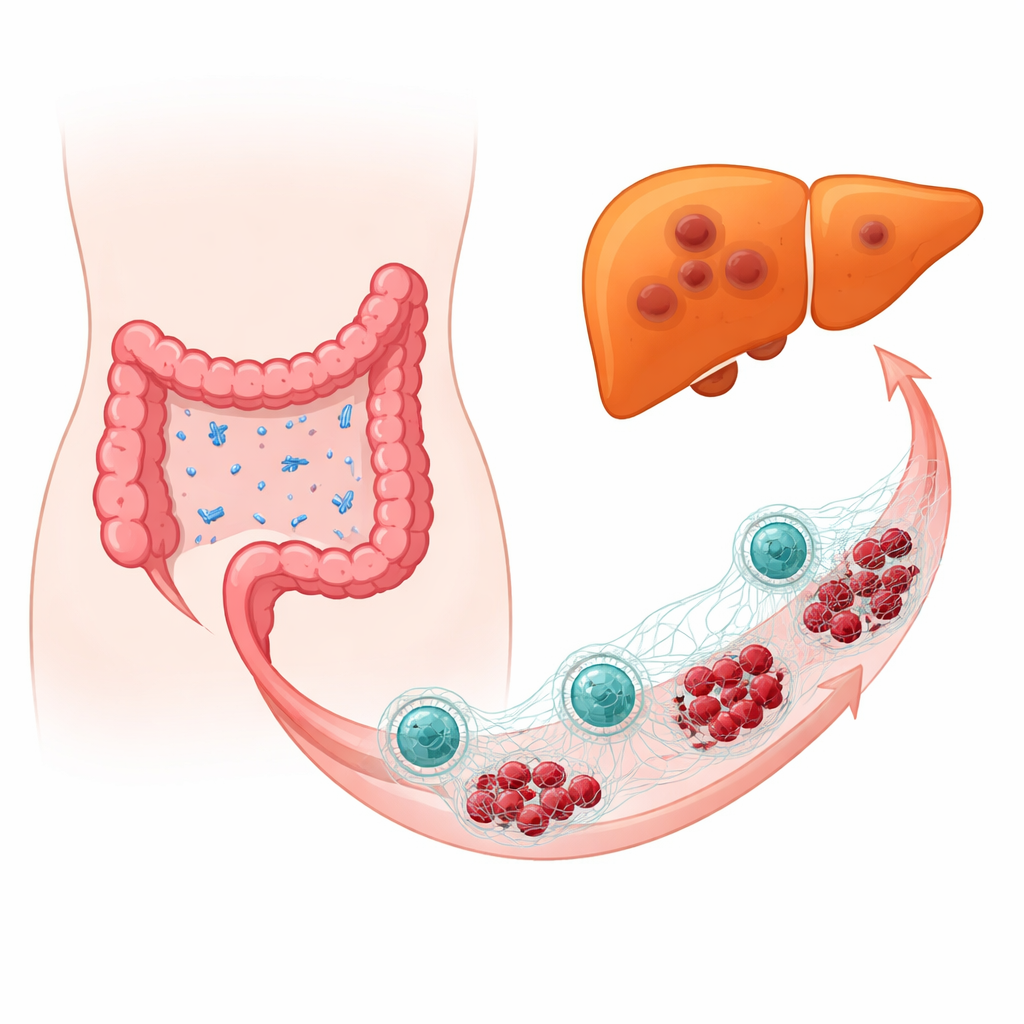
När vänliga bakterier blir fientliga
Gruppen undersökte tumörprover från personer med kolorektal cancer och jämförde dem som fått metastaser i levern med dem som inte hade det. Med högupplöst DNA-baserad mikrobiell profilering fann de att E. coli var mycket mer utbredd i de tumörer som redan hade etablerat levermetastaser. I musmodeller och i möss med humaniserat immunsystem gjorde avsiktlig tillsats av E. coli i närheten av kolorektala tumörer att levermetastaser blev större och vanligare, och drev tumörceller mot ett mer rörligt, invasivt tillstånd. Även när större delen av den normala tarmfloran avlägsnades med antibiotika och endast E. coli återintroducerades, ökade bakterien fortfarande tumörtillväxt och spridning, vilket pekar på att E. coli i sig snarare än en allmän störning av mikrobiomet var ansvarig.
Immuna nät som hjälper cancer att undkomma
Neutrofiler — immunceller i främsta linjen som normalt fångar och dödar mikrober — framträdde som avgörande mellanled. Som svar på E. coli frigjorde neutrofiler trådliknande strukturer kallade extracellulära nät, bestående av DNA och toxiska proteiner. Dessa nät är tänkta att fånga bakterier, men i detta sammanhang skyddade och stärkte de ofrivilligt cancercellerna. När forskarna bröt ner näten med enzymer eller blockerade nyckelenzym som behövs för att bilda dem, krympte levermetastaserna och tumörerna blev mindre aggressiva. Att tömma neutrofiler gav en liknande skyddande effekt, vilket pekar på en paradox: samma immunsvar som bekämpar infektioner kapades för att hjälpa cancer sprida sig.
Från elektriska signaler till genbrytare
Hur kunde klibbiga DNA-nät utanför en tumörcell påverka vad som händer djupt inne i dess kärna? Svaret låg i kalcium, en enkel jon som fungerar som en elektrisk signal i celler. Studien visade att neutrofila nät ökade nivån av en kanalprotein, TRPC1, på kolorektala cancerceller. TRPC1 tillät extra kalcium att strömma in i cellen, vilket i sin tur aktiverade en kalciumkänslig regulator kallad NFATC3 och skapade en självförstärkande cykel som höll TRPC1-nivåerna höga. Denna kalciumvåg uppmuntrade två små proteiner, S100A8 och S100A9, att haka ihop och därefter binda till ett stort tillväxtreglerande protein, STAT3. Tredjeparet rörde sig in i kärnan där de gjorde något särskilt slående: de bidrog till att böja och loopa DNA så att avlägsna regulatoriska regioner och geners startplatser kom i kontakt, vilket fysiskt stabiliserade "enhancer–promotor-loopar" som ökar aktiviteten hos vissa gener.
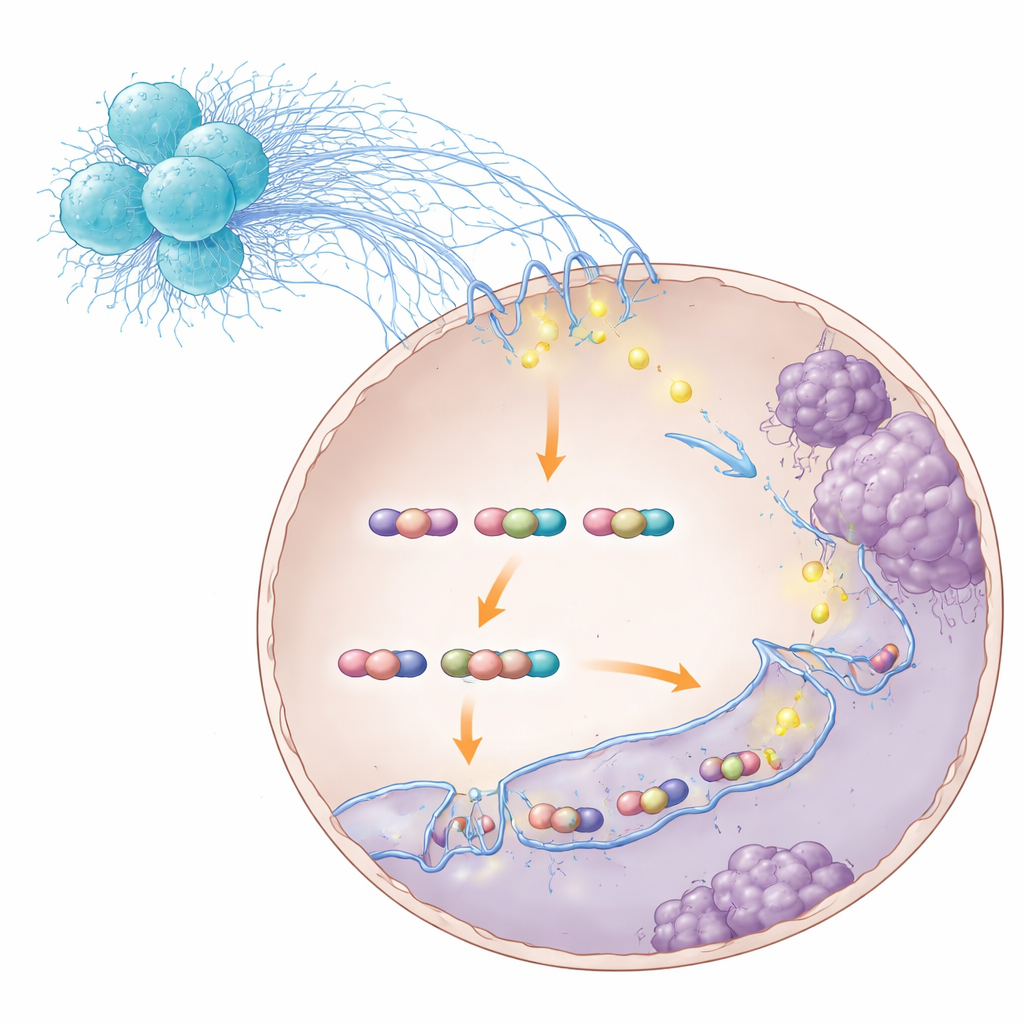
Omkoppling av cancerceller för metastasering
Genom att kartlägga de tredimensionella kontakterna längs genomet fann forskarna att STAT3–S100A8/9-komplexet främjade loopar som gynnade gener involverade i cellrörelse och invasion. En framträdande gen var TNS1, som driver celler att lossa sina fästen och migrera lättare. När STAT3–S100A8/9-komplexet stördes försvagades eller försvann många av dessa loopar, TNS1-nivåerna sjönk och cancercellerna förlorade en del av sin förmåga att invadera och etablera sig i levern. Viktigt är att denna störning inte hindrade STAT3 från att binda DNA helt — den destabiliserade specifikt den loopande arkitekturen som överladdade metastatiska program. I djurmodeller minskade blockering av olika steg i denna kedja — från bakteriesensorer som RIPK2 i neutrofiler, till S100A8/9, till STAT3 självt — levermetastasering och förbättrade överlevnaden.
Att bryta kedjan mellan bakterier och tumörer
För icke-specialister är kärnbudskapet att en vanlig tarmbakterie kan hjälpa kolorektal cancer att sprida sig genom att först provocera immunceller att kasta DNA-nät, och sedan använda dessa nät för att driva ett kalciumdrivet relä som omskriver hur cancergener sätts på. Istället för att förlita sig på bredspektrumantibiotika, som kan skada gynnsamma mikrober och dämpa cancerimmunterapi, pekar arbetet på mer precisa läkemedelsmål: bakteriesensorer som RIPK2, TRPC1–kalcium–S100A8/9-kaskaden och de STAT3-drivna DNA-looparna som låser metastasrelaterade gener i ett högaktiverat läge. Att avbryta denna kedja vid en eller flera punkter kan erbjuda en ny strategi för att hindra kolorektal cancer från att förvandla ett lokaliserat problem i tarmen till en dödlig sjukdom i levern.
Citering: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Nyckelord: metastasering av kolorektal cancer, tarmmikrobiom, neutrofila extracellulära nät, STAT3-signalering, epigenetisk genreglering