Clear Sky Science · sv
Kovalent hämmardesign ger aktivitet mot både GDP- och GTP-bundna former av KRAS G12C
Varför detta är viktigt för framtida cancerbehandlingar
Cancer som drivs av mutationer i genen KRAS har länge betraktats som några av de svåraste att behandla. Nyligen har nya läkemedel som slår ut en vanlig muterad form, KRAS G12C, nått patienter och börjat förändra den bilden. Denna artikel undersöker en ännu mer ambitiös idé: kan vi utforma läkemedel som blockerar KRAS G12C i båda dess huvudlägen i cellen, och skulle det göra cancerbehandling snabbare, starkare eller mer hållbar?
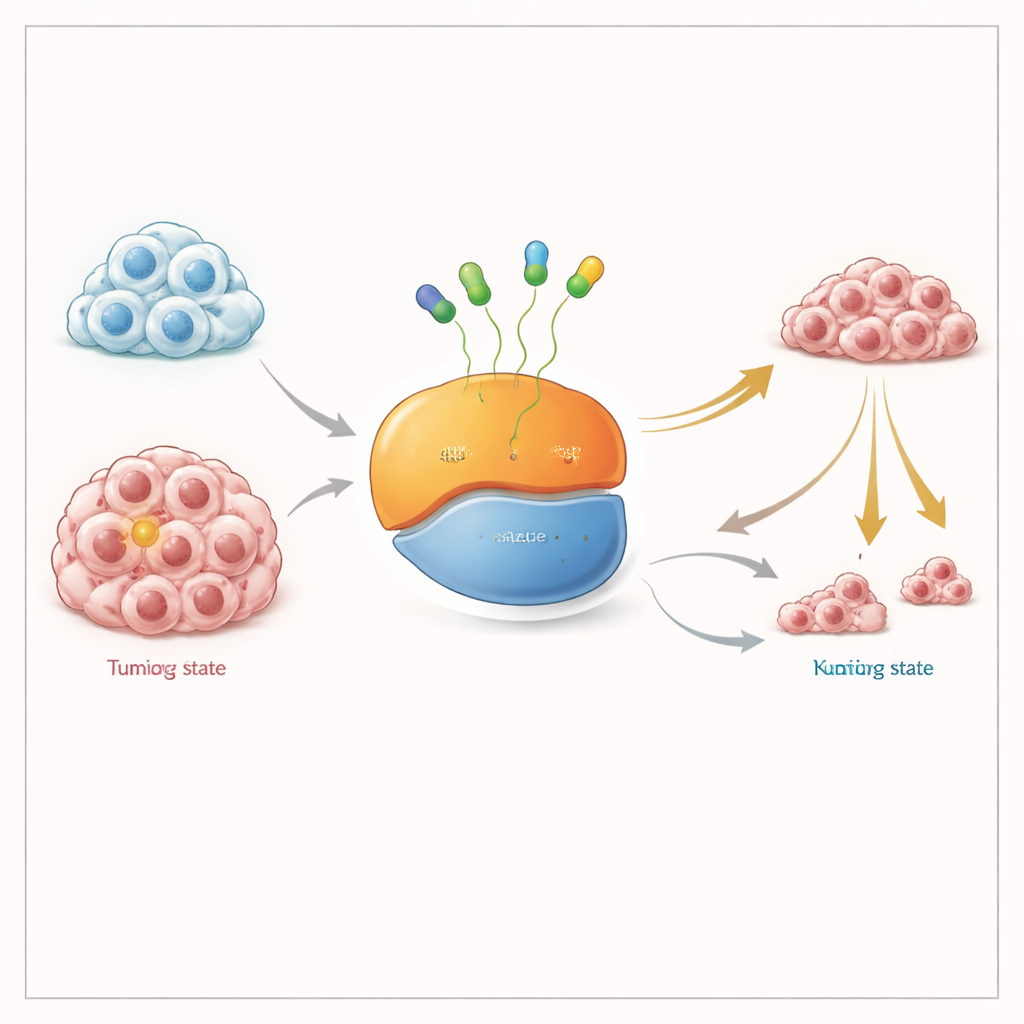
Att stänga av en molekylär strömbrytare i två positioner
KRAS fungerar som en liten av/på‑strömbrytare för signaler som styr celltillväxt. Den växlar mellan ett "av"‑tillstånd, där den håller en typ av energibärande molekyl (GDP), och ett "på"‑tillstånd, där den håller en annan (GTP). KRAS G12C‑mutationen fastställer denna brytare delvis i påläge och driver tumörtillväxt. Befintliga läkemedel som godkänts av FDA hakar fast vid det inaktiva formen och låser det, och med tiden, när mer KRAS passerar genom det tillståndet, blir den totala mängden muterat protein inaktiverat. Många forskare har hävdat att ett läkemedel som kan fånga KRAS i både dess på- och av‑former borde fungera bättre, särskilt i tumörer som anpassar sig genom att hålla mer KRAS i det aktiva läget.
Att designa en ny typ av molekylär krok
Författarna satte ut för att konstruera sådana dubbeländamålsläkemedel. De fokuserade på en liten fåra nära en flexibel region av KRAS kallad Switch II, där nuvarande läkemedel redan binder. Istället för att ändra hur tätt deras molekyler satt i den fåra, omkonstruerade de "krigshuvudet" som bildar en permanent kemisk bindning till den muterade cysteinen på position 12. Genom datormodellering och syntes av flera dussin varianter upptäckte de ett särskilt tre‑delat krigshuvud som närmar sig cysteinen från en något annan vinkel. Denna subtila förskjutning skapar tillräckligt med utrymme för den bulkigare GTP‑molekylen, vilket gör att de nya föreningarna kan binda till KRAS oavsett om den bär GDP eller GTP. Biokemiska tester bekräftade att ledande föreningar kunde störa KRAS:s samspel med en viktig signalpartner, RAF, i båda lägena.
Att se hur proteinet omformas
För att förstå varför dessa molekyler fungerade bestämde teamet högupplösta kristallstrukturer av läkemedlet bundet till KRAS. Dessa snapshots visade att det nya krigshuvudet reagerar vid en ovanlig plats på den kemiska stommen, bryter av en fluoratomen och bildar en kovalent bindning vid en annan kolatom än vad typiska cancerläkemedel som riktar sig mot cysteiner gör. Denna förändrade kemi hjälper läkemedlet att passa in i Switch II‑fickan även när GTP är närvarande. Strukturerna avslöjade också att när hämmaren binder, knuffar den på en liten vattenmolekyl och omarrangerar subtilt en annan loop, Switch I, som normalt kontaktar nedströms signalproteiner. Denna allosteriska omformning drar två aminosyror tillsammans för att bilda en stark saltbrygga, vilket förvränger ytan så att RAF inte längre kan docka och föra vidare tillväxtsignaler.
Snabb avstängning, men ingen starkare långtidsverkan
Med dessa strukturella insikter finslipade forskarna två ledande molekyler som effektivt och selektivt hakar fast vid KRAS G12C, samtidigt som de i stor utsträckning skonar andra proteiner med cysteiner. I cancercellinjer blockerade dessa dubbelståndshämmare snabbt en nyckel‑signalväg känd som MAPK‑banan, mätt som förlust av en kemisk markör på ERK‑proteinet och stark undertryckning av celltillväxt. De inaktiverade KRAS i celler snabbare än ett referensläkemedel som bara riktar sig mot det inaktiva tillståndet. I musmodeller för tumörer visade en ledande förening god oral biotillgänglighet, bildade snabbt kovalenta bindningar till målet och krympte tumörer eller bromsade deras tillväxt. När teamet dock jämförde dubbelstånds‑ och inaktiva‑tillstånds‑läkemedel över längre tid uppnådde båda klasserna så småningom liknande nivåer av KRAS‑avstängning, banhämning och tumörkontroll.
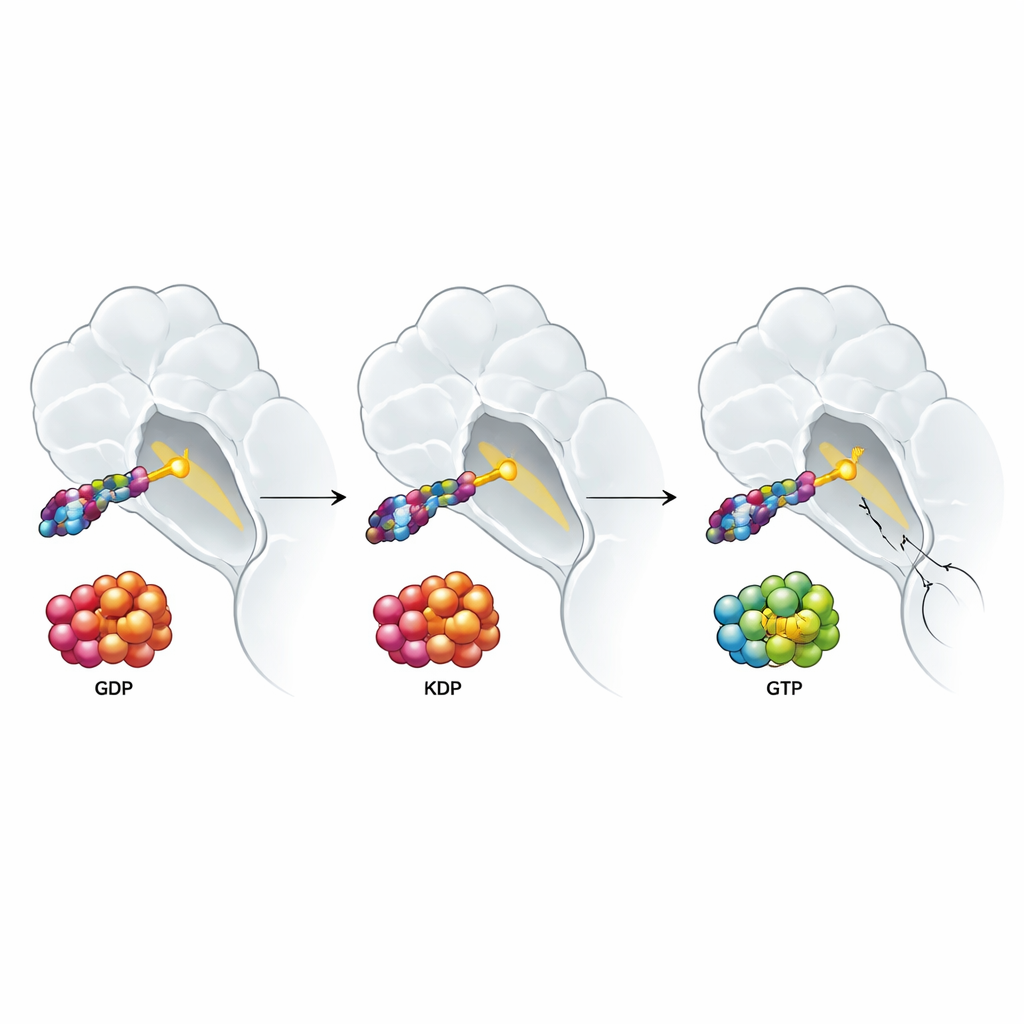
Varför tillväxtsignaler från tumörens omgivning fortfarande segrar
Studien undersökte också hur signaler från tumörens omgivning påverkar dessa läkemedel. Tillväxtfaktorer som EGF och HGF, som är rikliga kring många tumörer, skjuter RAS‑proteiner mot det aktiva GTP‑fyllda tillståndet och är kända för att försvaga svaren på riktade terapier. Man skulle kunna förvänta sig att ett läkemedel som binder den aktiva formen av KRAS G12C skulle kringgå detta problem. Istället fann författarna att både dubbelstånds‑ och inaktiva‑tillstånds‑hämmare tappade potens när sådana tillväxtfaktorer var närvarande. Detaljerade experiment pekade ut en överraskande bov: aktivering av de normala, icke‑muterade formerna av RAS (H‑RAS och N‑RAS), som kan kringgå KRAS G12C och hålla tillväxtsignalerna igång. När forskarna raderade H‑RAS och N‑RAS i en lungcancercellinje försvann i stor utsträckning tillväxtfaktor‑driven resistens för alla typer av KRAS G12C‑riktade läkemedel, medan ett läkemedel som blockerar ett nedströms steg i banan i första hand påverkades mindre.
Vad detta betyder för patienter och läkemedelsutveckling
Sammanfattningsvis visar arbetet att det är kemiskt och strukturellt möjligt att bygga kovalenta KRAS G12C‑läkemedel som fångar proteinet i både dess på‑ och av‑stater, och att dessa dubbelståndshämmare kan stänga av signaleringen snabbare än befintliga läkemedel. Den snabba inbindningen översattes dock inte till entydigt bättre tumörkontroll eller en lösning på tillväxtfaktor‑driven resistens i prekliniska modeller. För patienter antyder detta att det inte räcker med att enbart lägga till aktivitet mot den aktiva KRAS‑formen; kombinationsstrategier som även tar itu med andra RAS‑familjemedlemmar eller nedströms signalnoder kan behövas. Det nya krigshuvudet och den strukturella ritning som presenteras här utvidgar dock verktygslådan för att rikta in sig på KRAS och kommer att informera framtida generationer av precisionscancerterapier.
Citering: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Nyckelord: KRAS G12C, kovalent hämmare, dubbelståndshämning, MAPK‑signalering, läkemedelsresistens