Clear Sky Science · sv
En molekylärt definierad basalo‑prefronto‑thalamisk krets reglerar sensoriska och affektiva dimensioner av smärta hos hanmöss
Varför denna hjärnkrets är viktig för smärta
Smärta är mer än ett skarpt stick eller en dov värk; den har också en emotionell tyngd och kan förändra vårt humör och beteende under år. Många patienter med kronisk smärta får liten lindring av dagens läkemedel och riskerar ofta allvarliga biverkningar. Denna studie i hanmöss avslöjar en precist definierad hjärnkrets som hjälper hjärnan att skruva upp eller ner smärta, både vad gäller hur intensiv den känns och hur plågsam den är. Genom att kartlägga och styra denna bana pekar arbetet mot nya, mer riktade sätt att lindra kronisk smärta utan att enbart förlita sig på traditionella smärtstillande medel.
En dold motorväg från tänkande hjärna till smärtknutpunkt
Forskarna koncentrerade sig på den mediala prefrontala cortex, en framre hjärnregion som är involverad i beslutsfattande, känslor och smärtkontroll, och på thalamus, ett djupt reläcenter som formar både smärtans intensitet och obehag. De upptäckte att en specifik cellgrupp i mediala prefrontala cortex, markerad av genen Foxp2, bildar en huvudutgående bana till thalamus. Dessa celler sitter främst i det djupaste kortikala lagret och skickar långa fibrer till särskilda thalamiska kärnor, samtidigt som de i stort sett ignorerar andra typiska mål för prefrontala cortex. Med spårningsmetoder och helhjärnskartläggning visade teamet att dessa Foxp2‑markerade neuroner har starka förbindelser till tre thalamiska regioner kända för att påverka smärtbehandling: parataenialkärnan, mediodorsala thalamus och ventromediala thalamus. 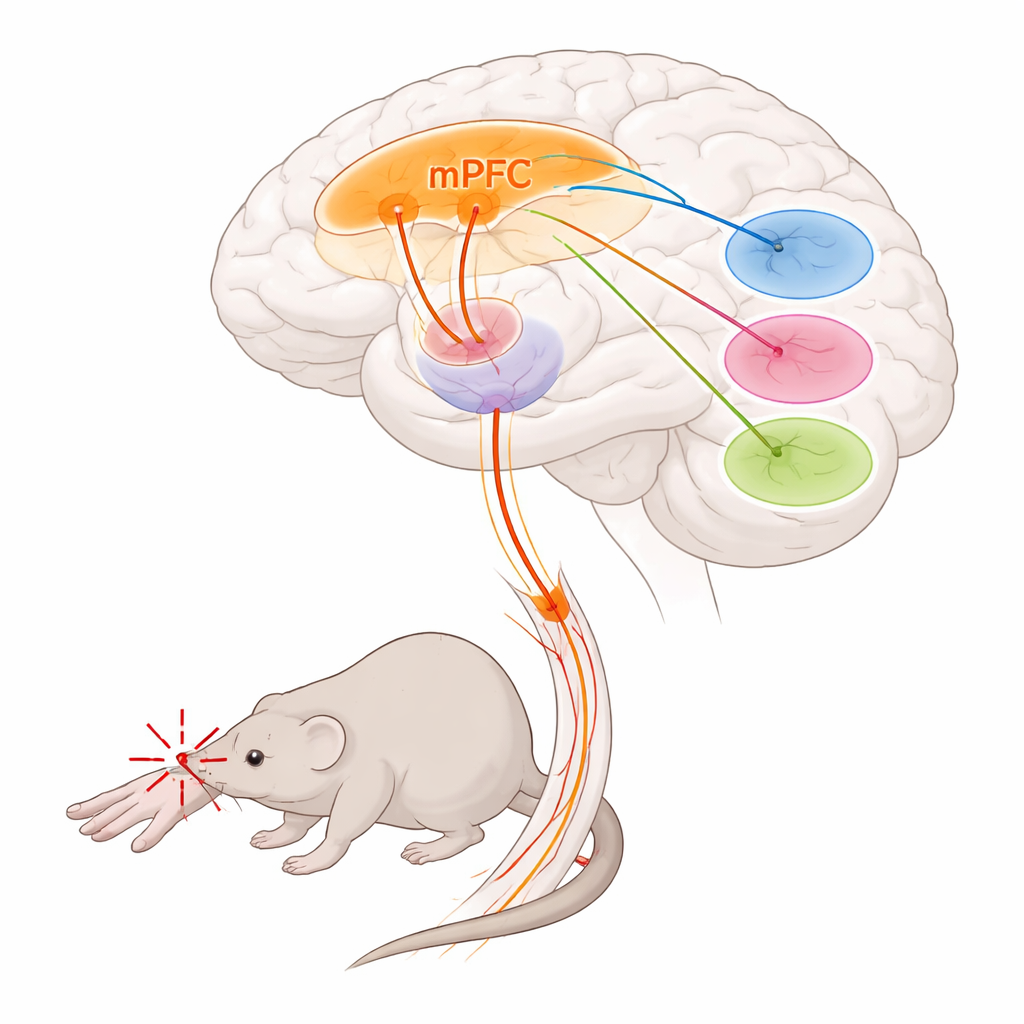
När smärtan träffar – ett nyckelkontrollcenter tystnar
För att se hur denna bana beter sig under smärta implanterade forskarna små linser ovanför mediala prefrontala cortex och registrerade aktiviteten hos individuella Foxp2‑markerade neuroner i vakna möss. Vid korta mekaniska nyp, kemisk smärta inducerad med formalin och långvarig inflammatorisk smärta tystnade dessa celler konsekvent: de flesta visade färre aktivitetsutbrott under smärtfyllda episoder och under dagarna efter inflammatorisk skada. Denna nedstängning var inte subtil; under vissa förhållanden blev mer än en tredjedel till nästan hälften av cellerna markant mindre aktiva. Resultatet tyder på att akuta och kroniska smärttillstånd delvis kan spegla tystandet av ett naturligt prefrontalt bromssystem som annars skulle hjälpa till att hålla smärtan i schack.
Att slå på och av kretsen formar smärtupplevelsen
Teamet undrade sedan om denna tystnad bara var en bieffekt av smärta eller en drivkraft bakom den. Med genetiska verktyg blockerade de antingen utflödet från Foxp2‑markerade neuroner under lång tid eller förstärkte deras aktivitet tillfälligt. Ihållande inaktivering gjorde möss mer känsliga för beröring och värme, vilket visar att denna bana normalt dämpar inkommande smärtsignaler. I kontrast höjde kortvarig aktivering tröskeln för smärtsamma stimuli, minskade sen‑fasens slickande i formalintestet (en mått på pågående, inflammatorisk smärta) och fick mössen att föredra miljöer där kretsen hade aktiverats, vilket signalerar lindring av smärtans emotionella börda. Genom att belysa specifika grenar av banan visade forskarna att projektioner till parataenial thalamus minskar både fysisk känslighet och coping‑beteenden, medan projektioner till mediodorsal och ventromedial thalamus främst finjusterar de emotionella och beteendemässiga dimensionerna. Tillsammans avslöjar resultaten ett noggrant uppdelat kopplingsschema där olika grenar av samma prefrontala population kontrollerar olika aspekter av smärtupplevelsen.
Kemisk finjustering: en kolinerg förstärkning för smärtlindring
Vad styr dessa prefrontala smärtlindrande neuroner? Spårningsexperiment visade starkt inflöde från ett kolinergt område i basala framhjärnan kallat den horisontella diagonala bandet. Många av cellerna som skickar signaler från detta område till Foxp2‑markerade neuroner använder acetylkolin, en budbärare involverad i uppmärksamhet och vakenhet. Aktivering av denna kolinerga projektion minskade mekanisk känslighet och coping‑beteenden och lindrade inflammatorisk överkänslighet, även om den inte tydligt ändrade smärtans negativa emotionella ton. På mottagarsidan visade sig Foxp2‑markerade neuroner vara berikade för en särskild typ av acetylkolinreceptor, känd som α4β2‑nikotinerga receptorn. Direkt administrering av en selektiv α4β2‑agonist i mediala prefrontala cortex gjorde möss mindre känsliga för smärtsam värme och beröring, även i kroniska inflammatoriska tillstånd, och ökade aktiviteten i Foxp2‑markerade neuroner. Blockering av dessa neuroner avlägsnade läkemedlets nytta, vilket visar att denna receptor lindrar smärta specifikt genom att excitera denna celltyp. 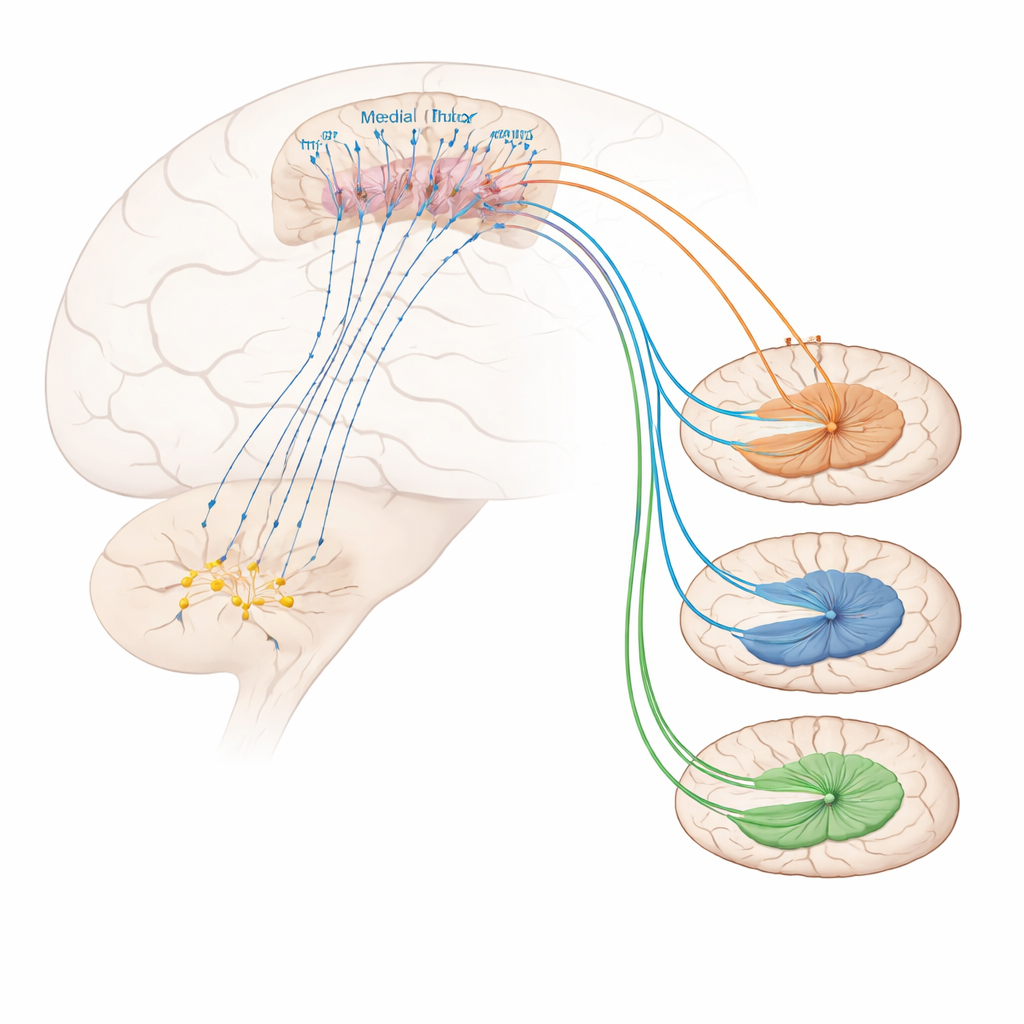
Vad detta betyder för framtida smärtbehandling
I vardagliga termer identifierar studien en precis trestegs‑bana: ett kolinergt ”start”‑område i basala framhjärnan, en specialiserad uppsättning kontrollceller i mediala prefrontala cortex och distinkta reläkärnor i thalamus som separat styr hur starkt smärtan känns, hur dåligt den upplevs känslomässigt och hur vi reagerar på den. Smärta verkar dämpa denna krets; att återaktivera den, antingen genom direkt stimulering eller genom att rikta in sig på dess acetylkolinreceptorer, minskar både sticket och lidandet vid inflammatorisk smärta hos hanmöss. Även om mycket återstår för att översätta dessa fynd till människor och till andra former av kronisk smärta, framhäver resultaten en lovande strategi: istället för att bedöva all känsel skulle framtida behandlingar kunna återställa eller finjustera hjärnans egna smärtlindringskretsar för mer effektiv och möjligen säkrare långtidsterapi.
Citering: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Nyckelord: kronisk smärta, mediala prefrontala cortex, thalamus, kolinerg signalering, nikotinerga receptorer