Clear Sky Science · sv
Kovalent modifiering av en glutaminsyra inspirerad av HaloTag-teknik
Göra proteiners ”ankare” till läkemedelsmål
Många moderna cancerläkemedel verkar genom att fästa vid proteiner inne i våra celler. Men några av de viktigaste proteinerna saknar enkla ”handtag” för läkemedel att greppa. Denna studie introducerar ett skickligt kemiskt knep, inspirerat av ett populärt laboratorieverktyg kallat HaloTag, för att fästa vid en normalt svåråtkomlig plats på ett protein som hjälper till att styra tillväxtsignaler relevanta för cancer. Arbetet kan öppna nya vägar för läkemedel som mer varaktigt slår av tumördrivande signalvägar.
Varför de flesta kovalenta läkemedel siktar på samma plats
Under senare år har så kallade riktade kovalenta läkemedel blivit en spännande läkemedelsklass. De bär en måttligt reaktiv kemisk grupp som bildar en permanent bindning till en specifik aminosyra på ett protein och låser läkemedlet på plats. Nästan alla dessa läkemedel riktar sig mot cystein, en relativt sällsynt men mycket reaktiv aminosyra. Tvärtemot detta är två andra aminosyror, aspartat och glutamat, mycket vanligare och ofta avgörande för ett proteins form och funktion, men deras sura karboxylatgrupper är mycket mindre reaktiva i cellens vattniga miljö. Det gör dem svåra att modifiera selektivt, och före detta arbete fanns endast ett fåtal framgångsrika exempel på kovalenta läkemedel som riktar sig mot glutamat eller aspartat.
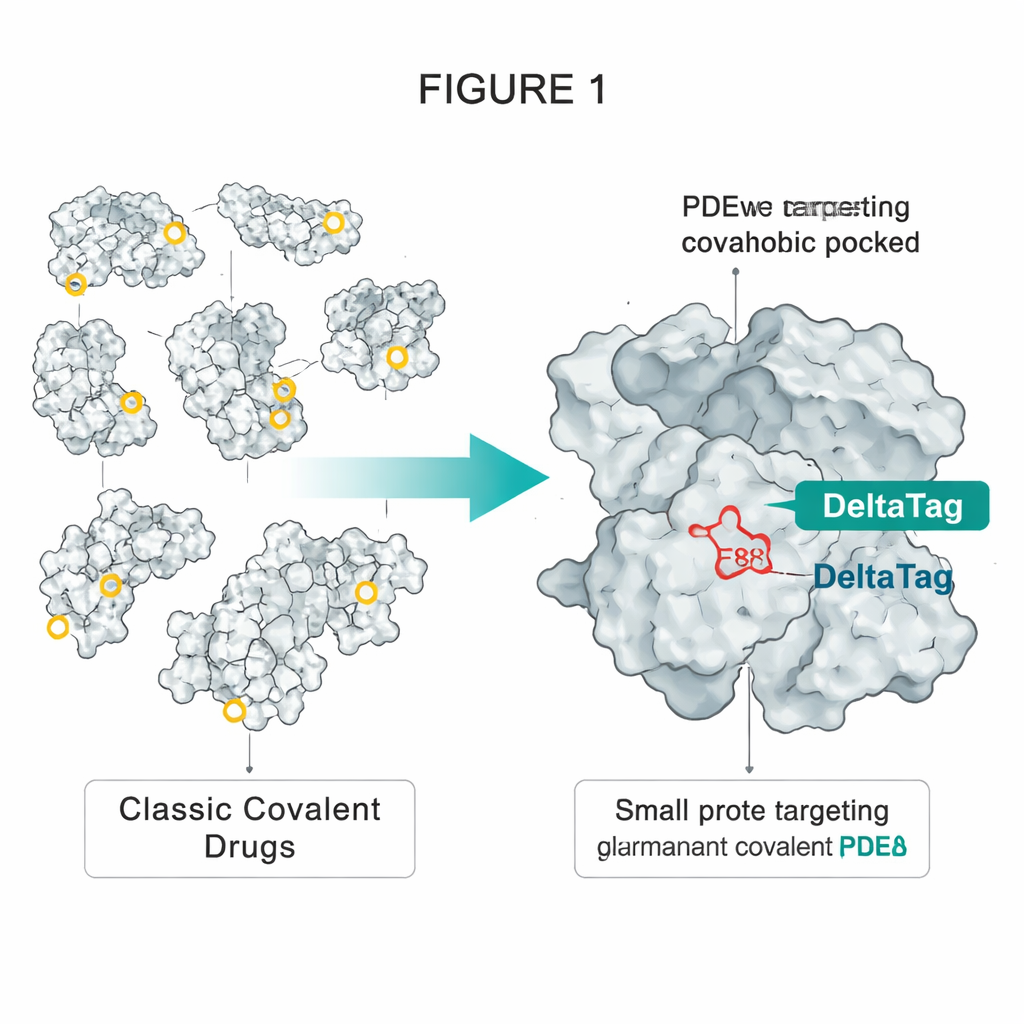
Låna ett trick från HaloTag‑tekniken
Författarna hämtade inspiration från HaloTag, ett i laboratorier brett använt konstruerat protein som kan märkas permanent med fluorescerande färgämnen. I HaloTag reagerar en särskilt placerad aspartat djupt inne i ett fettliknande ficka med en enkel kloroalkan‑kedja på färgämnet och bildar en stabil esterbindning. Forskarna noterade att ett annat protein, PDEδ, har ett något liknande hydrofobt ficka som innehåller en enda åtkomlig glutamat, kallad E88. PDEδ transporterar lipidmodifierade signalproteiner såsom den lilla GTPasen Rheb genom cellen och hjälper dem nå membraner där tillväxtfrämjande komplex som mTORC1 aktiveras. Tidigare icke‑kovalenta hämmare av PDEδ kunde blockera denna transport, men deras effekt var begränsad eftersom ett annat protein, Arl2, med tiden kan vrida ut dem ur fickan.
Designa DeltaTag för att låsa fast vid glutamat
För att övervinna detta ”utkastnings”problem började forskarna med en känd högaffinitetsblockerare av PDEδ och omkonstruerade en av dess sidokedjor så att den bar ett haloalkan‑”vapen” liknande dem som används i HaloTag‑ligander. Genom flera omgångar av strukturell finjustering, vägledd av proteinets kristallstrukturer, kom de fram till en förening kallad DeltaTag. Dess nyckelfunktion är en fenetylbromidgrupp placerad så att, när molekylen lägger sig i PDEδ:s lipidficka, är bromiden exakt inriktad för att reagera med E88. Biofysiska mätningar och högupplösta röntgenstrukturer bekräftade att DeltaTag bildar en kovalent esterbindning specifikt med denna glutamat och att andra potentiellt mer reaktiva aminosyror på PDEδ förblir orörda. Föreningen är tillräckligt reaktiv för att märka proteinet effektivt, men tillräckligt stabil i vatten och i närvaro av cellens huvudsakliga svavelbaserade antioxidant, glutathion, för att undvika omfattande, ospecifik skada.
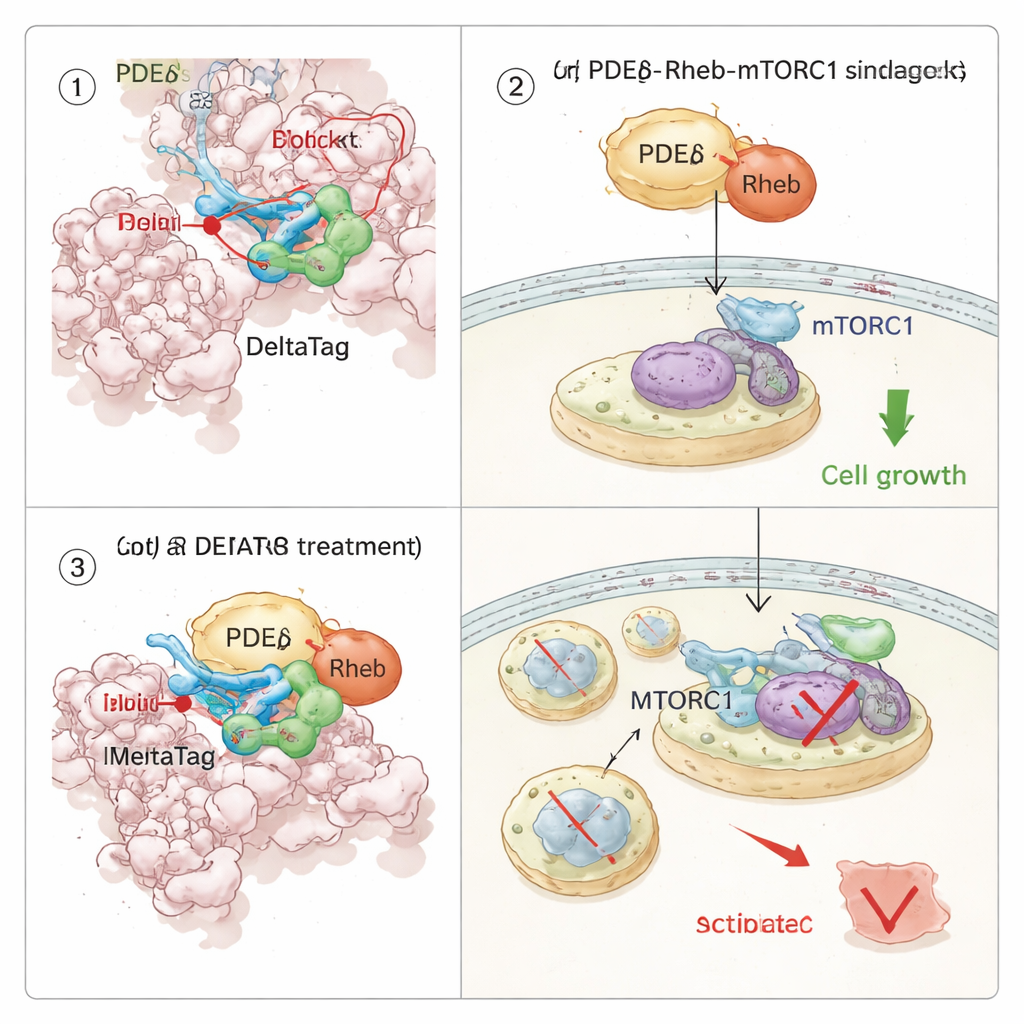
Omkoppling av en tillväxtväg inuti cancerceller
Eftersom PDEδ transporterar Rheb, och Rheb i sin tur aktiverar mTORC1‑tillväxtvägen, undersökte teamet hur kovalent hämning av PDEδ skulle påverka cellens signalering. Genom termisk stabilitetsprofilering över tusentals proteiner visade de att DeltaTag binder selektivt till PDEδ i cellextrakt och påverkar proteiner länkade till Rheb–mTOR‑axeln. I live‑cell‑avbildning orsakade DeltaTag att Rheb flyttade från ett diffust mönster i cellens inre till mer klustrade interna membraner, vilket stämmer med störning av dess normala transport. Global fosfoproteomik och riktade Western‑analyser visade att mTORC1‑aktiviteten, följd genom fosforylering av ett ribosomalt protein kallat S6, sjönk över tid medan kompensatoriska signaler i närliggande vägar ökade. Viktigt är att i flera mänskliga cancercellinjer drivna av muterat KRAS och beroende av stark mTOR‑signalering bromsade DeltaTag cellproliferationen mer effektivt än nära besläktade reversibla hämmare, och dess effekt var svagare i celler utan PDEδ, vilket stödjer att dess huvudsakliga verkan är på målet.
Öppnar en dörr till nya typer av läkemedelsmål
Detta arbete visar att det är möjligt att bygga små molekyler som bildar en permanent, mycket specifik bindning till en enskild glutamat dold i en fetthållande ficka på ett protein, med relativt enkel haloalkan‑kemi lånad från HaloTag. I modellsystemet PDEδ ger den kovalenta länken ett mer bestående block av en cancerrelevant tillväxtväg än tidigare reversibla läkemedel. Mer generellt kan samma designlogik tillämpas på andra proteiner som har hydrofoba håligheter men saknar de vanliga ”reaktiva” aminosyrorna, så länge de uppvisar en strategiskt placerad glutamat eller aspartat. Med vidare optimering kan glutamat‑riktade kovalenta hämmare som DeltaTag bli användbara verktyg för kemisk biologi och i slutändan ledande kandidater för nya terapier som tar sig an i dagsläget svår‑att‑läka proteiner.
Citering: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Nyckelord: kovalenta hämmare, riktning mot glutamat, PDEδ, mTOR‑signalering, cancerläkemedelsdesign