Clear Sky Science · sv
Konstruera syntetiska celler med intramembrandomäner som har distinkta tvålagersasymmetrier
Varför små syntetiska bubblor spelar roll
Varje levande cell är omsluten av ett membran som beter sig som en smart, flexibel hud. Denna hud är inte enhetlig: det inre och yttre lagret, och till och med olika fläckar längs ytan, kan ha mycket olika sammansättningar och former. De skillnaderna hjälper celler att sända signaler, binda proteiner och till och med dela sig. Ändå har det varit ovanligt svårt att bygga enkla, kontrollerbara modellmembran som fångar denna komplexitet. Denna studie presenterar ett praktiskt sätt att skapa cells-stora ”syntetiska celler” vars membran är asymmetriska på båda sidor och lateralt mönstrade i distinkta regioner — vilket öppnar en väg mot mer realistiska cellimiterare och mot att studera hur membranmönster driver knoppning och delning. 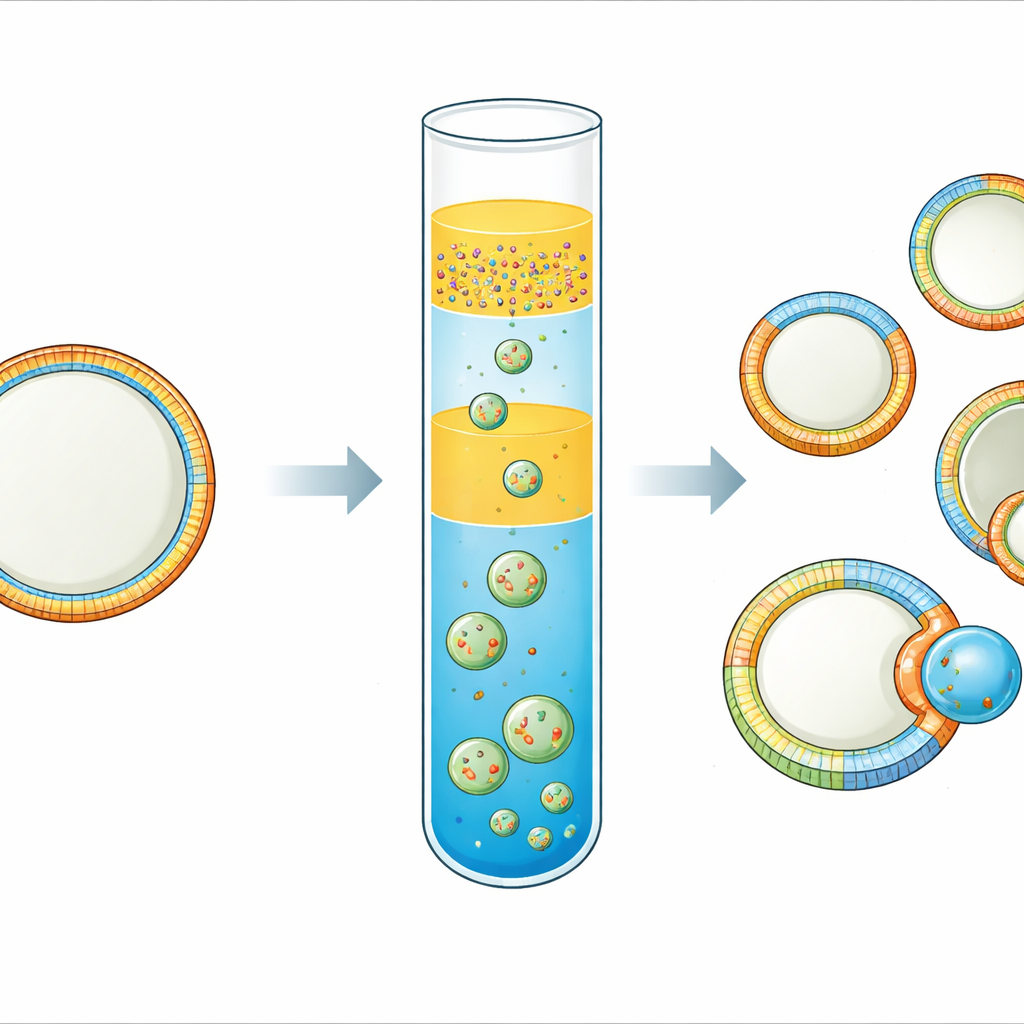
Bygga bättre cellimiterare
Riktiga cellmembran är asymmetriska: insidan är rik på negativt laddade lipider som rekryterar signalproteiner, medan utsidan bär andra lipider som medierar cell–cell-igenkänning. Många laboratoriemetoder kan skapa jättestora vesiklar — ihåliga sfärer av fettliknande molekyler — men deras två blad brukar bli likadana och insidan är svår att komma åt. Andra tillvägagångssätt som skapar asymmetri kräver ofta komplexa apparater, speciallipider eller gör att vesiklarna fastnar på en yta. Författarna ville skapa fristående, cells-stora vesiklar som kombinerar hög inneslutning av biomolekyler med robust, justerbar asymmetri mer lik den i en levande cell.
Recept i tre lager för asymmetriska membran
Gruppen förfinade en ”inverterad emulsion”-teknik, där små vattendroppar täckta med lipider pressas genom ett olja–vatten-gränssnitt för att bilda vesiklar. Deras nyckelinnovation är en trippellager-oljearrangemang. Längst ner ligger en olja som innehåller de lipider som ska bli det yttre bladet av membranet. Ovanpå detta placerar de ett tunt spacer-lager av olja utan lipider, och överst finns en emulsion av vattendroppar omgivna av en andra olja som bär lipider för det inre bladet. Under en kort centrifugeringssteg faller dropparna genom spacer- och bottenlagret, plockar upp en andra lipidkappa och sluter sig till vesiklar. Att välja två oljor med olika densitet och inkludera spacern begränsar kraftigt blandning mellan lipidförråden, så att inre och yttre blad behåller distinkta sammansättningar.
Testa att de två sidorna förblir olika
För att verifiera att de verkligen hade olika blad använde forskarna både kemiska och proteinbaserade avläsningar. I en uppsättning tester tillsatte de en fluorescerande lipid endast till ett blad och utsatte sedan vesiklar för ett kemiskt ämne i den yttre lösningen som släcker fluorescensen men inte kan korsa membranet. När den fluorescerande lipiden sattes på utsidan sjönk signalen nästan helt; när den sattes på insidan förändrades den knappt, vilket visade att de märkta lipiderna mestadels stannade där de var avsedda. I en andra experimentserie placerade de lipider som binder specifika proteiner — såsom biotin-märkta lipider för streptavidin eller speciella huvudgrupper för His-märkta grönt fluorescerande protein — endast i ett blad. Proteiner som tillsattes i motsatt fack (inuti eller utanför) band endast när deras matchande lipid fanns på samma sida av membranet, vilket bekräftar både stark asymmetri och bevarad proteinfunktion.
Skapa flottiljer och observera membranknoppning
Riktiga cellmembran innehåller också ”raftar”: små fläckar som är förtjockade i vissa lipider som kolesterol och sfingomyelin, vilka kan klustra proteiner och påverka form. Att åstadkomma sådan fasskillnad med inverterad emulsion-metoden hade varit svårt eftersom kolesterol tenderade att stanna löst i oljan snarare än gå med i membranet. Genom att använda squalen i bottenoljans lager — som håller kolesterol mindre starkt än standard mineralolja — kunde författarna reproducibelt bilda vesiklar vars membran delade upp sig i samexisterande flytande-ordnade och flytande-ordningslösa regioner, mycket likt raftar. De kombinerade sedan detta laterala mönster med blad-asymmetri: en domän bar ett inre-blad ligand som band streptavidin inuti, medan en annan domän bar glykolipider som band koleratoxin utanför. 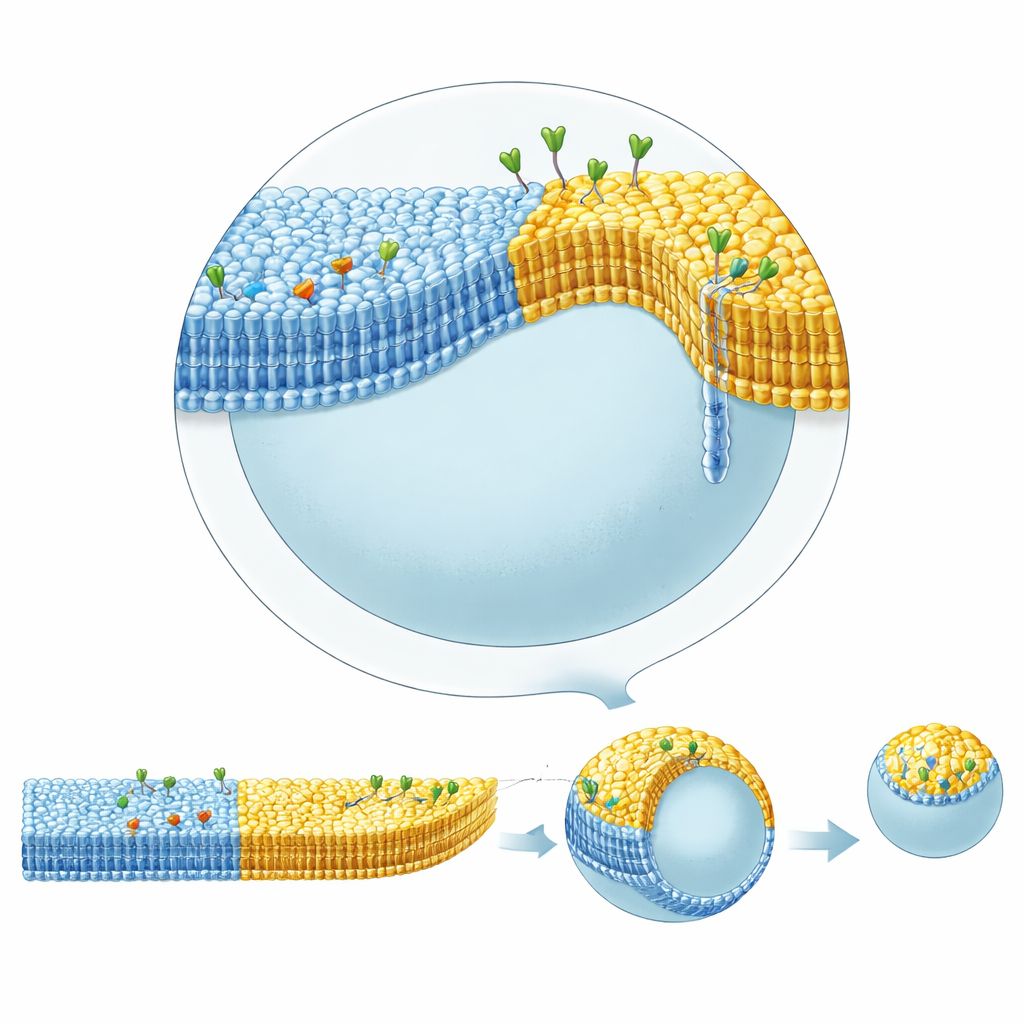
Hur proteiner och mönster driver formförändringar
Dessa komplexa vesiklar visade slående formdynamik. När koleratoxin band till glykolipider i den ordnade domänen på utsidan, buktade den domänen utåt till en krökt knopp kopplad med en smal nacke, och vid lätt osmotic deflation kunde den helt nypas av som en dottervesikel. Denna knoppning krävde inte energibärande molekyler som ATP eller specialiserad delningsapparatur; den uppstod rent från samverkan mellan lipidsammansättning, domängränser och asymmetrisk proteinbindning. Genom att öka mängden streptavidin bundet på insidan av den oordnade domänen kunde teamet motverka den utåtböjande kraften från den ordnade domänen och gradvis återställa en mer sfärisk form. Detaljerad geometrisk analys av vesikelkonturer visade att membranets krökning hoppar vid gränsen mellan domäner, och att de smala nackarna som sluts under knoppning måste tåla krafter på minst tiotals pikonewton — vilket kvantifierar hur domänstruktur och proteinträngsel mekaniskt kan forma membran.
Vad detta betyder för framtida syntetiska celler
I vardagliga termer har författarna utvecklat ett recept för att göra mjuka, cells-stora bubblor vars skinn är mönstrade och tvåsidiga på ungefär samma sätt som riktiga cellmembran. Eftersom metoden är relativt enkel, fungerar med många olika lipider och tillåter proteiner och andra stora molekyler att fångas inuti, banar den väg för att bygga mer livliknande konstgjorda celler från grunden. Sådana syntetiska celler kan hjälpa forskare att dissekera hur membranmönster styr signalering, trafik och delning, och de kan så småningom utnyttjas som smarta läkemedelsbärarna som ändrar form eller delar sig på kommando i kroppen.
Citering: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Nyckelord: syntetiska celler, lipidmembran, membranasymmetri, fasseparation, membranknoppning