Clear Sky Science · sv
Virala glykoproteiners nanodiscplattform för vaccinanalys
Att göra virusproteiner till mätbara mål
Moderna vacciner bygger i allt högre grad på noggrant designade versioner av de proteiner som pryder virusytan. Dessa proteiner är huvudmålen för skyddande antikroppar, men de är ökända för att vara svåra att studera i sin naturliga, membranbundna form. Den här artikeln beskriver en ny laboratorieplattform som placerar fullängds virala ytanproteiner i små, platta lipidpartiklar kallade nanodiskar. Denna uppställning låter forskare mäta hur väl vaccinämnen efterliknar verkliga virus, hur antikroppar fäster vid dem och hur man kan omdesigna vaccinerna för bättre skydd.
Varför det spelar roll att återskapa virusytan
Många av de viktigaste virusproteinerna är förankrade i ett fettrikt membran, precis som på ett faktiskt virus. Traditionella laboratoriemetoder kapar bort membrandelarna för att göra proteinerna enklare att producera och rena i lösning. Men den genvägen tar bort regioner nära membranet som innehåller särskilt värdefulla antikroppsmål, inklusive ett segment av HIV känt som den membran-proximala externa regionen (MPER). Dessa närmembranregioner kan se annorlunda ut och bete sig annorlunda när de inte är inbäddade i en realistisk lipidmiljö, vilket innebär att lösliga proteinfragment kan ge en ofullständig eller missvisande bild av hur ett vaccin kommer att prestera i kroppen.
Bygga en mångsidig nandiscplattform
Forskarna utvecklade ett strömlinjeformat femdagarsflöde för att hämta fullängds virala ytanproteiner från humana celler, behålla deras naturliga membrangenomgående segment intakta och återinsätta dem i en kontrollerad lipidskiva. De uttryckte först konstruerade HIV- och Ebola-glykoproteiner på cellytor, extraherade dem försiktigt med detergent och fångade dem på en reningsmatris. Medan proteinerna fortfarande satt fast blandade de in definierade lipider och ett bältesliknande scaffold-protein som självmonterar till en liten, diskformad membranstruktur. När detergenten avlägsnades satte sig de virala proteinerna i dessa nanodiskar. De resulterande preparaten var mycket rena, stabila i månader i kylskåp och bar glykankoatings (sockerlager) som nära matchade dem som finns på nativen virusspikar. 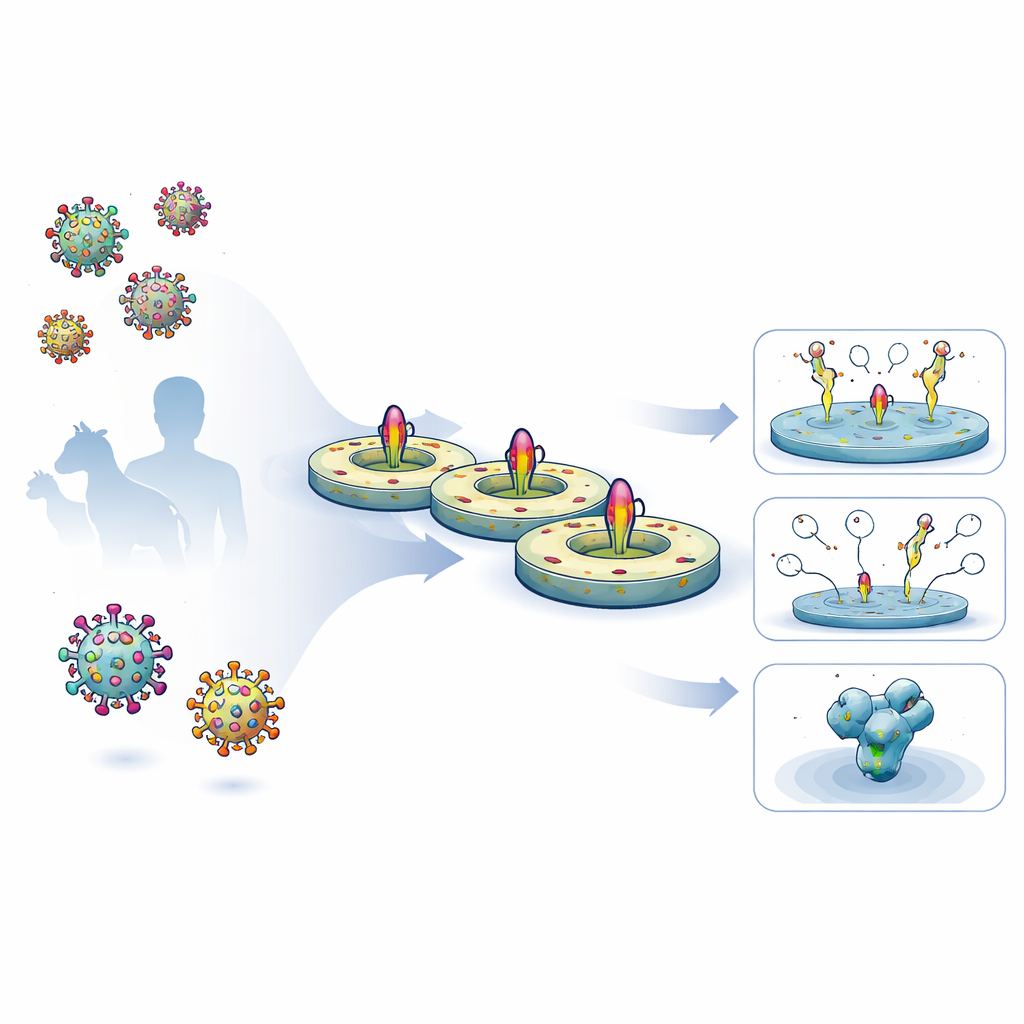
Avläsa antikroppsbindning och immunsvar
Med nanodisc-inbäddade proteiner i handen testade teamet hur väl olika antikroppar kunde binda under flera ytplasmonresonans- (SPR) upplägg, en teknik som följer bindning i realtid. Med HIV-nanodiskar designade för att exponera MPER-regionen visade de att en potent brett neutraliserande antikropp kallad 10E8 band ungefär 70 gånger starkare till den designade konstruktionen än till en tidigare design, mestadels därför att den släppte mycket långsammare. Kontrollmutationer som störde MPER-regionen eliminerade helt 10E8-bindningen, vilket bekräftar att plattformen känsligt kan rapportera hur designändringar påverkar viktiga epitoper. Samma nanodiskar fungerade som prober i flödescytometri, där de hjälpte till att fånga ut B‑celler från immuniserade möss och apor som kände igen den fulla transmembranformen av HIV-proteinet, inklusive delar som saknas i standardlösliga prober. 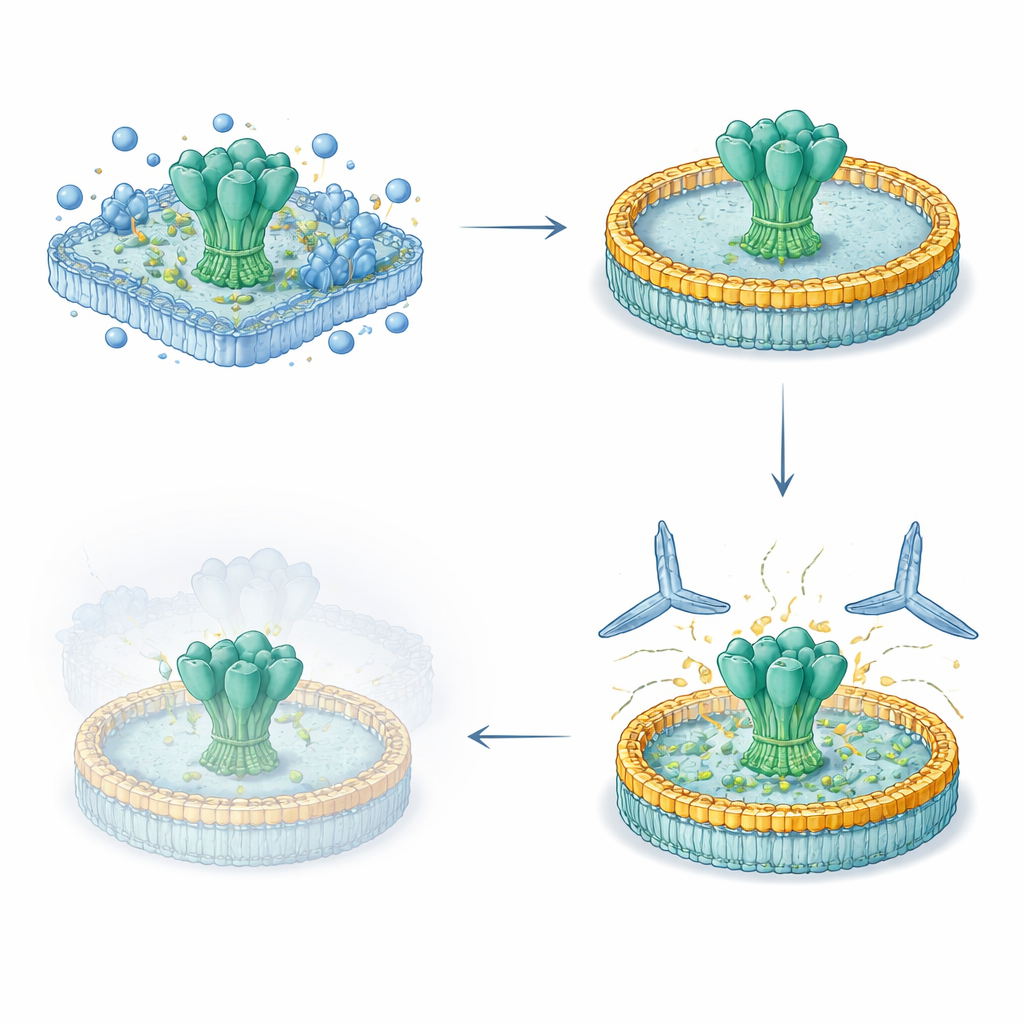
Se målet i atomdetalj
För att förstå exakt hur antikroppar känner igen MPER i dess naturliga miljö använde författarna kryogen elektronmikroskopi för att avbilda de designade HIV-nanodiskarna bundna till tre olika brett neutraliserande antikroppar. De erhöll en 3,5 ångström struktur av en antikropp, 10E8, som engagerar MPER-segmentet medan resten av HIV-spiken förblev förankrad i lipidskivan. Detta avslöjade ett kontinuerligt nätverk av kontakter mellan 10E8 och både MPER och närliggande delar av det yttre proteinet, inklusive en djup ficka vid skarven mellan två subenheter. Genom att jämföra denna struktur med tidigare bilder av 10E8 bunden endast till ett kort peptidfragment visade teamet att membranmiljön och fullängds-spiken tillåter extra kontakter och dynamiska rörelser som var osynliga i enklare modeller, och att specifika aminosyror i viruset starkt påverkar hur lätt 10E8 kan neutralisera det.
Breda tillämpningar för smartare vacciner
I praktiska termer ger denna nandiscplattform vaccinformgivare ett sätt att utvärdera transmembrana vaccin-kandidater med samma kraftfulla analytiska verktyg som länge reserverats för lösliga proteinfragment. Den fungerar över olika virus, stöder detaljerade bindningsmätningar, möjliggör precis sortering och sekvensering av vaccininducerade B‑celler och ger högupplösta strukturer som fångar realistiska membranproximala epitoper. För en lekmannaläsare är slutsatsen att forskare nu har en mer livlik testbädd för virala ytanproteiner — en som kan visa vilka vaccindesigner som verkligen ser ut och beter sig som det verkliga viruset och hur man justerar dem för starkare, bredare antikroppssvar. Detta bör påskynda utvecklingen av nästa generations vacciner inte bara för HIV utan för många andra omslutna virus.
Citering: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Nyckelord: nanodiskar, HIV-vacciner, virala glykoproteiner, brett neutraliserande antikroppar, kryo-EM