Clear Sky Science · sv
Radikal footprinting i hela däggdjursblod
Se proteiner i arbete i verkligt blod
Proteiner i vårt blod ändrar ständigt form när de utför viktiga uppgifter som att bekämpa infektioner, transportera järn och reagera på sjukdom. Hittills har de flesta verktyg för att studera dessa små formförändringar fungerat endast i förenklade prov eller isolerade celler. Denna studie visar för första gången att forskare kan avläsa proteinernas former direkt i intakt däggdjursblod, vilket öppnar en väg att i realtid följa sjukdomsprocesser i kroppen.
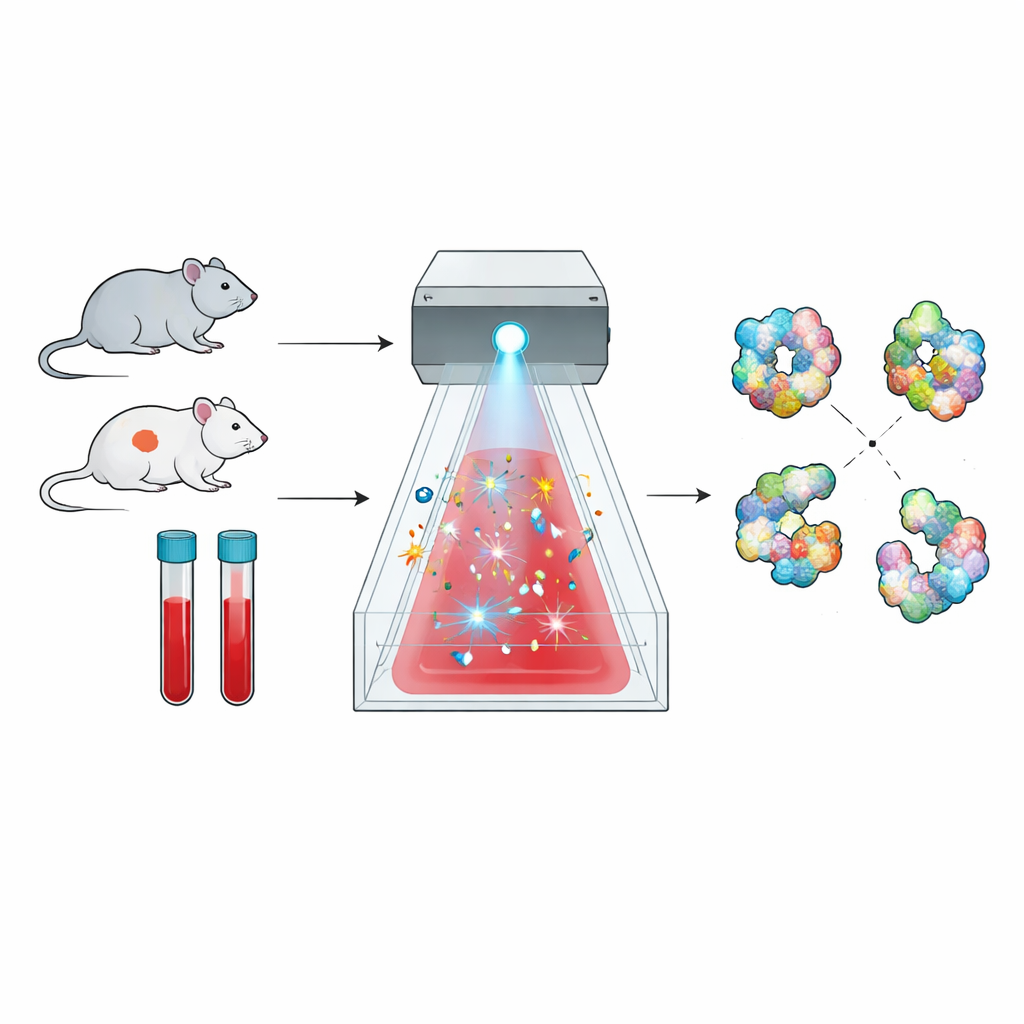
En ny metod för att kartlägga proteinformer
Proteiner är inte stela kulor; de viker sig till intrikata tredimensionella former, och dessa former avgör vad de kan göra. Metoden som här undersöks, kallad radikal protein-footprinting, utnyttjar detta. Korta stötar av mycket reaktiva molekyler fungerar som en kemisk ”kamerablixt” och angriper endast de delar av ett protein som är utsatta mot omgivande vätska. Sen används masspektrometri för att räkna var dessa kemiska träffar skett, vilket producerar en slags ytkarta, eller fotavtryck, av varje proteins form. Skillnader i det fotavtrycket mellan friska och sjuka tillstånd visar subtila skiftningar i hur proteinet är vikt eller hur det interagerar med partners.
Få tekniken att fungera i hela blodet
Att tillämpa detta tillvägagångssätt direkt i blod har länge varit en utmaning. Blod absorberar ultraviolett ljus kraftigt och är fullpackat med enzymer, som katalas, som snabbt förstör de vanliga radikalgenererande kemikalierna innan de hinner markera proteinerna. Forskarna löste detta genom att byta till natriumpersulfat, som kan splittras av ett starkt bredbandsblixtljus till kraftfulla sulfatradikaler. Med ett kommersiellt system kallat FOX visade de att persulfat kan aktiveras pålitligt och att en inbyggd dosimetriläsning kan spåra hur många radikaler som produceras, vilket möjliggör noggrann kontroll av den ”exponering” varje prov får.
Skydda celler samtidigt som detaljer fångas
Eftersom metoden är avsedd att studera proteiner i något som ligger nära deras naturliga miljö var det avgörande att blodcellerna inte förstördes. Tester på musblod visade att tillsats av koncentrerat persulfat orsakade endast mindre, reversibla förändringar i röda blodkroppars form och mindre än två procents cellruptur, liknande enkla saltslösningar. Teamet utvecklade också en förbättrad ”quench”-blandning som snabbt tar upp kvarvarande reaktiva arter och förhindrar oönskad skada från långsammare sidoreaktioner efter blixten. Tillsammans gjorde dessa förbättringar det möjligt att märka proteiner i intakt musblod samtidigt som cellstrukturen bevarades och bakgrundsbruset hölls mycket lågt.
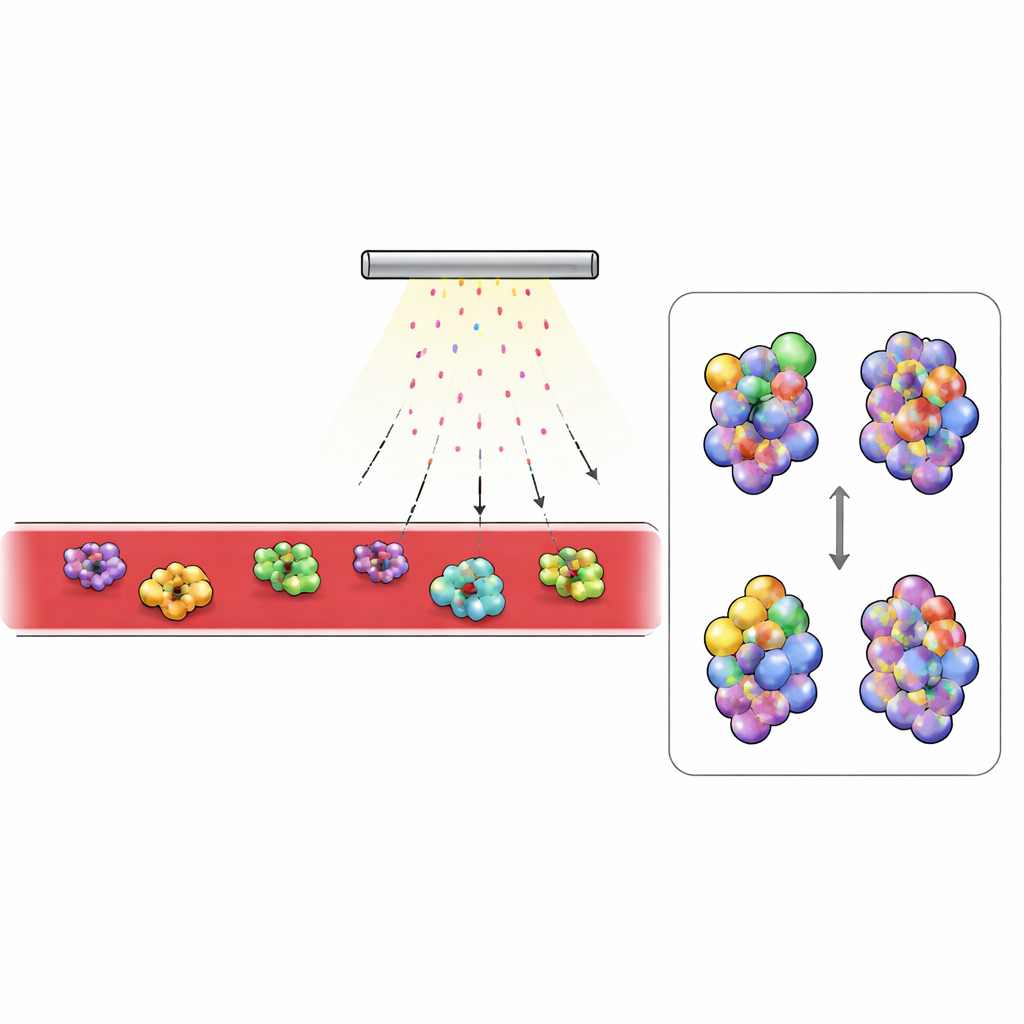
Vad som förändras i diabetiskt blod
Med denna plattform i handen jämförde forskarna blod från friska möss och från en vanlig modell för typ 2-diabetes. De fokuserade på de mest abundanta proteinerna som upptäcktes, särskilt de som cirkulerar utanför cellerna. Extracellulära proteiner visade mycket kraftigare märkning än de inne i cellerna, vilket speglar begränsad penetration av persulfat in i cellernas inre. Två blodproteiner stack ut: komplement C3, en nyckelkomponent i immunsystemet, och transferrin, som transporterar järn. Hos diabetiska möss var regioner av C3 som blir dolda när proteinet övergår till sin aktiva form mindre märkta, medan normalt dolda regioner var mer exponerade. Detta mönster stämde överens med den kända strukturella förändringen när C3 omvandlas till sin aktiva fragmentform C3b, och blodtester bekräftade att diabetiska djur hade mycket mer aktiverat C3. I transferrin var områden nära järnbindningsstället mer skyddade i diabetiskt blod, vilket överensstämmer med att proteinet bar mer järn. Oberoende mätningar visade högre serumjärn och en större andel transferrin mättat med järn hos de diabetiska mössen.
Varför detta är viktigt för hälsa och medicin
För en icke-specialist är det väsentliga budskapet att författarna har skapat ett sätt att ”känna” formerna hos många proteiner samtidigt direkt i verkligt blod och sedan använda dessa formmönster för att härleda hur sjukdom ändrar kroppens kemi. I denna musmodell av typ 2-diabetes avslöjar metoden överaktiv komplementaktivering och högre järnlast på transferrin — förändringar som klassiska tester kan missa eller bara se indirekt. Eftersom tillvägagångssättet fungerar i små blodprov och använder en standardiserad ljuskälla kan det så småningom hjälpa till att identifiera tidiga strukturella varningstecken för sjukdom, följa hur biologiska läkemedel beter sig i blodomloppet och vägleda utformningen av mer effektiva behandlingar.
Citering: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
Nyckelord: strukturell proteomik, blodproteiner, typ 2-diabetes, komplementsystemet, järnmetabolism