Clear Sky Science · sv
Variationer i proteiners C-terminal påverkar proteostas
Hur proteiners svansform påverkar hälsan
Varje protein i våra celler slutar med en liten ”svans” bestående av bara några byggstenar. Dessa svansar kan verka som en bisak, men denna studie visar att de tyst avgör vilka proteiner som blir kvar och vilka som snabbt tas bort. Eftersom proteinnivåer ligger bakom cancer, genetiska sjukdomar och hur celler reagerar på stress, ger förståelsen av dessa svansar nya sätt att bedöma sjukdomsrisk och även utforma framtida behandlingar.
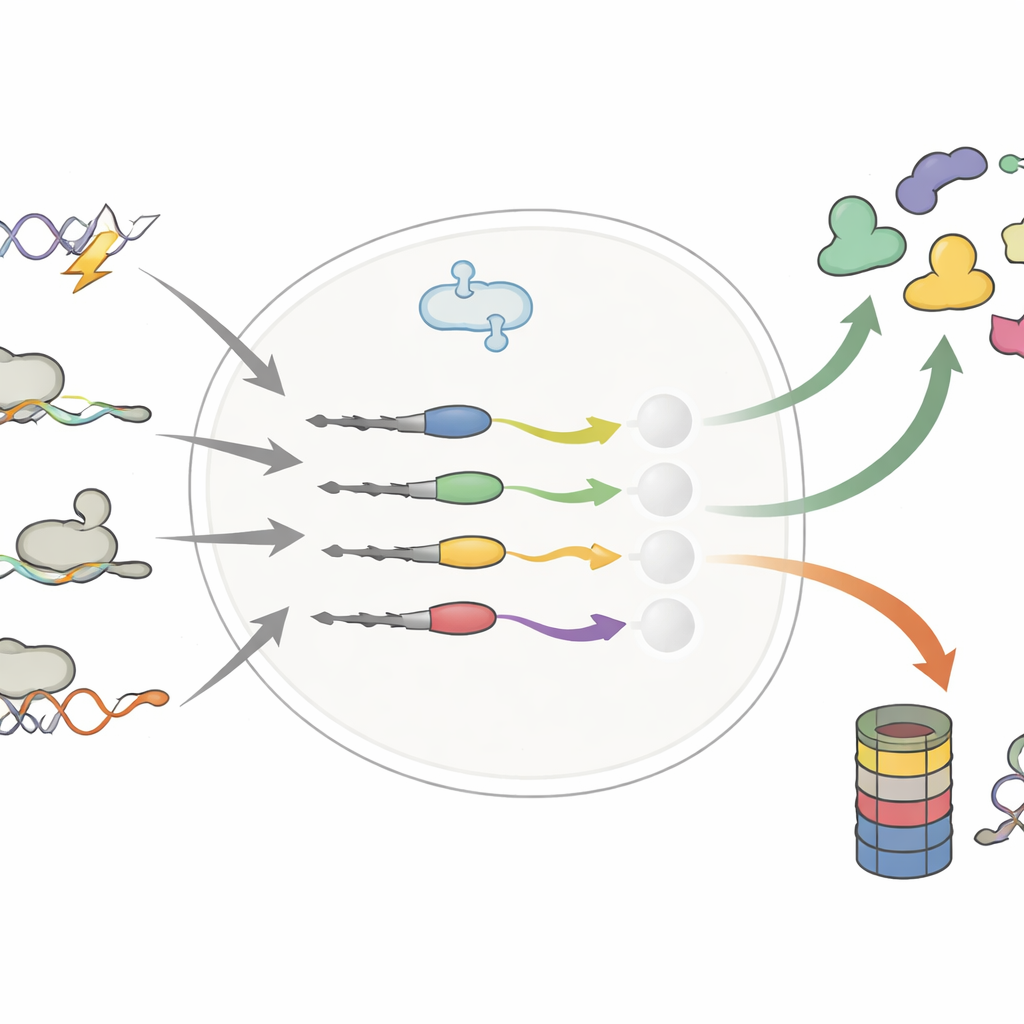
Små förändringar i proteinsvansen, stora skillnader i livslängd
Författarna fokuserade på proteinerna längst ut — C-terminalen — där redan några extra eller utbytta byggstenar kan uppstå genom DNA-mutationer, alternativ RNA-splitsning eller att ribosomer läser förbi den vanliga stoppmarkeringen. Tidigare arbete antydde att sådana ”felaktiga” svansar främst fungerar som märken för borttagning och skickar defekta proteiner till cellens kvarn. Genom att systematiskt jämföra tusentals normala och förändrade svansar omstörtar denna studie den enkla bilden. Gruppen visar att ändrade svansar antingen kan förkorta eller förlänga ett proteins livslängd, ibland stabilisera cancerdrivare eller destabilisera tumörhämmare.
När genetiska fel hjälper eller skadar proteiner
En huvudorsak till svansförändringar är nonstop-mutationer, som utplånar en normal stopp-signal så att ribosomen fortsätter in i ett RNA-område som vanligtvis är tyst. Forskarna testade över 3 000 sjukdomsassocierade nonstop-varianter med en tvåfärgad rapportör som mäter hur väl varje svans skyddar eller försvagar ett modellprotein. I genomsnitt gjorde de mutanta svansarna fortfarande proteiner mindre stabila än deras normala motsvarigheter, men en betydande andel gjorde tvärtom: ungefär en av tio nonstop-mutationer stabiliserade proteiner, medan nästan en tredjedel destabiliserade dem. Dessa förändringar påverkade välkända onkoproteiner och tumörsuppressorer, vilket tyder på att vad som verkade vara subtila mutationer i själva verket kan rubba balansen mellan celltillväxt och celldöd.
Inbyggd variation från splitsning och läsgenom
Inte alla svansskillnader är olyckor. Våra gener producerar rutinmässigt flera proteinkonfigurationer genom alternativ splitsning och programmerad läsgenomgång av stoppkodon. Genom att gräva i humana genkataloger fann författarna att nästan två tredjedelar av generna ger upphov till proteiner med mer än en svansdesign, och många skiljer sig endast i de sista få byggstenarna. Test av utvalda exempel visade att dessa nästan identiska versioner ofta har tydligt olika halveringstider. Vissa läsgenomgenererade svansar gjorde proteiner mer stabila, andra mindre. Detta tyder på att celler avsiktligt använder svansvariation som en finjusteringsmekanism och anpassar hur länge specifika proteinformer kvarstår i olika vävnader eller förhållanden.
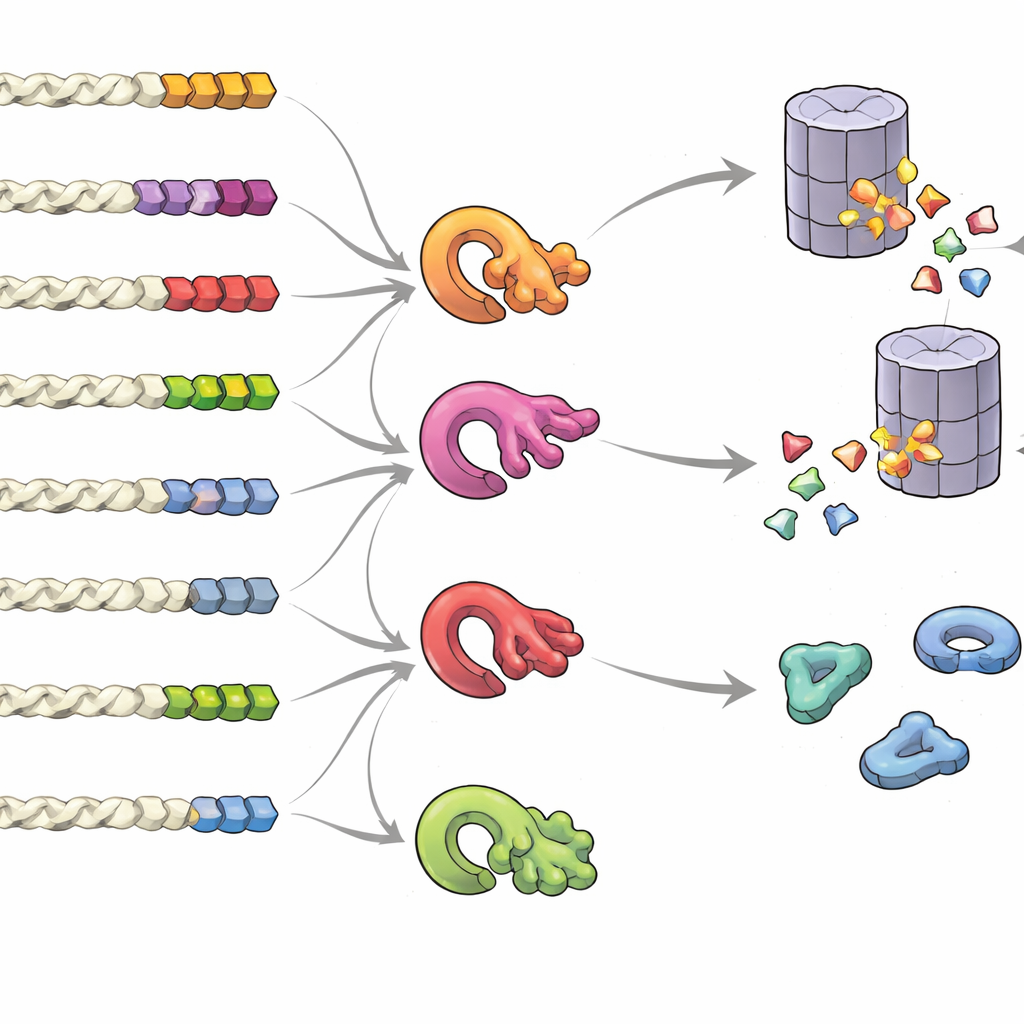
Vad gör en svans till en ”behåll mig”- eller ”släng mig”-signal
För att förstå vilka egenskaper hos en svans som påverkar proteinets öde skapade teamet bibliotek av slumpmässiga svansar och mätte deras påverkan i stort. De fann att det inte bara är ett enda fast ”motiv” utan den totala sammansättningen, positionen och klustringen av vissa byggstenar som spelar roll. Svansar rika på små eller oljiga komponenter, eller de mer sällsynta cystein- och tryptofanresiduerna, tenderade att inbjuda nedbrytning, särskilt när dessa rester klustrade. Däremot gynnade svansar med många sura komponenter stabilitet. Sett över många arter visade normala proteinsvansar tydliga tecken på evolutionärt tryck att undvika riskfyllda mönster, medan felbenägna läsgenom- eller frameshift-svansar var förskjutna mot destabiliserande sammansättningar. Gruppen upptäckte också att flera kvalitetskontrollenzymer — olika ubiquitin-ligasar — specialiserar sig på att känna igen distinkta hydrofoba svansmönster och bildar ett intrikat nätverk som avgör vilka proteiner som ska förstöras.
Varför detta är viktigt för medicin och bioteknik
Arbetet omformulerar proteinsvansar från passiva ändpunkter till aktiva regulatorer av proteinmängd. För en lekman innebär det att många sjukdomar kan uppstå inte bara av defekta proteiner utan också av subtila förändringar i hur länge proteiner består, drivna av små skillnader i deras ändar. Det varnar också för att terapier som avsiktligt främjar läsgenom av stoppsignaler, använda för att behandla vissa genetiska sjukdomar, oavsiktligt kan förändra livslängden för många normala proteiner. Samtidigt antyder fynden kraftfulla nya strategier: genom att konstruera svanssekvenser eller påverka celler att favorisera vissa splitsformer eller läsgenomgångar kan forskare en dag justera proteinnivåer upp eller ner med anmärkningsvärd precision.
Citering: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Nyckelord: proteinstabilitet, C-terminal svans, proteinnedbrytning, genetiska mutationer, proteostas