Clear Sky Science · sv
FANCD2 begränsar gaffelns framdrift och förhindrar bräcklighet vid tidiga origin vid re-replikation
När DNA-kopiorna avviker lite från manus
Varje gång en cell delar sig måste den kopiera hela sitt DNA-arkiv exakt en gång. Om delar av arkivet kopieras två gånger, eller kopieras på ett förhastat och slarvigt sätt, kan det leda till brutna kromosomer och mutationer som driver cancer. Denna studie undersöker vad som händer när cellens skydd mot extra kopieringsomgångar börjar svikta, och visar hur ett reparationsprotein kallat FANCD2 träder in för att hindra lindrigt olydiga celler från att glida in i fullständig genomisk kaos.
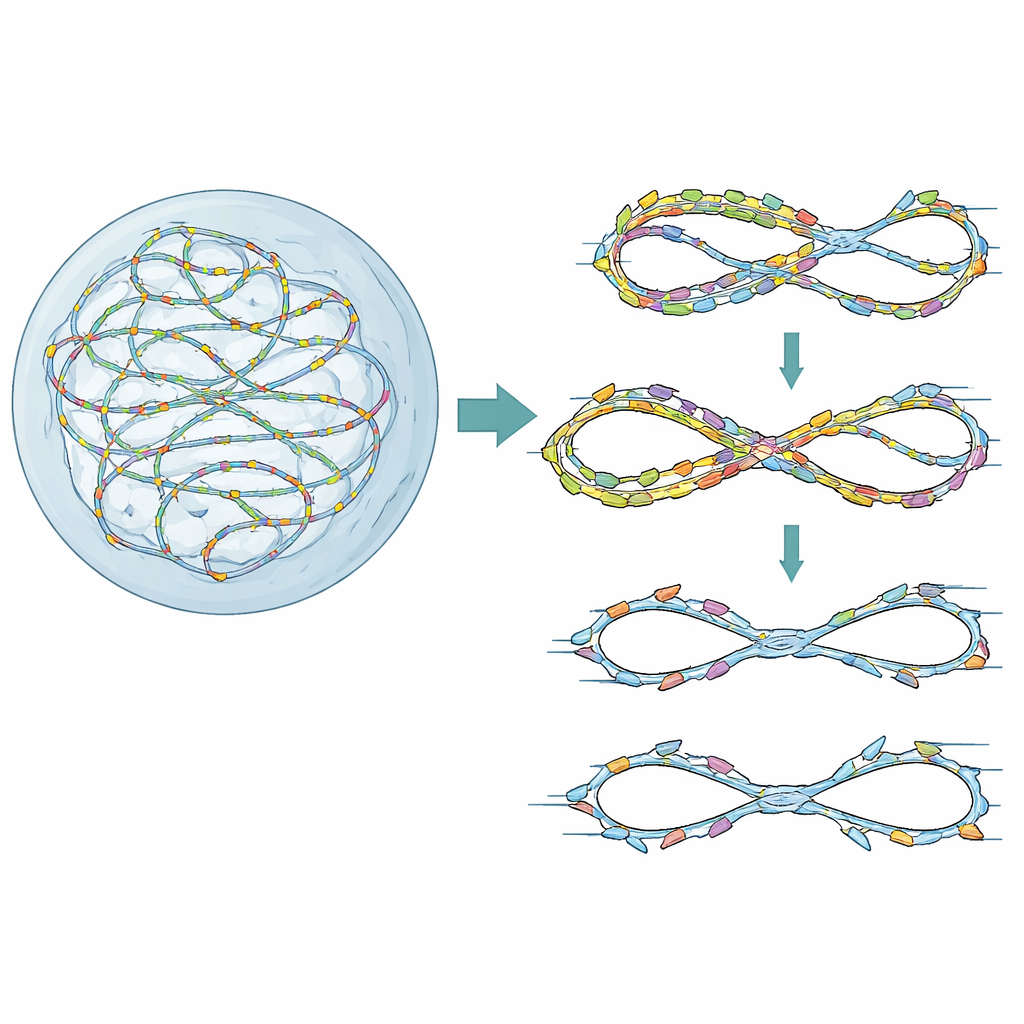
Väggrenar för en ren kopia
Våra kromosomer dupliceras från tusentals startpunkter, eller ”origin”, som licensieras och sedan aktiveras i en noggrant tidsbestämd ordning. Ett litet protein som heter Geminin hjälper normalt till att säkerställa att varje origin bara aktiveras en gång per cellcykel. När Geminin förloras eller försvagas kan vissa origin aktiveras igen på redan kopierat DNA, en situation som kallas re-replikation. Cancerceller, som ofta överproducerar licensieringsfaktorer, är särskilt benägna för detta problem. Författarna använde först en höginnehålls genetisk skärm i mänskliga celler som var förberedda för låg nivå av re-replikation genom att avlasta Geminin. De undersökte vilka DNA-reparations- och kontrollpunktgener som blir avgörande i detta stressade tillstånd och fann att FANCD2, mest känt för att reparera DNA-crosslinks vid Fanconi-anemi, framträdde som en nyckelaktör för cellsurvival och genomisk integritet.
Först på plats vid överarbetade kopieringsmaskiner
Gruppen följde sedan var och när FANCD2 dyker upp i celler som genomgår re-replikation. Strax efter att Geminin tagits bort ansamlas FANCD2 snabbt på kromatin och bildar starka nukleära fokus, långt innan utbredda DNA-brott är detekterbara. Genom att markera nysyntetiserat DNA tillsammans med närhetsanalyser visade de att FANCD2 rekryteras direkt till aktiva replikationsmaskiner, särskilt i celler där DNA redan kopieras en andra gång. I synkroniserade celler som släpptes in i nästa delningscykel framträdde en distinkt population med ett diffust, över-replikationsmönster i DNA:t. Dessa celler visade starka FANCD2- och RPA-signaler, vilket indikerar pågående replikationsstress, och hölls vid gränsen före mitos av en aktiv kontrollpunkt, vilket tyder på att FANCD2 är del av ett tidigt svar som stabiliserar stressade gafflar snarare än att enbart reagera på brutet DNA.
Hålla tillbaka okontrollerade gafflar och dolda luckor
För att testa hur FANCD2 påverkar DNA-kopieringen kombinerade forskarna Gemininförlust med FANCD2-avlastning. Överraskande ökade inte avlägsnandet av FANCD2 andelen celler med uppenbart re-replikerade genom. Istället visade enkelmolekylära DNA-fiberanalyser att replikationsgafflar färdades längre och blev mer asymmetriska, ett tecken på ojämn och instabil progression. Dessa snabbare gafflar lämnade efter sig fler enkelsträngade luckor i det nyligen gjorda DNA:t, synliga som intensiva RPA- och nativa BrdU-fokus och bekräftade av att de märkta spåren var känsliga för ett enzym som klipper enkelsträngade regioner. Celler som saknade både Geminin och FANCD2 uppvisade ett hopp i kromosombrott, fragment, nukleära kroppar och mikronuclei — alla kännetecken för svår genomisk instabilitet. Att blockera PARP, en faktor som normalt hjälper till att hantera sådana luckor, efterliknade och förvärrade dessa defekter, vilket understryker att okontrollerad luckbildning är central för skadorna.
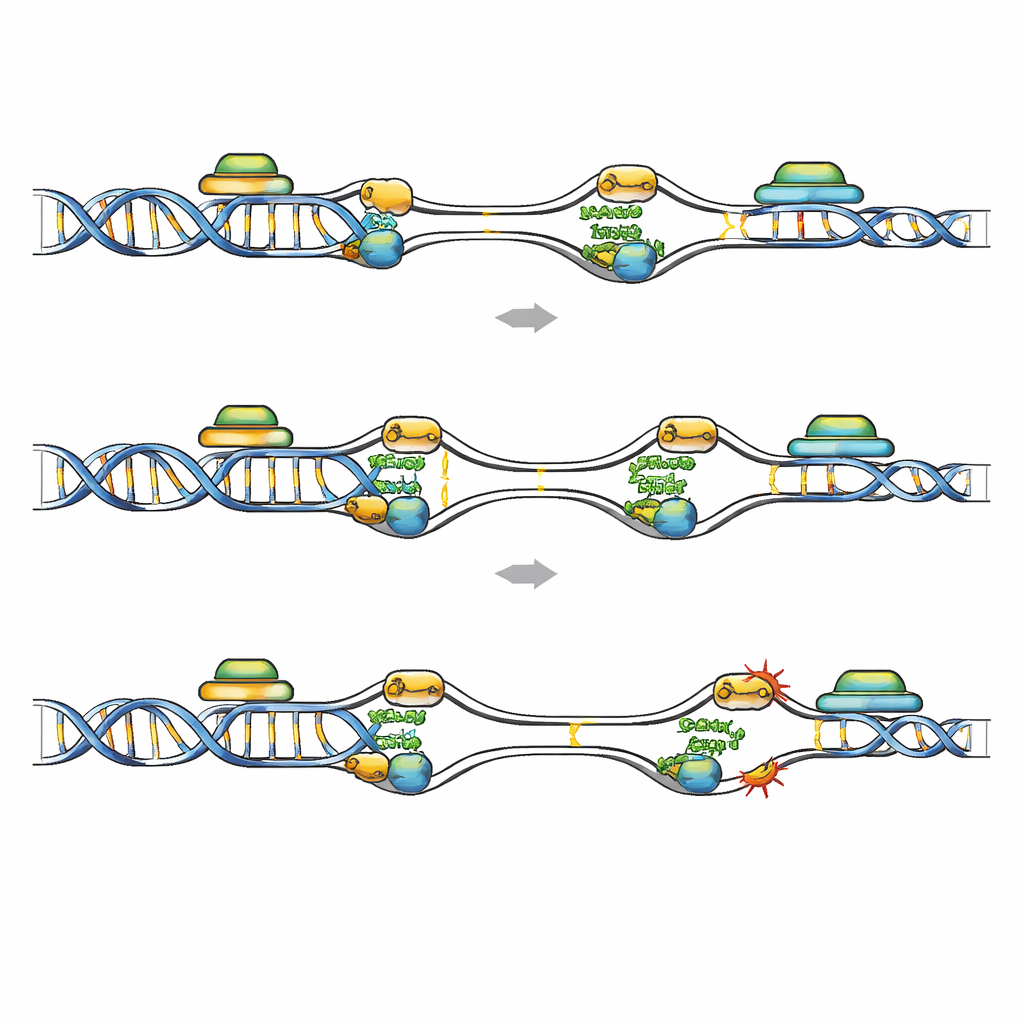
Bräckliga hotspots där kopiering och avläsning kolliderar
Genom att kartlägga FANCD2-bindning över genomet fick man en bild av var re-replikation är som farligast. I leukemiceller utan Geminin försköts FANCD2 från klassiska common fragile sites till tidigt aktiverade replikationsorigin inbäddade i korta, GC-rika, högt transkriberade gener. Dessa regioner bär tecken på aktiv transkription och är benägna att bilda R-loopar, där nybildad RNA hybridiserar med sitt DNA-templat och potentiellt blockerar replikation. Offentliga dataset visade mer DNA-skada och förhöjda RNA–DNA-hybrid-signaler i FANCD2-berikade gener efter Gemininförlust, och dessa regioner överlappade med så kallade tidigt replikativa bräckliga platser. När transkription dämpades bredare med ett läkemedel, eller när R-loopar specifikt avlägsnades genom överuttryck av RNase H1, minskade antalet FANCD2-, RPA- och DNA-skadefokus i Geminin-defekta celler markant. Detta indikerar att kollisioner mellan återaktiverade origin och aktiva transkriptionsenheter, förstärkta av R-loopar, skapar bräckliga hotspots som FANCD2 måste skydda.
Fintuning av skydd genom kemiska märken
FANCD2 aktiveras delvis genom fästning av en liten ubiquitinliknande tagg. Genom att avlasta FANCA, en kärnkomponent i märkessystemet, och genom att använda celler som uttrycker en FANCD2-mutant resistent mot denna modifiering, visade författarna att mono-ubiquitinering förbättrar överlevnaden hos re-replikerande celler men inte är absolut nödvändig. Även icke-märkt FANCD2 gav ett delvis skydd, vilket är förenligt med distinkta roller både i att känna av och i att stabilisera stressade gafflar. Helhetsbilden är att FANCD2 hjälper till att sakta ner och organisera replikationen vid känsliga tidiga origin och begränsar hur många och hur stora de enkelsträngade luckorna blir.
Varför detta spelar roll för cancerbehandling
För icke-specialister är kärnbudskapet att inte alla replikationsmisstag är katastrofala från början. Lindrig re-replikation, som förekommer i vissa tumörer, kan tolereras om skyddssystem som FANCD2 håller tillbaka okontrollerad DNA-kopiering och förhindrar att bräckliga luckor utvecklas till brutna kromosomer. När detta skydd tas bort eller överväldigas eskalerar samma låggradiga licensieringsfel snabbt till genomisk krossning. Eftersom Geminin-förlust och defekter i replikationslicensiering är förhöjda i cancerceller, och många tumörer redan har svagheter i Fanconi/BRCA-nätverket, tyder de sårbarheter som identifierats här på terapeutiska strategier: att kombinera inhibitorer som pressar cancerceller mot re-replikation med läkemedel som förvärrar luckansamling, såsom PARP-hämmare, skulle kunna driva maligna celler förbi deras toleransgräns samtidigt som normala celler med intakt skydd i större utsträckning sparas.
Citering: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Nyckelord: DNA-replikationsstress, FANCD2, Geminin, re-replikation, genominstabilitet