Clear Sky Science · sv
Låser upp enzymatisk deracemisering av strukturellt mångfaldiga allener med designade fotoenzymer
Varför mix‑and‑match av molekyler spelar roll
Många läkemedel fungerar endast när deras atomer sitter i en mycket specifik tredimensionell ordning, ungefär som att en vänsterhand bara passar i en vänsterhandske och inte i en höger. Kemister kan ofta framställa dessa ”entydigt handade” molekyler, men det är svårt att göra det rent när byggstenarna är komplexa. Denna artikel tar sig an den utmaningen för en knepig klass av vridna strukturer kallade allener genom att använda specialbyggda, ljusdrivna enzymer. Arbetet visar hur biologi och fotokemi kan kombineras för att sålla ut önskad molekylär ”hand” ur en förväxlad blandning och lovar snabbare och renare vägar till framtida läkemedel och material.
Vridna byggstenar med stor utdelning
Allener är linjära kedjor av tre kolatomer med två intilliggande dubbelbindningar, men denna enkla uppställning vrider rymden på ett sätt som ger hela molekylen en handighet. Dessa axiella vridningar förekommer i naturprodukter, växtskyddsmedel och avancerade katalysatorer. Tyvärr är traditionella metoder för att framställa chirala allener ofta mycket specialiserade: en katalysator som fungerar utmärkt för en allene misslyckas ofta för en annan med små strukturella förändringar. Även nyligen utvecklade ljusdrivna kemiska katalysatorer kämpar med detta problem. Följaktligen måste kemister gång på gång designa om katalysatorer från grunden när de vill utforska nya allener, vilket bromsar upptäcktstakten och ökar avfallet.
Lånar naturens selektivitet och tillsätter ljus
Enzymer i levande system är mästare på att känna igen och omvandla specifika former med anmärkningsvärd precision, men de har utvecklats för naturliga mål, inte för människotillverkade allener. Författarna gav sig därför i kast med att skapa ett ”fotoenzym” som kombinerar enzymlik selektivitet med förmågan att skörda ljus som energikälla. De började från ett proteinskellett kallat CTB10 och omprogrammerade det genetiskt för att bära en icke‑naturlig aminosyra som fungerar som en liten inbyggd ljusantenn. När denna specialbyggsten absorberar ultraviolett ljus kan den överföra energi till en närliggande allene, tillfälligt excitera den och låta dess vridning skakas om. Genom att upprepa denna process många gånger kan enzymet selektivt avlägsna ena handen från en 50:50‑blandning och lämna kvar mestadels den andra. 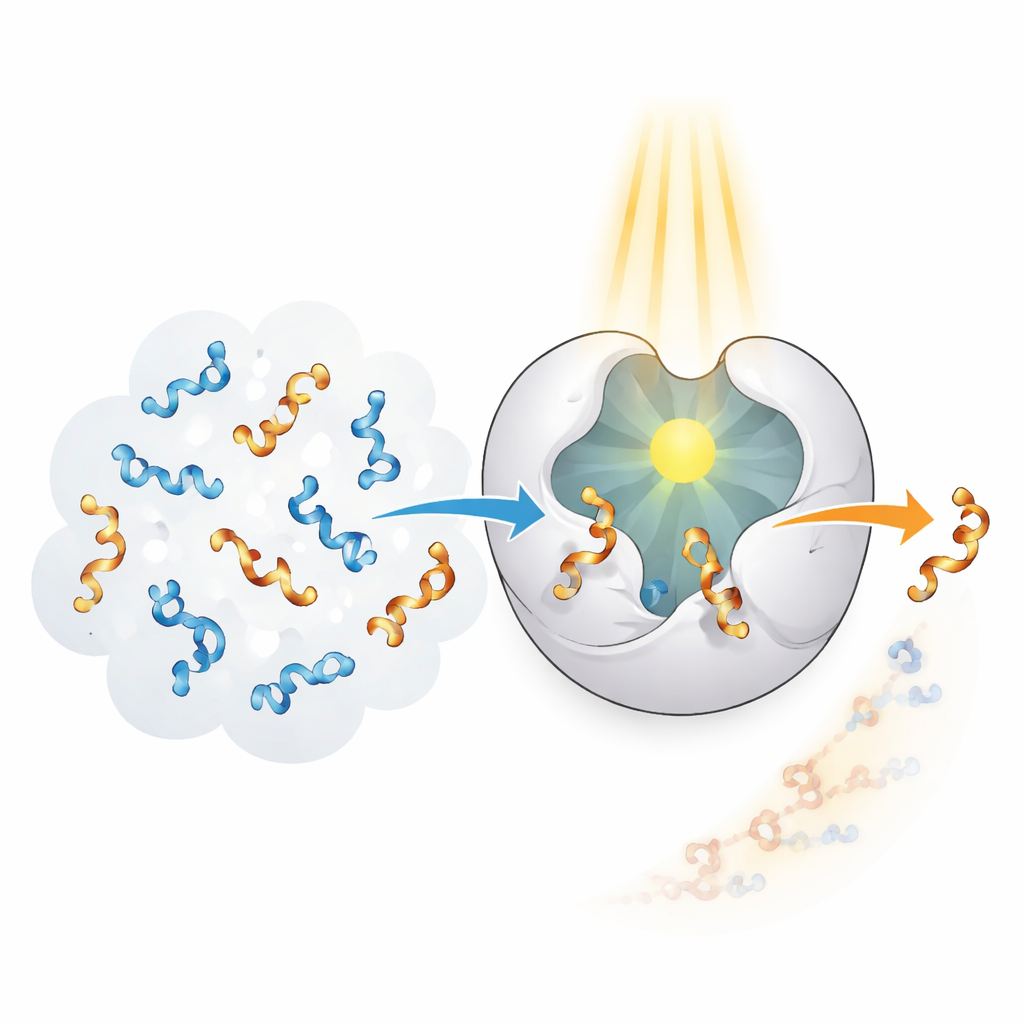
Skär ut åtsittande fickor för många olika gäster
Att designa ett sådant system är inte lika enkelt som att bara lysa på ett protein. Teamet använde datorbaserad modellering, strategiska mutationer och röntgensnapshots för att skulptera flera varianter av fotoenzymet, var och en med en något annorlunda intern ficka. Dessa fickor håller allenen i en definierad ställning intill ljusantennen och stabiliserar nyckeldelar av molekylen via vätebindningar och subtila packningsinteraktioner. Steg för steg förbättrade forskarna både bindningsstyrkan och inpassningen mellan enzym och allene, vilket är avgörande för effektiv energitransfer. De slutliga varianterna visade imponerande prestanda och omvandlade allensyror, estrar och amider till enhandade produkter med mycket hög renhet, ofta över 99 % av en handighet, och gjorde detta under luft utan behov av känsliga betingelser.
Observera mekanismen i atomupplösning
För att förstå varför de nya fotoenzymerna föredrar ena handen framför den andra, kristalliserade författarna enzym–substratpar och granskade dem i atomupplösning. De fann att den gynnade allenen sitter närmare ljussamlande gruppen och kan anta flera något olika former, alla kompatibla med effektiv energitransfer. Den ogynnade handen binder antingen svagt eller sitter längre bort, vilket gör att den är mycket mindre benägen att exciteras. Ytterligare experiment med rena höger‑ respektive vänsterhänta utgångsmaterial bekräftade denna skevhet: enzymet omvandlar snabbt den föredragna handen till ett reaktivt mellanled, som sedan relaxerar i lösning tillbaka till en blandning där motsatt hand ansamlas. I praktiken beter sig proteinet som en molekylär snurrgrind, som upprepade gånger exciterar och förbrukar ena handen medan den andra tillåts hopa sig. 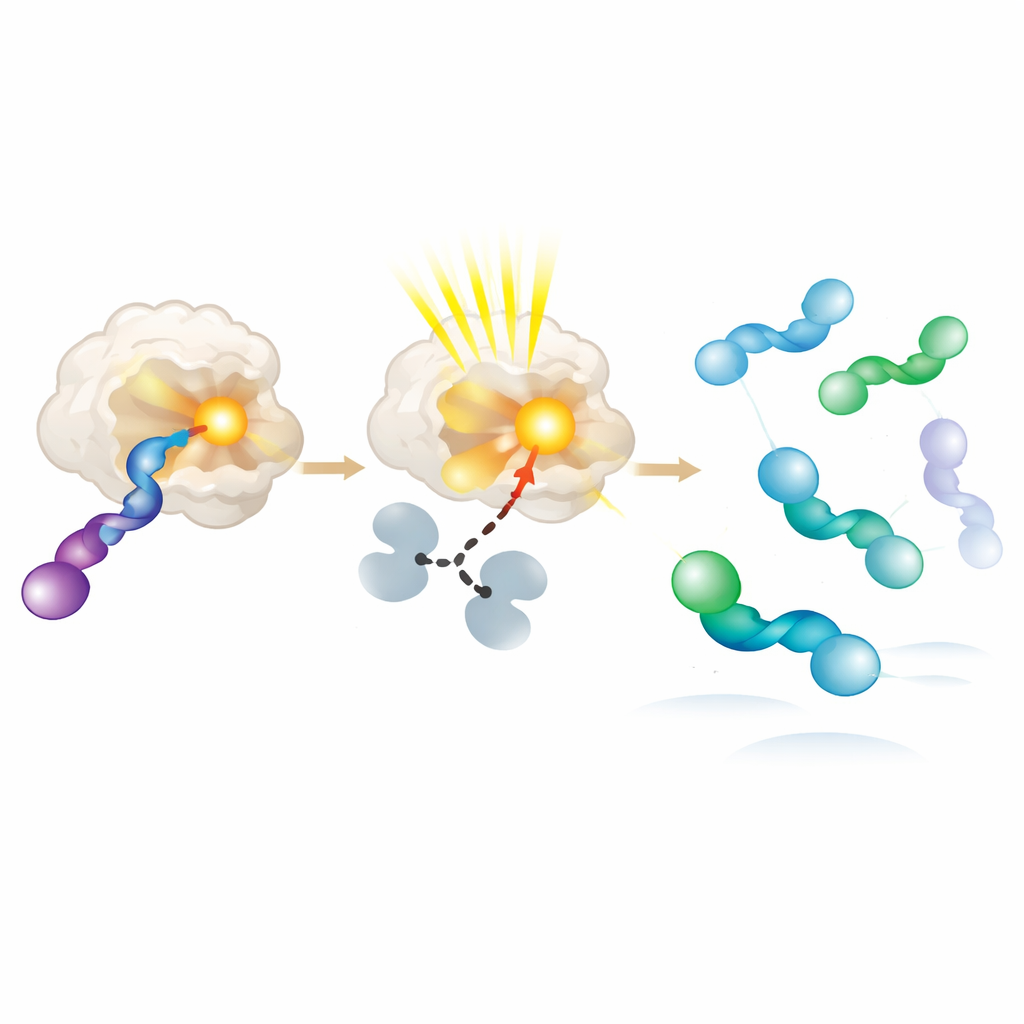
Vad detta betyder för framtidens kemi
För icke‑specialister är huvudbudskapet att teamet har skapat en programmerbar proteinkonstruktion som använder ljus för att sortera och uppgradera vridna molekyler med enastående mångsidighet. Istället för att designa en helt ny kemisk katalysator för varje mål kan forskare nu utgå från denna fotoenzymplattform och justera dess interna ficka för att acceptera många olika allener. Detta tillvägagångssätt minskar klyftan mellan naturens utsökta kontroll och den kemiska industrins behov av breda, robusta metoder. På längre sikt kan sådana ljusdrivna enzymer hjälpa kemister att framställa komplexa, enhandade byggstenar för läkemedel och material mer effektivt, med färre steg och mindre avfall.
Citering: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Nyckelord: fotoenzym, deracemisering, kiralt allen, biokatalys, tripletenergitransfer