Clear Sky Science · sv
HCMV-infektion stör barriärfunktioner och främjar epitel–mesenkymal övergång i en cholangiocyt-organoidmodell
Varför den här virus-i-levern-berättelsen är viktig
Humant cytomegalovirus är ett mycket vanligt virus som de flesta av oss bär utan att veta om det. Hos nyfödda och personer med skört immunsystem kan det dock kopplas till allvarliga lever- och gallgångsproblem, inklusive en sällsynt men förödande barndomssjukdom kallad biliär atresi. Denna studie använder miniartade, laboratorieodlade mänskliga gallgångar för att visa hur viruset direkt kan skada dessa fina rör och utlösa ärrbildande förändringar som kan bidra till att förklara länge debatterade samband mellan infektion och livslång leversjukdom.
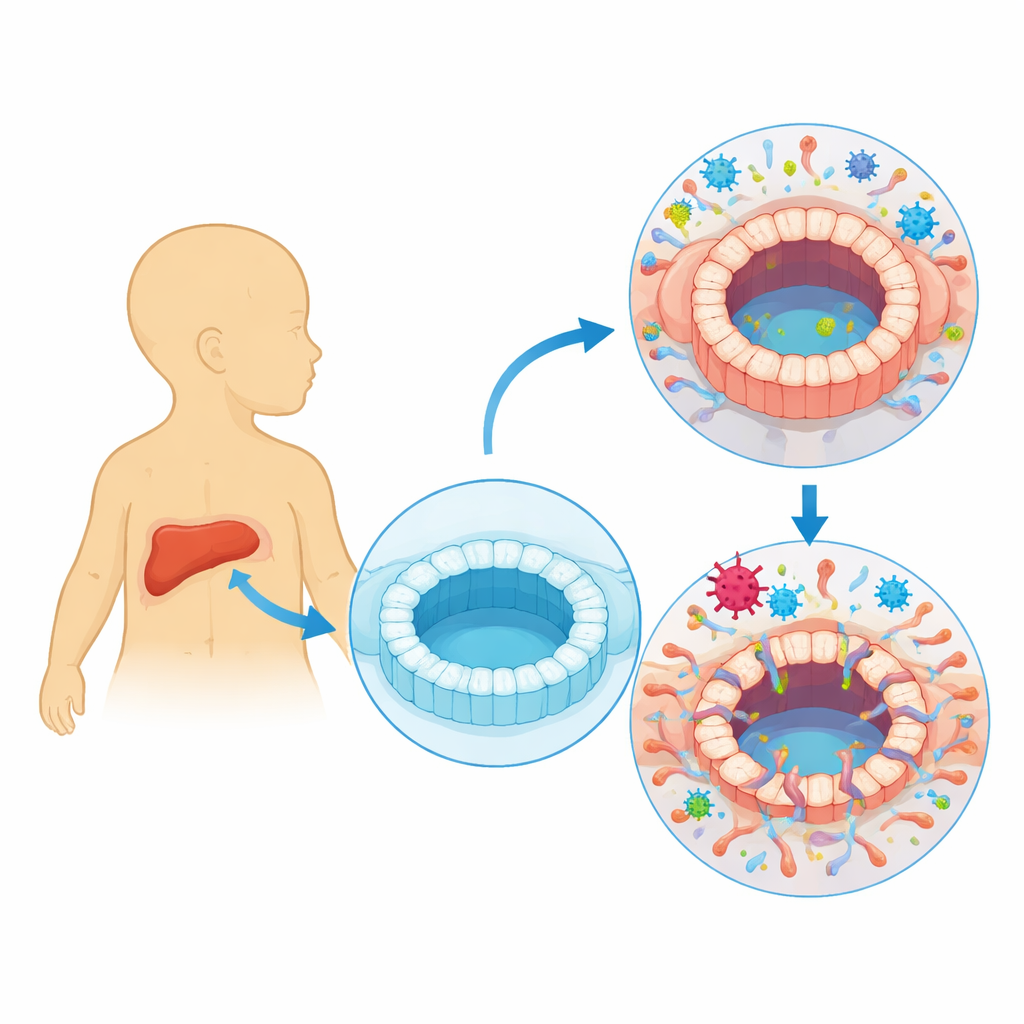
Närmare granskning av ett vanligt men tyst virus
Humant cytomegalovirus (HCMV) lever vanligen tyst i våra kroppar och växlar mellan en aktiv fas, där det bildar nya viruspartiklar, och en tyst fas, där det gömmer sig i vissa blodceller. Läkare har länge noterat att personer med tydlig HCMV-infektion kan utveckla skador på gallgångarna och kolestas, där gallflödet hindras. Många spädbarn med biliär atresi, ett tillstånd där gallgångar blir blockerade och ärriga strax efter födseln, visar också tecken på nylig HCMV-infektion. Det har emellertid varit oklart om viruset faktiskt infekterar cellerna som täcker gallgångarna eller bara är en bisittare i samband med sjukdom.
Bygga små gallgångar i en petriskål
För att besvara detta skapade forskarna tredimensionella ”organoider” som efterliknar mänskliga gallgångar. De började med inducerade pluripotenta stamceller, omprogrammerade från mänskligt blod, och styrde dem att bilda cholangiocytliknande celler—typen som bekläder gallgångarna. Dessa celler organiserade sig själva till ihåliga sfärer med ett centralt hålrum och täta cell–cell-förbindelser, vilket liknade en miniaturiserad gallgång. Teamet exponerade sedan dessa organoider för en HCMV-stam märkt med en fluorescerande markör som lyser upp när viruset replikerar aktivt. Detta gjorde det möjligt att spåra infekterade celler och mäta hur organoiderna förändrades över tid.
Hur infektion förstör struktur och försvagar barriären
När de blivit infekterade slutade organoiderna växa normalt och blev missformade, med förtjockade och oregelbundna väggar. Vissa celler glänste starkt och visade full viral aktivitet och produktion av nya viruspartiklar; andra bar virusets genetiska material på lägre nivåer, vilket antydde ett mer vilande, latensliknande tillstånd. Funktionstester visade att infekterade organoider förlorade viktiga gallgångsfunktioner. De svällde inte längre normalt som svar på en stimulans som är beroende av jontransportkanaler, och de läckte lättare i ett elektriskt resistansprov som mäter barriärtäthet. Proteiner som normalt tätar utrymmena mellan celler, såsom komponenter i tight junctions, var minskade, och transporten av ett testfärgämne in i och ut ur det inre hålrummet blev onormal. Tillsammans visar dessa förändringar att HCMV kan kompromettera gallgångsväggen direkt, göra den läckande och dysfunktionell.
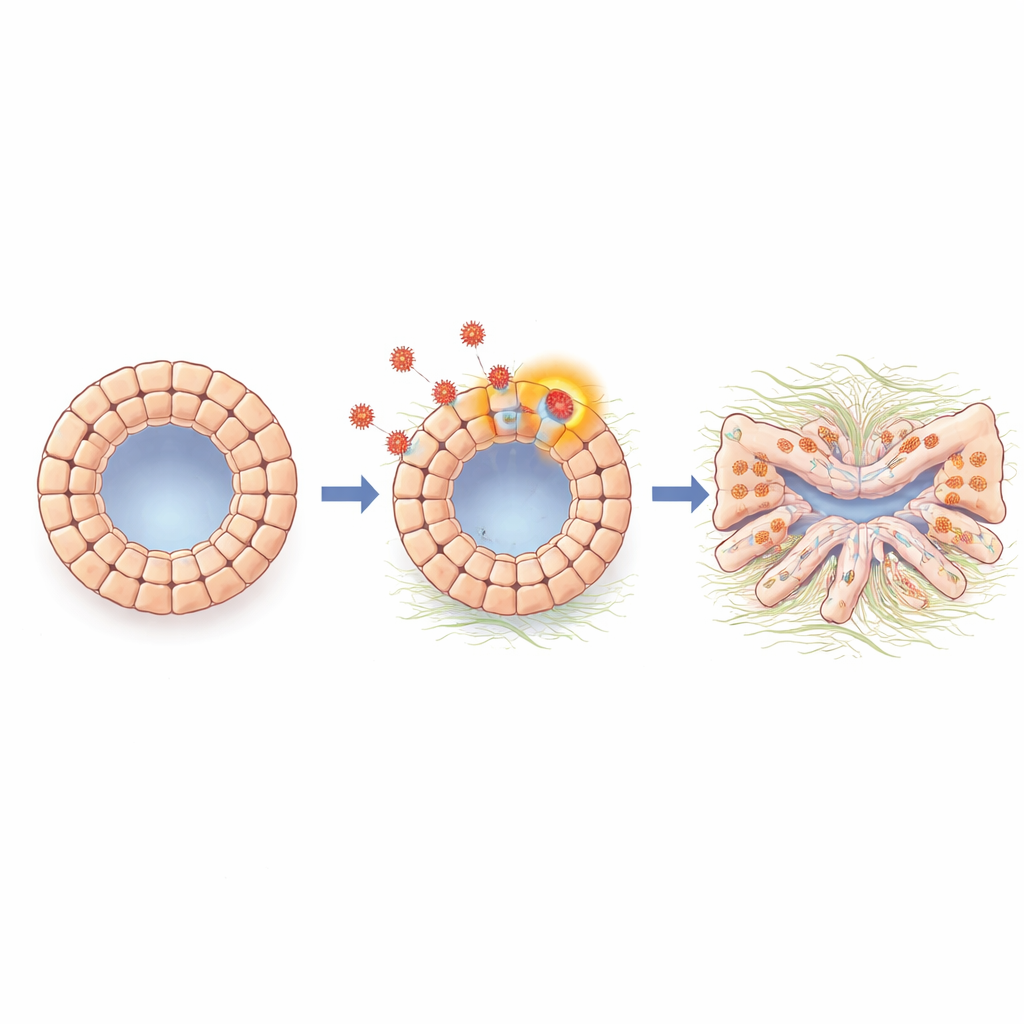
Cellerna ändrar identitet mot ett ärrbildande tillstånd
Vid en närmare analys undersökte forskarna genaktivitet i organoiderna både i bulk och på enskild cellnivå. De fann en stark aktivering av ett epitel–mesenkymalt övergångsliknande program, en process där tätt sammankopplade yt-celler lossnar från sina kontakter, antar en mer rörlig, fibrös karaktär och börjar producera molekyler kopplade till vävnadsärrbildning. Infekterade organoider visade ökade nivåer av N-kadherin och andra markörer kopplade till denna förskjutning, samt gener involverade i fibros och matrixproduktion. En signalsubstans kallad TGF-beta, välkänd för att driva ärrbildning i många organ, ökade under infektionen. När teamet blockerade TGF-beta-signaleringen med en småmolekylinhibitor eller en antikropp återgick organoiderna till en mer normal form, och många av de ärr- och övergångsrelaterade generna sjönk tillbaka mot baslinjen, vilket indikerar att TGF-beta är en viktig mellanhand som kopplar viral närvaro till skadliga cellförändringar.
Från laboratorieodlade rör tillbaka till sjuka barn
För att se om dessa laboratoriefynd relaterar till verklig sjukdom undersökte forskarna levrar från barn med biliär atresi och från andra pediatriska leversjukdomar. Med känsliga prober upptäckte de HCMV-DNA i cholangiocyter—gallgångscellerna—i ungefär två tredjedelar av proverna från biliär atresi, men långt mer sällan i icke-biliär atresi-lever. I samma områden där viralt DNA påträffades visade gallgångscellerna högre nivåer av TGF-beta och N-kadherin, vilket stämde överens med den övergångs- och ärrbildningsprofil som sågs i organoiderna. Detta tyder på att HCMV i åtminstone en del av fallen direkt infekterar gallgångsceller och skjuter dem mot ett fibrotiskt tillstånd genom att aktivera TGF-beta-drivna vägar.
Vad detta betyder för förståelse och behandling av gallgångssjukdom
Enkelt uttryckt visar detta arbete att ett vanligt virus kan invadera cellerna som klär gallgångarna, luckra upp deras täta förbindelser och driva dem mot en ärrbildande, mindre specialiserad identitet via ett TGF-beta-baserat signalspår. Dessa förändringar försvagar gångarnas barriär- och transportfunktioner och kan bidra till de blockerade, fibrotiska gallgångarna som ses vid sjukdomar som biliär atresi. Även om inte varje fall av gallgångssjukdom orsakas av HCMV, stärker studien argumentet för att viral infektion i sårbara spädbarn kan vara en viktig del av förklaringen—och att riktade insatser mot TGF-beta-relaterade vägar en dag kan hjälpa till att skydda eller återställa sköra gallgångar.
Citering: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Nyckelord: cytomegalovirus, biliär atresi, gallgångsorganoider, epitelial-mesenkymal övergång, TGF-beta-signalering