Clear Sky Science · sv
AI-baserad multiomikprofilering avslöjar kompletterande omiska bidrag till personlig förutsägelse av hjärt-kärlsjukdom
Varför det spelar roll att kunna förutsäga hjärtproblem tidigare
Hjärt-kärlsjukdom och stroke är fortfarande världens största dödsorsaker och drabbar ofta till synes friska personer utan förvarning. Läkare använder redan checklistor med ålder, blodtryck, kolesterol och rökning för att bedöma risk, men dessa verktyg kan missa många framtida patienter och överskatta risken för andra. Denna studie ställer en tidsenlig fråga: om vi går djupare in i de molekyler som cirkulerar i vårt blod och analyserar dem med artificiell intelligens, kan vi då upptäcka hjärt-kärlsjukdomar år innan de uppträder — och skräddarsy förebyggande åtgärder för varje person?
Att leta efter dolda varningssignaler i blodet
Forskarna använde UK Biobank, ett omfattande hälsoprojekt som följer hundratusentals frivilliga över många år. För en delmängd av dessa deltagare hade man noggrant mätt tusentals molekyler i blodprover: små metaboliter kopplade till fetter, sockerarter och aminosyror, samt proteiner involverade i inflammation, blodkoagulation och andra kroppsliga processer. Teamet fokuserade på sex stora kardiovaskulära tillstånd — kranskärlssjukdom, stroke, hjärtsvikt, förmaksflimmer, perifer kärlsjukdom och venösa blodproppar — för att se om dessa molekylära fingeravtryck kunde förutsäga vem som skulle utveckla vilken sjukdom.
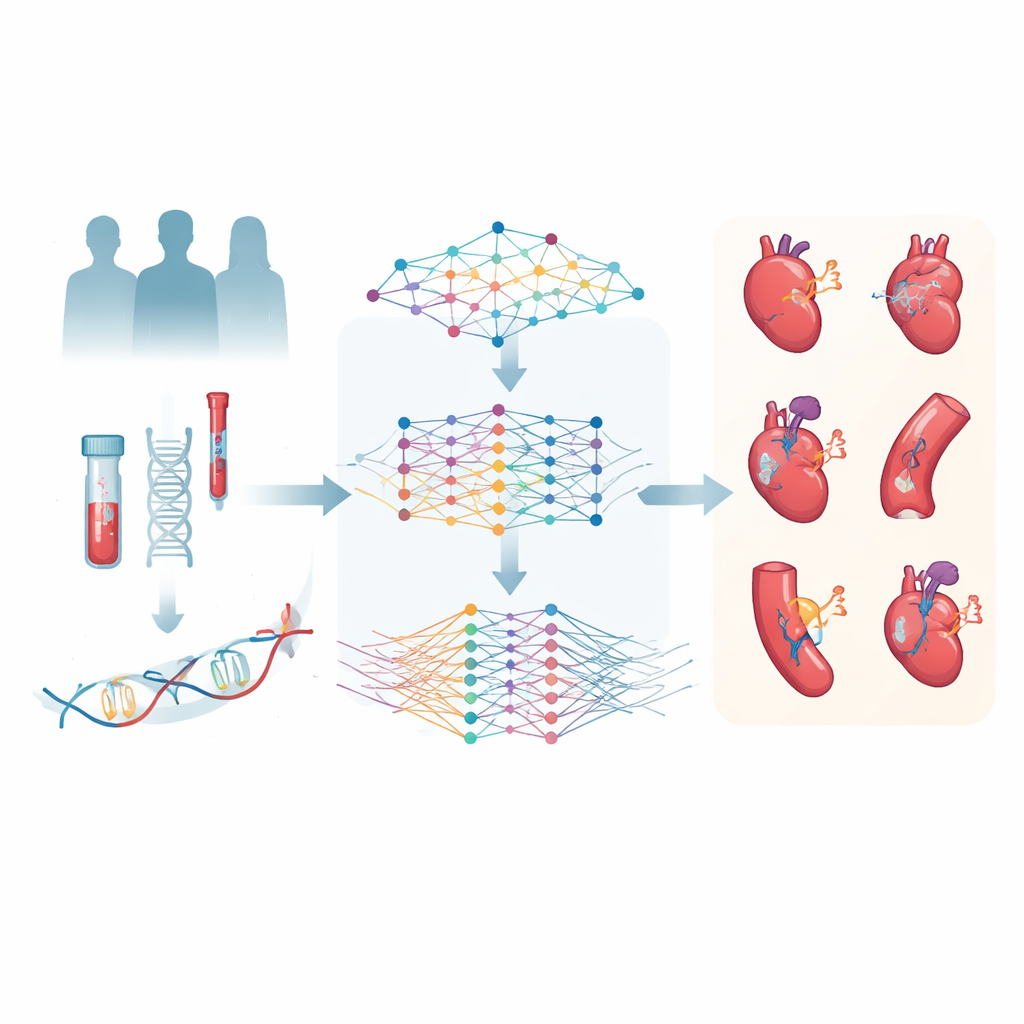
Att lära artificiell intelligens att läsa molekylära mönster
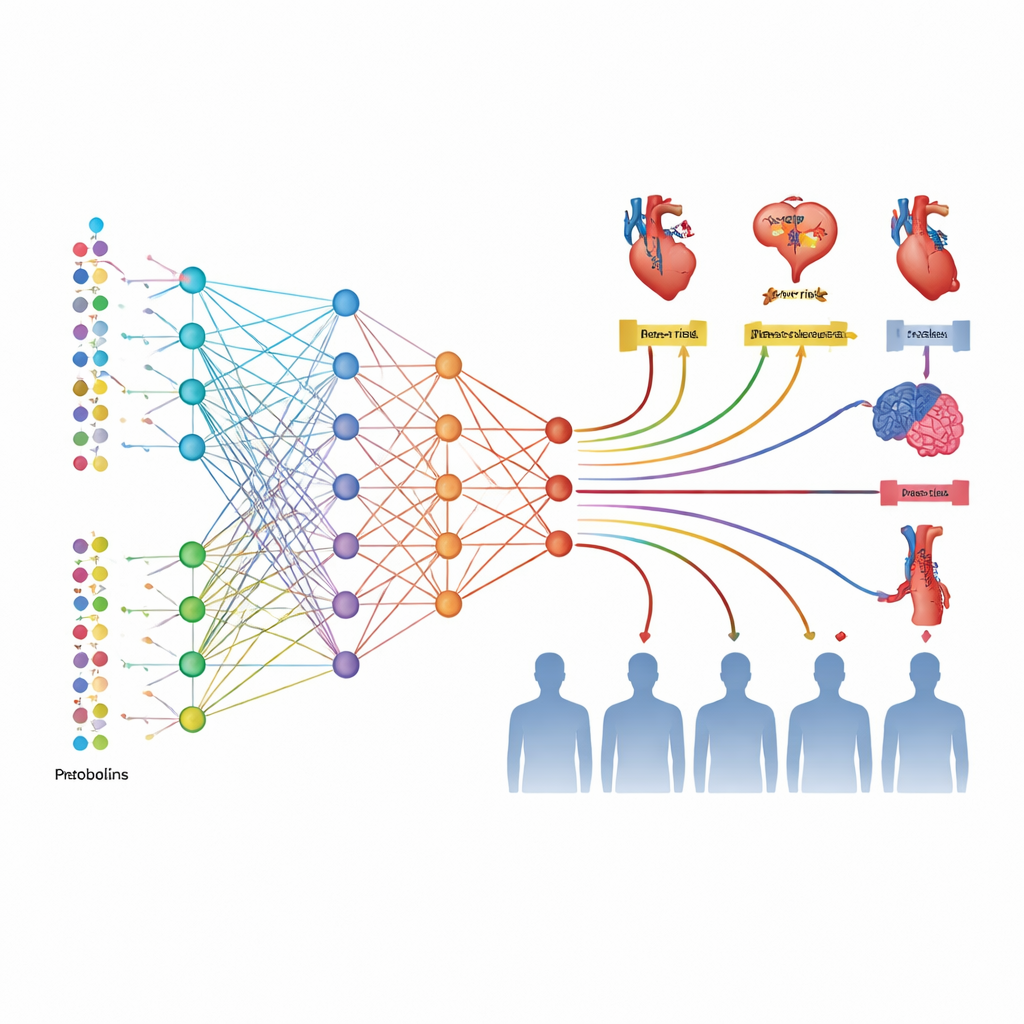
För att tolka nästan 3 000 proteiner och 168 metaboliter byggde författarna två djupinlärningsmodeller, MetNet och ProNet. Istället för att förutsäga en sjukdom i taget lärde sig dessa modeller mönster kopplade till alla sex kardiovaskulära utfall samtidigt. Från metabolitdata producerade MetNet en samlad riskscore kallad MetScore; från proteindata producerade ProNet ProScore. Varje person fick därmed sex poäng per system — en för varje typ av kardiovaskulär sjukdom — som sammanfattade miljontals möjliga molekylära interaktioner till några få tal som en standardstatistisk modell kunde använda tillsammans med ålder, blodtryck, mediciner och genetisk risk.
Hur mycket bättre är dessa molekylära riskscorer?
När teamet testade scorena i en oberoende grupp om 24 287 personer som hade alla typer av data tillgängliga, var både MetScore och ProScore starka prediktorer på egen hand och delade tydligt upp deltagarna i lågrisk-, medelrisk- och högriskgrupper över 15 års uppföljning. Proteinvärdena presterade bäst och överträffade ofta traditionella polygena (DNA-baserade) riskmått med god marginal. Att lägga till ProScore och MetScore till konventionella kliniska faktorer förbättrade träffsäkerheten i riskförutsägelsen för varje studerat kardiovaskulärt utfall, även när basmodellerna redan var detaljerade. I vissa fall, särskilt för perifer kärlsjukdom och förmaksflimmer, var förbättringen av prestanda betydande, och beslutskurvsanalyser antydde att läkare skulle kunna fatta mer gynnsamma beslut om vem som borde få förebyggande behandling.
Vad molekylerna avslöjar om sjukdomsbiologin
Utöver förutsägelse undersökte forskarna vilka specifika molekyler som var mest inflytelserika i AI-modellerna med en förklaringsmetod kallad SHAP. De bekräftade betydelsen av välkända markörer såsom kreatinin och albumin (som speglar njur- respektive allmänhälsa), liksom inflammatoriska signaler som GlycA och hjärtstressproteiner som NT-proBNP. Samtidigt framhävde modellerna mindre kända proteiner och metaboliter kopplade till inflammation, koagulation, kärlombyggnad och även nervskada, med delvis delade och delvis sjukdomsspecifika mönster. Intressant nog kunde ingen enskild molekyl matcha prediktiv kraft hos den kombinerade MetScore eller ProScore, vilket understryker att kardiovaskulär risk uppstår genom många subtila förändringar som verkar tillsammans snarare än en ensam bov.
Från stordata till mer personlig hjärtvård
Studien slutsatser är att genom att väva samman genetik, detaljerade molekylära blodprofiler och rutinmässig klinisk information kan man avsevärt skärpa vår bild av vilka som sannolikt kommer att utveckla stora kardiovaskulära sjukdomar, ofta ett decennium eller mer i förväg. Proteinanalyser tycks särskilt bära rik, handlingsbar information om pågående biologisk stress långt innan symtom uppstår. Även om de nödvändiga testerna ännu inte är vanliga eller billiga, sjunker kostnaderna, och författarna har gjort sin CardiOmicScore-metod tillgänglig som ett prototypverktyg. Med vidare validering i mer mångfaldiga populationer skulle sådan AI-driven multiomikprofilering kunna hjälpa kliniker att gå från universella checklistor till verkligt personlig förebyggande — identifiera hög-riskindivider tidigare, anpassa behandlingar efter underliggande biologi och potentiellt minska den globala bördan av hjärt- och kärlsjukdom.
Citering: Luo, Y., Zhang, N., Yang, J. et al. AI-based multiomics profiling reveals complementary omics contributions to personalized prediction of cardiovascular disease. Nat Commun 17, 2269 (2026). https://doi.org/10.1038/s41467-026-68956-6
Nyckelord: förutsägelse av kardiovaskulär risk, proteomik, metabolomik, djupinlärning, biomarkörer