Clear Sky Science · sv
RiboBright avslöjar celltyp-specifika skillnader i ribosomernas organisation och rörelse
Att se cellens proteinfabriker lysa upp
Varje sekund tillverkar varje cell i våra kroppar tusentals nya proteiner med hjälp av små maskiner som kallas ribosomer. Hittills har det varit förvånansvärt svårt att i levande celler se var dessa maskiner sitter och hur de rör sig. Denna studie presenterar RiboBright, ett litet fluorescerande molekylärt verktyg som fäster vid ribosomer och får dem att lysa, vilket gör det möjligt för forskare att följa dessa proteinfabriker cell för cell. Arbetet visar att ribosomer organiseras och används mycket olika i olika celltyper, särskilt när stamceller väljer sin framtida bana.
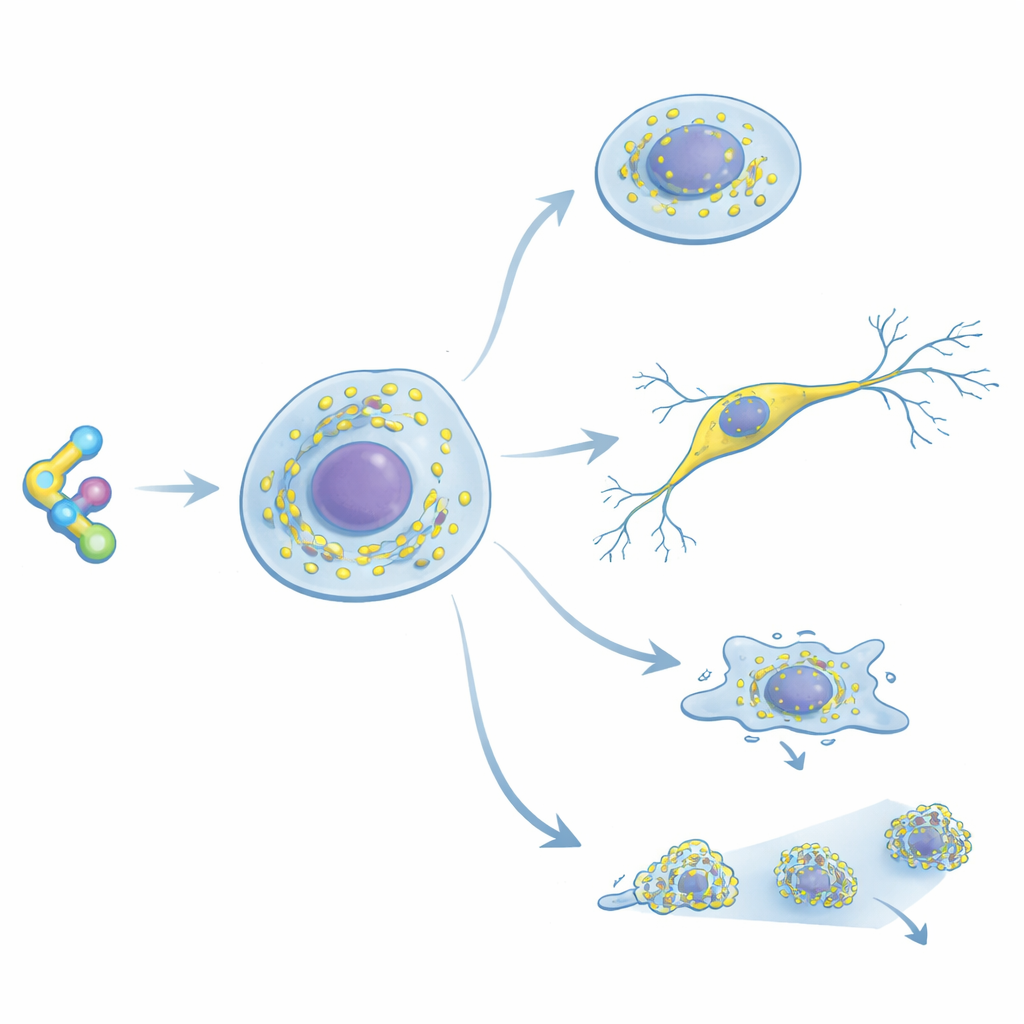
Ett nytt sätt att markera ribosomer
Forskarna konstruerade RiboBright genom att modifiera cykloheximid, ett klassiskt läkemedel känt för att binda starkt och selektivt till ribosomer hos djur och människor. De fäste en särskild ”molekylär rotor”-färg på en position på läkemedlet som inte försvagar dess grepp om ribosomen. Denna färg lyser knappt när den snurrar fritt i lösning, men blir ljusstark när dess rörelse begränsas—till exempel när proben kilas in i ribosomen. Tester i provrör visade att de modifierade molekylerna fortfarande stänger ner proteinproduktion vid nästan samma doser som originalmedlet, vilket bekräftar att de binder väl. I levande celler gav en särskild variant skarpa, ljusa prickar, vilket tyder på att den hade rätt balans mellan tät ribosombindning och stark ljusemission; denna optimerade probe döptes till RiboBright.
Bevisa att proben riktar sig mot verkliga ribosomer
För att vara säkra på att RiboBright verkligen markerar ribosomer kombinerade teamet flera kompletterande metoder. När celler förbehandlades med antingen cykloheximid självt eller en annan, orelaterad ribosom-blockerande förening, försvann RiboBright-signalen nästan helt, vilket antyder att alla tre konkurrerar om samma bindningsficka. Kemisk prövning av ribosomalt RNA visade dessutom att RiboBright skyddar samma nukleotid som cykloheximid skyddar, i linje med en identisk dockningsplats. Högupplöst mikroskopi avslöjade att RiboBright-signalen överlappar starkt med markörer för den stora ribosomala subenheten och med strukturer som det endoplasmatiska nätverket och mitokondrier, där många ribosomer finns. Samtidigt flöt några ljusa prickar fria i cytoplasman, troligen representerande rörliga ribosomer som inte sitter fast vid membraner.
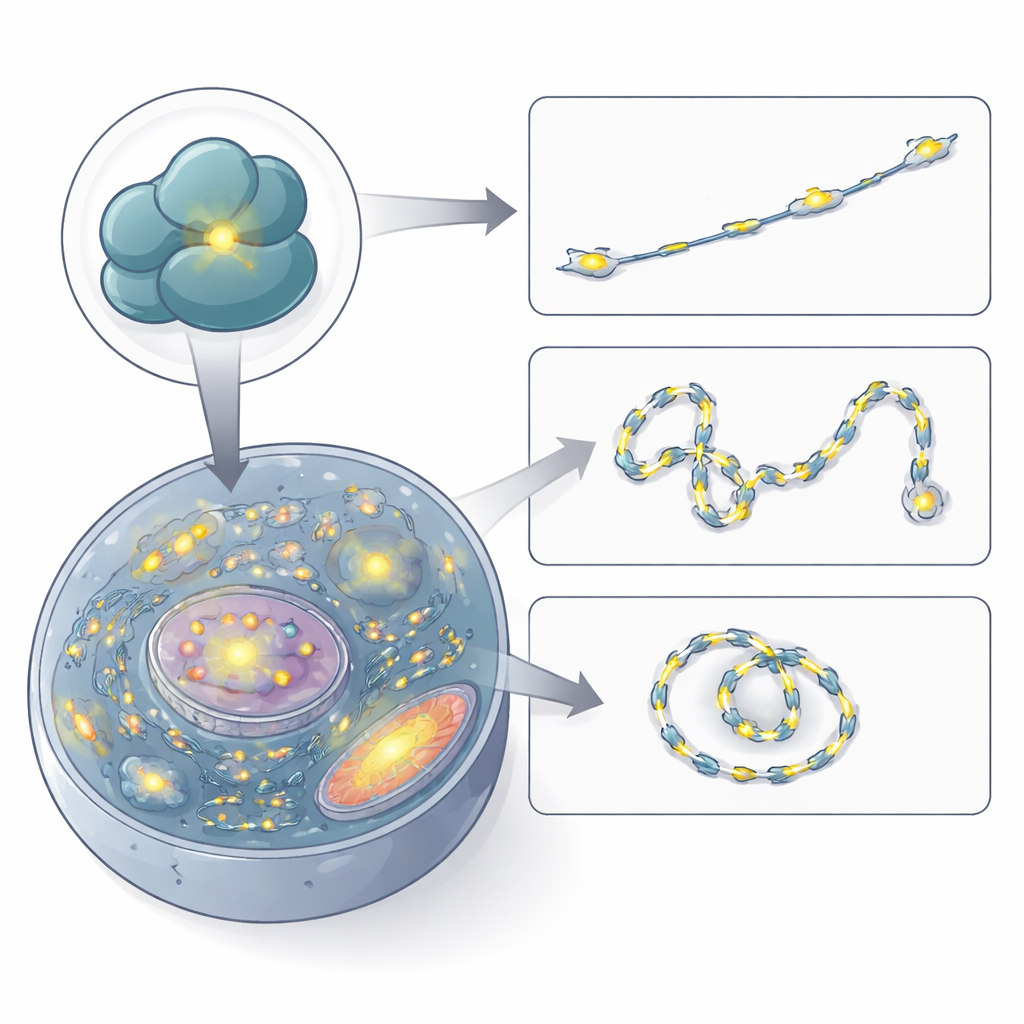
Att följa ribosomer i rörelse i levande celler
Med förtroende för dess specificitet använde författarna RiboBright för att filma ribosomer i arbete. Genom att spela in bilder med några hundra millisekunders mellanrum spårade de banorna för individuella fluorescerande prickar över cellen. Många prickar rörde sig knappt eller höll sig inom små områden, vilket tyder på ribosomer som översätter på plats på förankrade budbärar-RNA eller på det endoplasmatiska nätverket. Andra vandrade på ett slumpmässigt, diffusivt sätt, och en mindre andel visade tydlig riktad rörelse, vilket antyder aktiv transport längs cellulära spår. De hastigheter de mätte stämmer överens med tidigare uppskattningar för budbärar-RNA och ribosomkluster, vilket bekräftar att RiboBright kan fånga realistisk ribosomdynamik i realtid.
Olika celltyper, olika ribosomstrategier
RiboBright avslöjade också hur starkt ribosominnehåll och organisation beror på cellidentitet. Över tio humana och musala cellinjer, inklusive stamceller, cancerceller och icke-cancerösa celler, varierade mönstret och ljusstyrkan hos ribosomprickarna dramatiskt. Vissa celler innehöll stora, ljusa kluster som kan motsvara regioner med intensiv proteinproduktion, medan andra visade mest små, spridda prickar. Överraskande nog förutspådde inte antalet ribosomer i en cell pålitligt hur mycket protein den producerade: i de flesta celltyper visade proteinutbytet och ribosomantalet liten korrelation. Embryonala stamceller stack ut genom att ha låg produktivitet per ribosom och relativt enhetlig translation mellan enskilda celler, vilket tyder på att de upprätthåller stora reserver av underutnyttjade ribosomer samtidigt som de håller brus i proteinproduktionen lågt.
Ribosomer under tidiga celldestinationsbeslut
Teamet följde därefter mus-embryonala stamceller när de började differentiera till två tidiga linjer: en ectoderm-liknande gren och en extraembryonal endoderm (XEN)-liknande gren. Med hjälp av RiboBright tillsammans med ytmarkörer fann de att båda framväxande linjerna fick något mer totalt ribosominnehåll än odifferentierade celler, men arrangerade dessa ribosomer olika. XEN-liknande celler, som utvecklar långa utskott, visade långsammare och mer begränsad ribosomrörelse, i linje med lokaliserad proteinsyntes i specialiserade regioner. Däremot visade ectoderm-liknande celler mer rörliga ribosomer och utvecklade, efter ungefär två dagar, iögonfallande ”translationella nav” där både ribosomsignal och ny proteinsyntes nådde toppar. Under de första 72 timmarna av differentiering minskade den totala proteinproduktionen och ribosomnivåerna måttligt, men de kvarvarande ribosomerna blev något mer effektiva, särskilt i de differentierande cellerna.
Vad detta betyder för förståelsen av celler
Tillsammans ger dessa fynd en rikare bild av ribosomer som dynamiska, kontextberoende maskiner snarare än enhetliga arbetshästar. RiboBright ger forskare ett praktiskt verktyg för att visualisera och räkna ribosomer i många celltyper, i både fixerade och levande prover, och att relatera ribosomposition och rörelse till hur mycket protein en cell faktiskt producerar. För icke-specialister är huvudpoängen att celler inte bara finjusterar hur många proteinfabriker de bygger, utan också var de placerar dem och hur aktivt de körs, på sätt som beror på celltyp och utvecklingsstadium. Denna nya fluorescerande probe gör den dolda logistiken synlig och öppnar dörren för att studera hur ribosomers beteende bidrar till utveckling, sjukdom och svar på behandling.
Citering: Poulladofonou, G., Grandi, C., Hu, X. et al. RiboBright reveals cell-type-specific differences in ribosome organization and movement. Nat Commun 17, 2734 (2026). https://doi.org/10.1038/s41467-026-68947-7
Nyckelord: ribosomer, fluorescerande prober, avbildning av enskilda celler, stamcellsdifferentiering, proteinsyntes