Clear Sky Science · sv
En allosterisk hämmare av Zika‑virusets NS2B‑NS3‑proteas med oral effekt i musmodeller
Ett nytt sätt att överlista ett farligt virus
Zikaviruset slog igenom i globala nyhetsrubriker för ett decennium sedan när infektioner hos gravida kvinnor kopplades till barn födda med onormalt små huvuden och hjärnskador. Än i dag finns dock inget godkänt läkemedel för att behandla eller förebygga Zika. Denna studie beskriver en lovande ny tablettliknande förening som stänger av ett viktigt virusenzym på ett oväntat sätt och skyddar möss från svår Zikainfektion, vilket pekar mot ett framtida läkemedel som en dag skulle kunna skydda sårbara personer, särskilt under utbrott.
Varför Zika fortfarande spelar roll
Zikavirus sprids huvudsakligen av Aedes‑myggor och tillhör samma familj som dengue‑ och West Nile‑virus. De flesta infekterade känner liten eller ingen sjukdom, men ungefär en av fem utvecklar problem som sträcker sig från feber och utslag till allvarliga komplikationer såsom ögonskador, organsvikt och nervsystemsjukdomar. Den största faran gäller foster: infektion under graviditet kan leda till mikrocefali och livslång funktionsnedsättning. Eftersom det saknas godkänd vaccin eller antiviral behandling kan läkare i dag endast erbjuda stödjande vård. Forskare ser därför Zika som en prioritet för pandemiberedskap och söker läkemedel som kan användas både för att skydda riskgrupper och för att begränsa nya utbrott.
Jakt på dolda svaga punkter
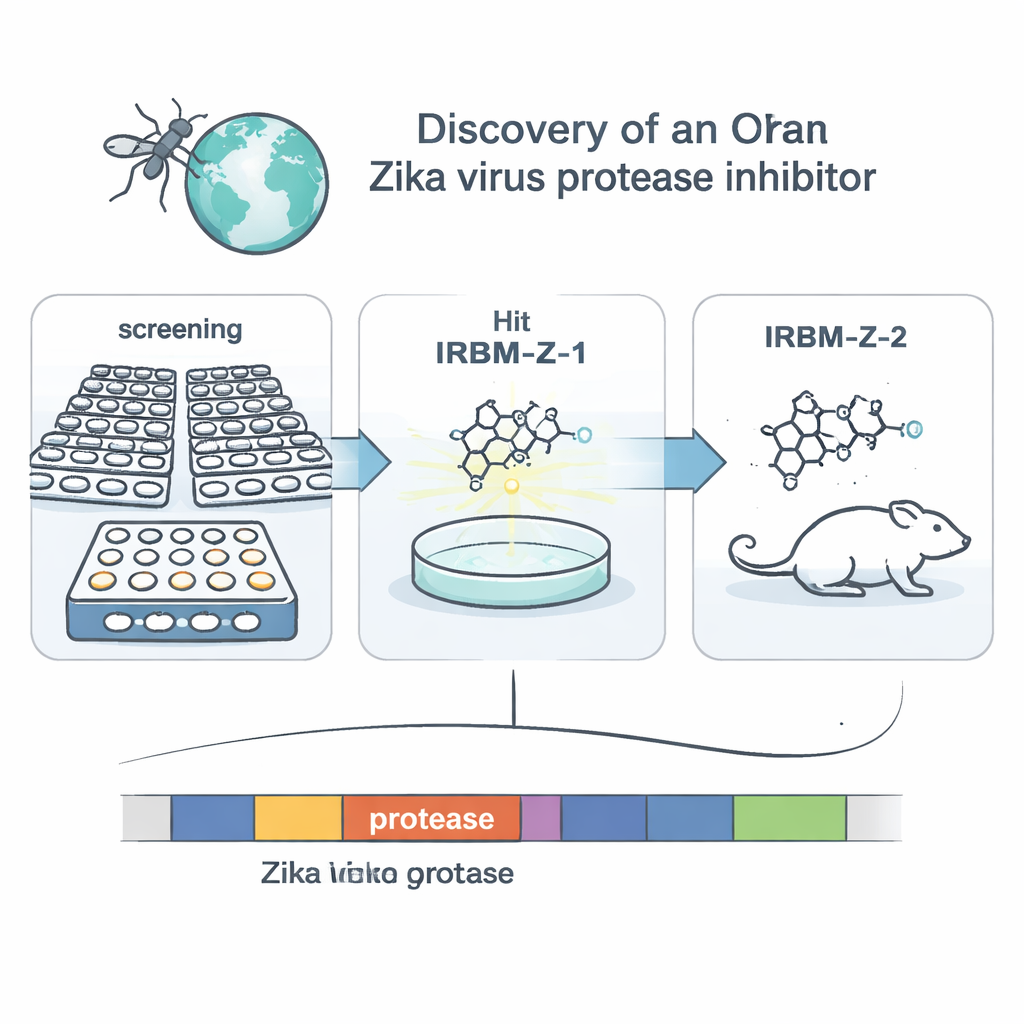
Forskarna fokuserade på ett virusenzym som kallas NS2B–NS3‑proteas. Dessa molekylära ”saxar” klyver virusets stora startprotein i de bitar som behövs för att bygga nya virus, vilket gör proteasen till ett attraktivt måltavla för läkemedel. Istället för att designa ett läkemedel mot den uppenbara klyvningsplatsen använde teamet ett cellbaserat screensystem som efterliknar Zika‑replikation i apnjursceller. De byggde ett modifierat Zika‑genom, en replikon, som saknar strukturella gener men innehåller en luciferasrapportör så att ljusutsläpp speglar viruskopiering. Efter att ha screenat mer än 120 000 småmolekyler från ett nationellt kemiskt bibliotek valde de ut de ämnen som kraftigt minskade ljussignalen utan att skada cellerna och framavlade sedan virusreplikoner som blev resistenta mot varje träff. Denna genetiska undersökning pekade ut proteasen som huvudmålet för en familj av föreningar, med en initial molekyl kallad IRBM‑Z‑1 i spetsen.
Låsa enzymet i fel form
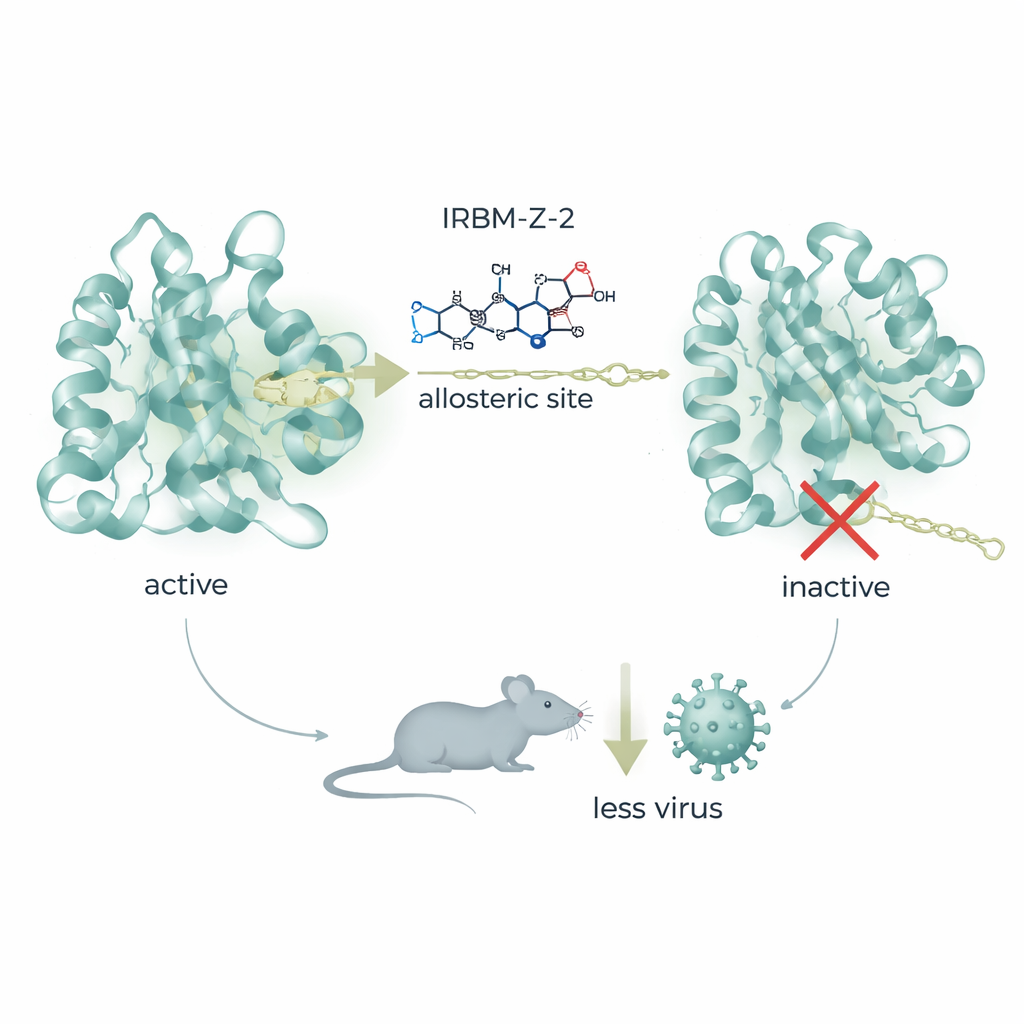
Biokemiska tester visade att IRBM‑Z‑1 inte konkurrerade med det vanliga substratet vid klyvningsstället. Istället betedde det sig som en icke‑kompetitiv, det vill säga allosterisk, hämmare—det binder i ett separat ficka och hindrar enzymet från att anta sin aktiva form. Högupplöst röntgenkristallografi visade att föreningen lägger sig i en tidigare okänd ficka långt från det katalytiska centrumet. Där bildar dess ovanliga ”N‑acylsydnon‑imin”‑kärna ett nätverk av vätebindningar och staplingsinteraktioner som pressar en nyckelregion av proteasen in i en öppen, inaktiv konformation. En enda aminosyreförändring i denna region, vid position 156, gör viruset resistent, vilket understryker hur precist föreningen utnyttjar denna dolda plats. Denna ficka skiljer sig också från allosteriska platser som beskrivits i närbesläktade flavivirus, och erbjuder därmed ett genuint nytt ingångsställe för läkemedelsdesign.
Från träff till skyddande läkemedel i möss
Vägledda av strukturella insikter förfinade teamet IRBM‑Z‑1 till en mer potent molekyl kallad IRBM‑Z‑2. Denna förbättrade förening blockerar Zika‑proteasen vid nanomolära koncentrationer, hämmar kraftfullt virusreplikation i flera celltyper och visar aktivitet mot närbesläktade dengue‑ och West Nile‑proteaser samtidigt som mänskliga enzymer skonas. I djurstudier uppvisade IRBM‑Z‑2 gynnsamma ”läkemedelslika” egenskaper: den var stabil i kroppen, hade bra oral absorption och bibehöll blodnivåer långt över dem som krävs för att stänga ner viruset, utan tydliga tecken på toxicitet. I starkt mottagliga AG129‑möss infekterade med Zika minskade daglig behandling—antingen via injektion eller peroralt—dramatiskt mängden virus‑RNA i blodet, förhindrade viktnedgång och sjukdomssymtom och gjorde att alla behandlade djur överlevde, medan obehandlade kontroller avled av infektionen.
Vad detta kan innebära för framtida utbrott
Tillsammans introducerar dessa fynd en ny klass Zika‑antiviraler som verkar genom att frysa ett kritiskt virusenzym i en inaktiv ställning i stället för att blockera dess aktiva centrum direkt. Eftersom IRBM‑Z‑2 kan ges oralt, visar starkt skydd i stränga musmodeller och hittills har en ren säkerhetsprofil, framstår den som en lovande kandidat för fortsatt utveckling som ett förebyggande läkemedel—möjligen för att skydda gravida kvinnor, vårdpersonal och resenärer om Zika återkommer. Mer generellt kan den nyupptäckta allosteriska fickan inspirera liknande läkemedel mot närbesläktade virus och öppna en ny front i kampen mot myggburna sjukdomar.
Citering: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Nyckelord: Zikavirus, antiviralt läkemedel, proteashämmare, allosterisk modulering, myggburen sjukdom