Clear Sky Science · sv
FCHo2, inte talin, möjliggör inifrån-och-ut-aktivering av integrin ɑvβ5 i böjda adhesioner
Hur celler känner formen på sin omgivning
Våra kroppar är uppbyggda av celler som ständigt griper tag i sin omgivning, drar och trycker för att förflytta sig, dela sig eller sitta kvar. Denna artikel visar att celler inte bara uppfattar hur styv deras miljö är — de läser även dess form. Genom att upptäcka ett särskilt adhesionssystem som aktiveras endast där cellmembranet är starkt böjt, visar författarna att celler använder olika inre ”grepp” för plana respektive fibrösa omgivningar, med viktiga konsekvenser för hur vävnader bildas och hur cancer sprider sig.
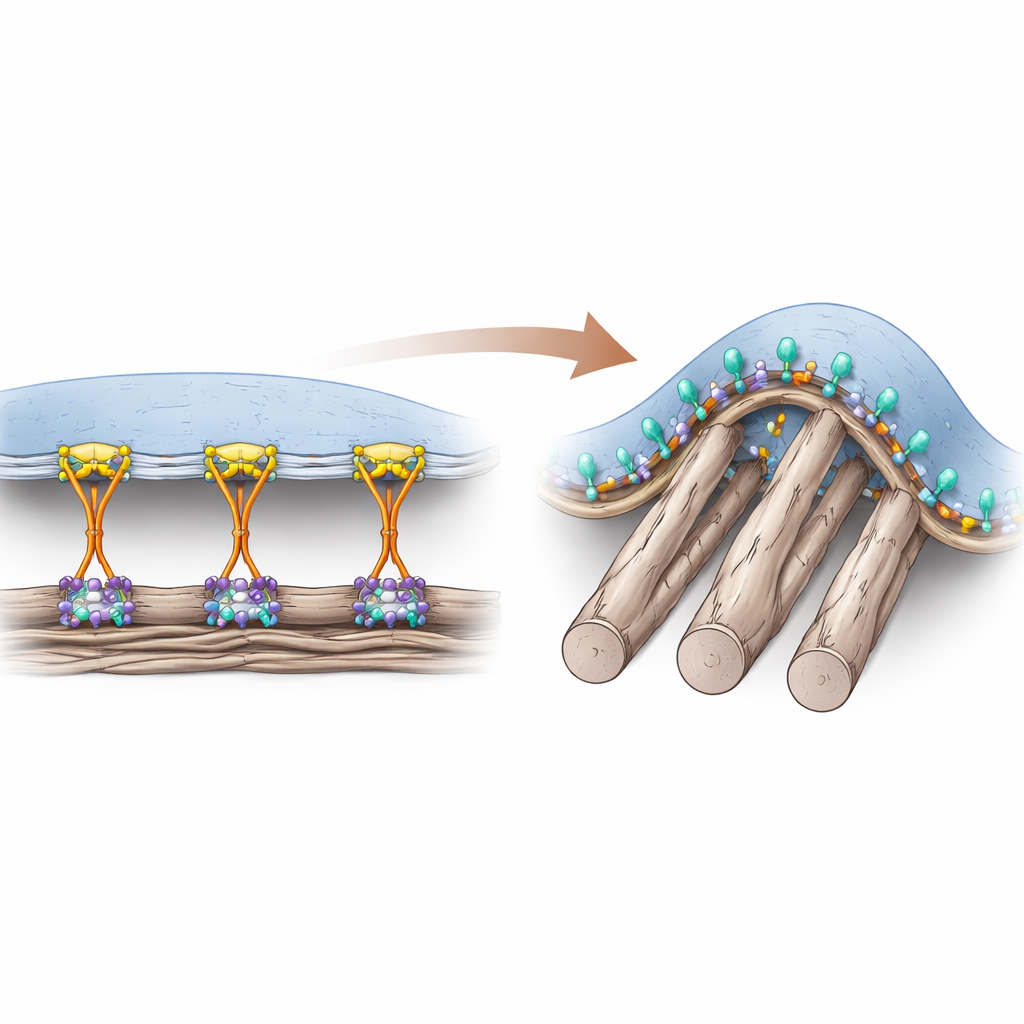
Två sätt celler håller fast
Celler fäster vid det proteinrika materialet omkring dem med hjälp av yt-receptorer som kallas integriner. Under lång tid trodde forskare att ett hjälpprotein vid namn talin var absolut nödvändigt för att slå på integriner ”inifrån” cellen, vilket möjliggör stark vidhäftning i klassiska ankare som kallas fokala adhesioner. Dessa adhesioner bildas huvudsakligen på plana, styva ytor och överför stora dragkrafter genom cellskelettet. I levande vävnader är många av de omgivande fibrerna dock mjuka och cylindriska, vilket skapar böjda kontaktpunkter som inte lätt stödjer dessa kraftkrävande strukturer. Författarna fann tidigare en annan typ av adhesiv struktur, kallad böjd adhesion, som uppstår precis där membranet böjs runt tunna fibrer och som förlitar sig på ett specifikt integrin, αvβ5.
Böjda grepp använder en annan hjälpare
I den nya studien visar teamet att talin, trots att det fortfarande finns närvarande, inte är den avgörande aktivatorn av integrin αvβ5 i böjda adhesioner. Istället tar ett kurvaturkännande protein kallat FCHo2 över denna uppgift. Genom att använda precist konstruerade nano-stora stänger och pelare för att böja cellmembran på kontrollerade sätt observerade de att αvβ5 klustrar starkt vid böjda regioner, men endast när FCHo2 kan binda till en mycket kort sekvens — ett HDRRE-motiv — precis inuti cellen på β5-svansen. När detta motiv störs fungerar integrinet fortfarande i fokala adhesioner men kan inte längre bilda böjda adhesioner. Nedsättning av FCHo2 lämnar de klassiska fokala adhesionerna i stort sett intakta men utplånar de böjda adhesionerna, medan avlägsnande av talin kraftigt försvagar fokala adhesioner men lämnar de böjda adhesionerna i stort sett opåverkade.
En enda aminosyra som formväljare
En gåta var varför ett nära besläktat integrin, αvβ3, inte kan bilda böjda adhesioner trots att dess inre svans ser väldigt lik ut den hos β5. Genom att byta domäner mellan de två integrinerna och införa punktmutationer identifierade författarna en enda avgörande position nära talin-bindningsstället: de flesta β-integriner har en tryptofan (W), men β5 har unikt en tyrosin (Y766). När β5:s tyrosin ersattes med tryptofan förlorade integrinet sin förmåga att delta i böjda adhesioner och uppförde sig mer som β3, med en preferens för enbart fokala adhesioner. Den omvända förändringen — att sätta tyrosin i den β3-liknande chimären — återställde känsligheten för kurvatur. Ytterligare experiment med varianter som efterliknar fosforylerade eller icke-fosforylerade tillstånd av denna tyrosin tyder på att dess kemiska modifiering kan styra integrinet mot antingen plana, högkraftiga fokala adhesioner eller böjda, lågkraftadhesioner.
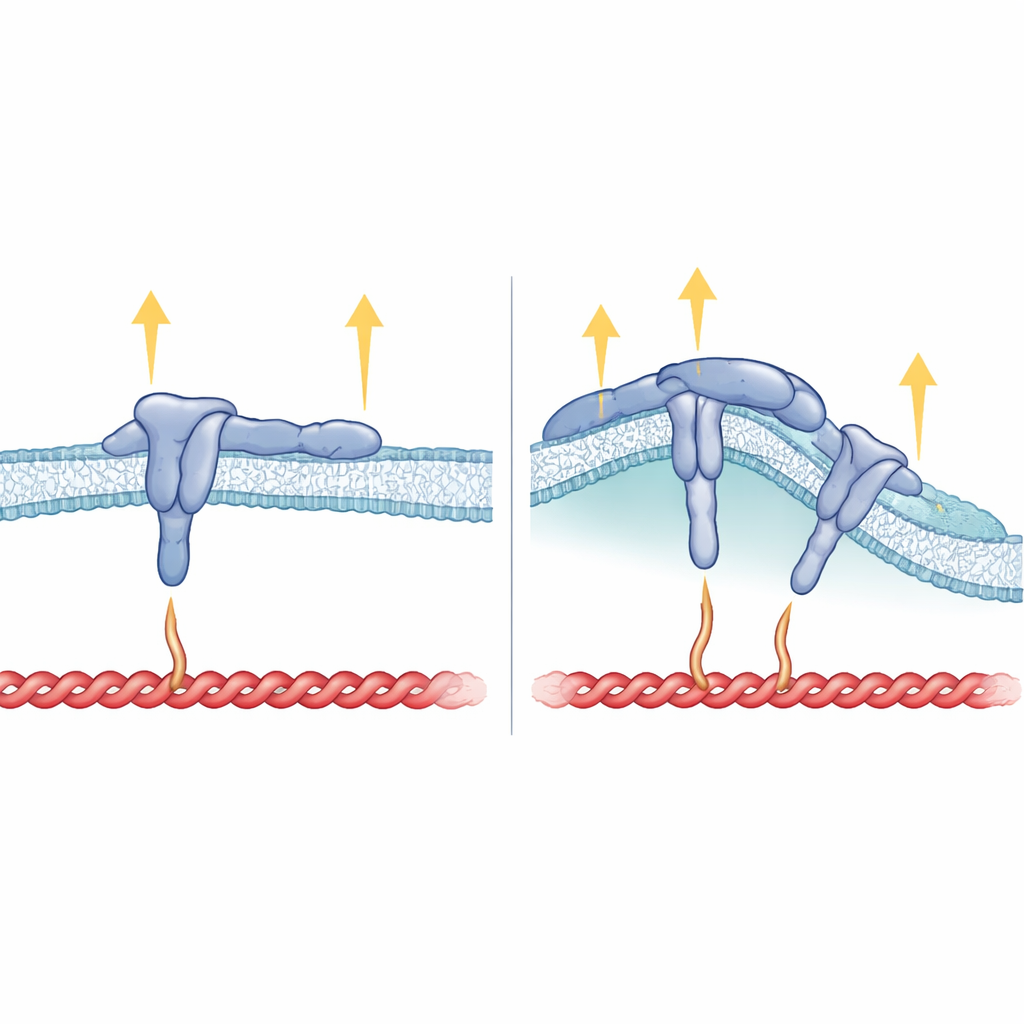
Hur membranform, integrinstruktur och kraft hänger ihop
Bortom den inre svansen visade sig också den del av β5 som går genom membranet vara kritisk. När forskarna bytte ut β5:s transmembrana segment mot det från β3 kunde det resulterande integrinet fortfarande bilda fokala adhesioner men föredrog inte längre böjda platser eller följa FCHo2. Detta tyder på att hur integrinet sitter i membranet hjälper till att orientera HDRRE-motivet så att FCHo2 kan haka i vid böjda regioner och stabilisera ligandbundna, aktiva αvβ5. I böjda adhesioner verkar talin endast röra vid en mer avlägsen del av integrinsvansen och utsätts inte för hög spänning, vilket förklarar varför andra kraftälskande komponenter som vinculin, tensin och kindlin i stor utsträckning saknas där. I kontrast griper talin i fokala adhesioner både närliggande och mer avlägsna platser på svansen och membranet, vilket stöder starka dragkrafter men blockerar FCHo2 från att nå samma region.
Vad detta betyder för cellbeteende
För en lekmannaögon är budskapet i detta arbete att celler har två separata ”greppslägen” för att fästa vid sin omgivning. På plana, styva områden använder de talin-drivna fokala adhesioner som är byggda för att dra hårt. På mjuka, fibrösa och böjda strukturer växlar de till FCHo2-drivna böjda adhesioner som stabiliserar integrin αvβ5 med avsevärt lägre kraft. En liten förändring i integrinets sekvens — och om denna plats är kemiskt modifierad — hjälper till att avgöra vilket läge som används. Detta dubbla system låter celler tolka både styvhet och form i tredimensionella miljöer, vilket påverkar hur de migrerar, organiserar vävnader och potentiellt hur de invaderar vid sjukdom.
Citering: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Nyckelord: integriner, celladhesion, membranets kurvatur, FCHo2, cytoskelett