Clear Sky Science · sv
En experimentellt informerad polymermodell avslöjar genomiska lokiers organisation i hög upplösning
Hur DNA-veckning formar cellidentitet
Varje cell i din kropp bär i huvudsak samma DNA, men nervceller, hudceller och stamceller beter sig mycket olika. En viktig orsak är hur DNA:t veckas och packas i kärnan. Denna studie introducerar ett nytt sätt att ”se” den veckningen i påtaglig detalj och knyter den fysiska ordningen av DNA till om viktiga gener är på- eller avstängda. Genom att förena experiment med fysikbaserade datorsimuleringar avslöjar författarna dolda kluster av genetiskt material som verkar fungera som grundläggande byggstenar i genomorganisationen.
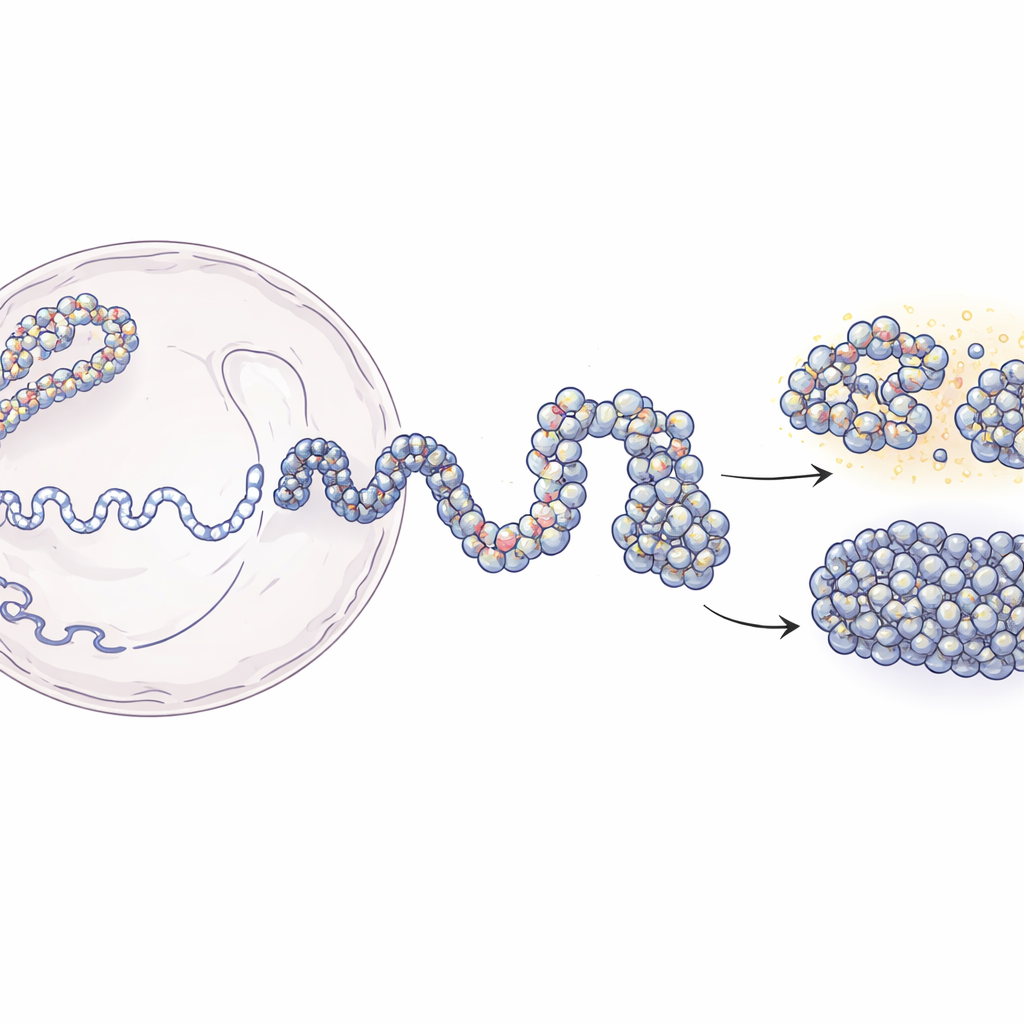
Från långa DNA-trådar till 3D-kartor över genomet
I kärnan är DNA lindat runt proteinspolar kallade nukleosomer och bildar en pärlbandlik struktur som kallas kromatin. Moderna tekniker som Hi-C och Micro-C kan tala om vilka DNA-delar som ligger nära varandra i 3D, men de ger ofta suddiga, populations‑genomsnittliga ögonblicksbilder. Å andra sidan ger experiment som lokaliserar enskilda nukleosomer skarp lokal detalj men liten uppfattning om den större strukturen. Detta arbete överbryggar den klyftan. Författarna utgår från lågupplösta kontaktkartor som rapporterar hur ofta avlägsna DNA-sekvenser rör varandra, och kombinerar dem med experimentella kartor över nukleosompositioner. Med principer från polymerfysik bygger de simulerade 3D-ensemblear av kromatin som stämmer med experimentella data men ändå upplöses ned till några tiotals DNA-bokstäver.
En tvåstegsstrategi för att rekonstruera kromatin
Modelleringsansatsen utvecklas i två huvudsteg. Först använder teamet Hi-C-data för att generera många möjliga storskaliga former av ett 200 000‑bokstävers långt DNA‑område, där kromatinet behandlas som en flexibel kedja där 5 000‑bokstavssegment försiktigt styrs att göra eller undvika kontakter enligt experimenten. Dessa grova strukturer fångar det övergripande veckmönstret som cellens proteiner hjälper till att skapa. I andra steget ersätts varje stort pärlsegment av en mycket finare kedja bestående av individuella nukleosomer och de korta DNA‑länkarna mellan dem. Nukleosomernas positioner kommer från en enzymbaserad kartläggningsmetod (MNase‑seq) som visar var de typiskt sitter längs genomet. De finare kedjorna får sedan veckas samtidigt som de fortfarande respekterar den bredare arkitekturen. När forskarna ”suddar” sina högupplösta modeller tillbaka till experimentell upplösning, reproducerar de både Hi‑C‑ och Micro‑C‑kontaktkartor med hög noggrannhet.
Upptäckten av nukleosom‑blobs som strukturella enheter
När författarna zoomade in på sina simulerade strukturer framträdde ett slående mönster: nukleosomerna var inte jämnt fördelade utan samlades i oregelbundna kluster, som författarna kallar nukleosom‑blobs. Dessa blobs liknar de klumpiga strukturer som tidigare setts i superupplösningsmikroskopibilder av verkliga celler. Genom att analysera många tusen simulerade ögonblicksbilder visade gruppen att dessa blobs är förlängda, inte sfäriska, och typiskt innehåller flera tätt packade nukleosomer. Viktigt är att kontakter inom dessa blobs överensstämmer väl med de domänlika interaktionsblock som ses i experimentella data, vilket indikerar att blobs inte är slumpmässiga utan fundamentala 3D‑enheter i kromatinorganisationen. Simuleringarna förutspår till och med ytterligare subtila domängränser som är svåra att upptäcka experimentellt, vilket tyder på att denna fysiska modell kan avslöja finkorniga funktioner dolda i brusiga data.
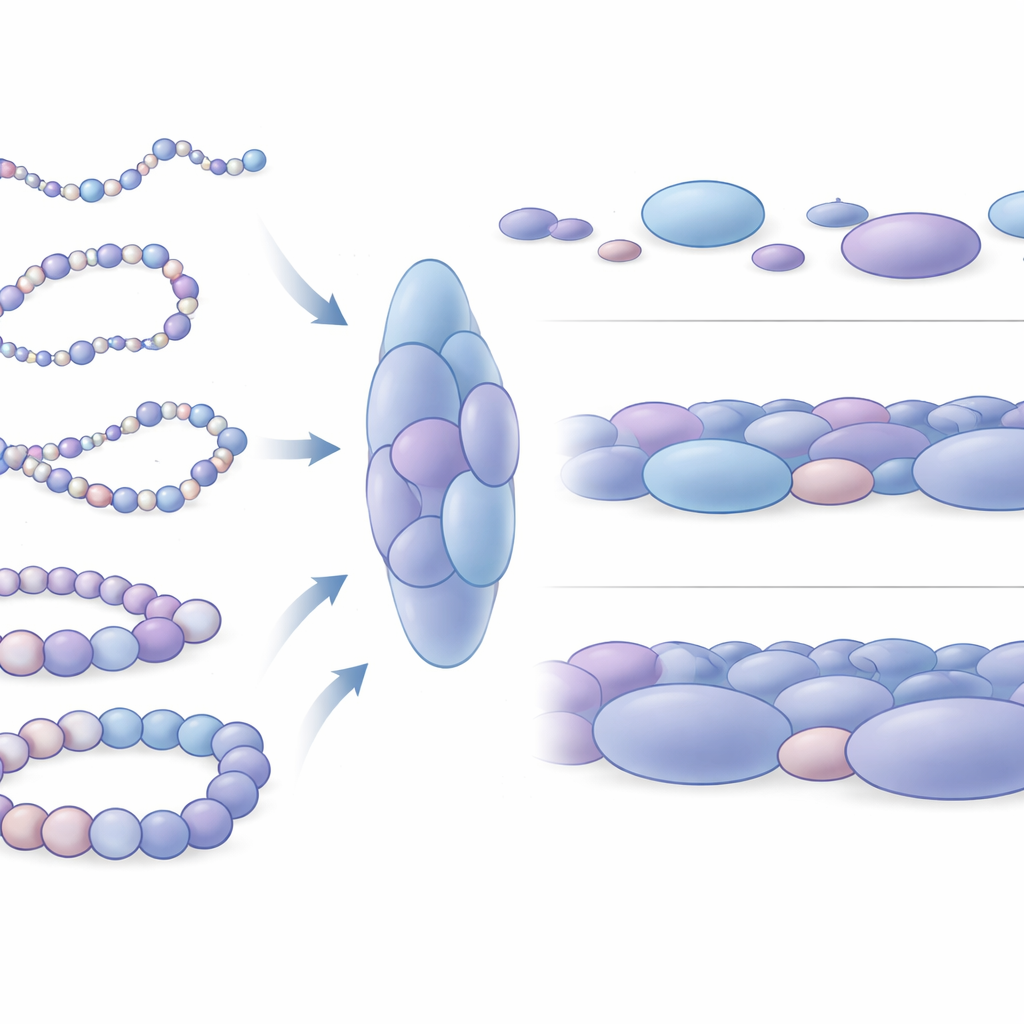
Hur packningsskillnader speglar genaktivitet
Forskarna undersökte sedan hur dessa blobs skiljer sig runt gener som är aktiva jämfört med de som är tysta. De fokuserade på fyra välstuderade mänskliga DNA‑sträckor, inklusive två gener som hjälper stamceller att hålla sig flexibla och odifferentierade (Nanog och Lin28A) och två utvecklingskontrollgener (HoxB4 och HoxA13) som är avstängda i samma celler. Runt de inaktiva generna var blobs i genomsnitt större och tätare packade, med nukleosomer som bildade mer helt slutna lokala arrangemang. I kontrast var blobs nära aktiva gener mindre, något lösare och mer varierade. I ett bredare perspektiv provade DNA runt aktiva gener många fler distinkta former och var mekaniskt mer böjligt, medan regioner runt tysta gener uppträdde som styvare kromatinsegment. Denna mekaniska skillnad påverkar sannolikt hur lätt avlägsna regulatoriska DNA‑element kan mötas och samarbeta med genreglage.
Varför detta betyder något för förståelsen av genkontroll
Tillsammans målar resultaten upp en bild där genomet byggs av dynamiska kluster av nukleosomer vars storlek, form och inbördes avstånd bidrar till om närliggande gener är åtkomliga eller inlåsta. Den nya modellen förenar experimentella kontaktdata, nukleosomkartor och fysikaliska principer i ett enda ramverk som förklarar hur stamcellsgener kan förbli flexibla och interaktiva medan utvecklingsgener förblir isolerade i styvare, mer kompakta kvarter. För icke‑specialister är huvudidén att genaktivitet inte styrs enbart av DNA‑sekvensen; den beror också på hur DNA:t veckas i tredimensionella strukturer. Genom att avslöja nukleosom‑blobs som byggstenar i denna veckning erbjuder arbetet en kraftfull väg att koppla mikroskopisk genomarkitektur till storskaliga processer som utveckling, cellidentitet och sjukdom.
Citering: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Nyckelord: kromatinveckning, nukleosomkluster, 3D-genomorganisation, genreglering, polymermodellering