Clear Sky Science · sv
Klonal expansion av cytotoxiska CD8⁺ T‑celler vid lecanemab‑associerad ARIA
Varför detta är viktigt för personer med Alzheimer
Lecanemab är ett av de första läkemedlen som kan avlägsna amyloid från hjärnan och måttligt bromsa minnesförlust vid Alzheimers sjukdom. Men vissa patienter som får denna behandling utvecklar hjärnsvullnad eller små hjärnblödningar, förändringar som syns i magnetkameraundersökningar och grupperas under begreppet amyloid‑relaterade bildgivningsavvikelser (ARIA). Denna studie ställer en avgörande fråga för patienter och anhöriga: vad händer i immunsystemet när ARIA uppträder, och kan ett enkelt blodprov en dag hjälpa till att förutsäga vem som löper störst risk?
Löftet och risken med en ny Alzheimer‑behandling
Lecanemab är en antikropp som ges via infusion och riktar sig mot klumpar av proteinet amyloid‑beta, ett kännetecken för Alzheimers sjukdom. Genom att hjälpa kroppen att rensa bort amyloid kan den måttligt sakta kognitiv försämring. Men denna nytta följer med en säkerhetsaspekt: vissa personer utvecklar ARIA, vilket kan omfatta områden med hjärnsvullnad eller finstilta blödningar. Dessa biverkningar kräver frekvent MR‑övervakning och kan begränsa vilka som får läkemedlet. Inte alla är lika sårbara—bärare av en genvariant kallad APOE4 har högre risk—men gener ensam förklarar inte varför ARIA uppstår, särskilt tidigt efter behandlingsstart. Eftersom lecanemab ges via blodbanan resonerade författarna att en noggrann granskning av immunceller i blodet kanske kan avslöja tidiga varningstecken eller till och med mekanismer som kopplar behandlingen till vaskulär skada i hjärnan. 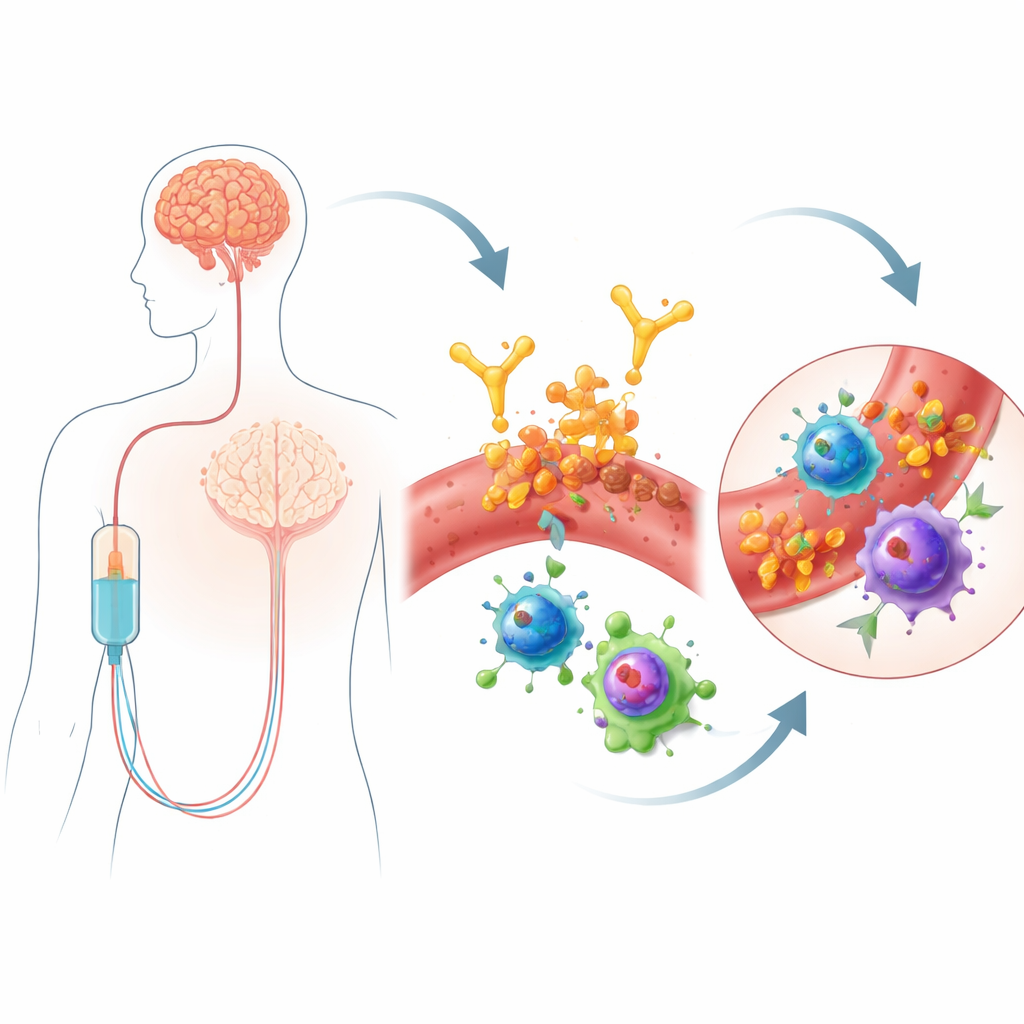
Spåra immunceller hos patienter som utvecklade respektive inte utvecklade ARIA
Forskarna studerade sex personer med Alzheimer som fick lecanemab på en regional minnesmottagning. Tre utvecklade olika former av ARIA, och tre matchade patienter (lika i ålder, kön, APOE‑genotyp och antal infusioner) gjorde det inte. Blod togs strax före infusionerna, och teamet använde en intensiv "multi‑omisk" metod: enkelcells‑RNA‑sekvensering för att läsa vilka gener som var aktiva i tusentals individuella immunceller, antikroppsbaserade taggar för att definiera celltyper, sekvensering av T‑cellreceptorer för att spåra kloner, och riktad metabolomik för att mäta hundratals små molekyler som ingår i cellmetabolism. Detta tillät dem att fråga inte bara vilka celltyper som var närvarande, utan hur aktiva de var, vilket bränsle de använde och om specifika T‑cellsfamiljer expanderade som svar på någon utlösare.
Expansion av starkt beväpnade mördarceller (T‑celler)
Ett tydligt mönster framträdde hos patienterna som utvecklade ARIA. Jämfört med kontroller hade de en högre andel CD8 "mördarceller" och färre CD4‑hjälparceller. Inom CD8‑poolen utmärkte sig två undergrupper: effektorminnesceller och en terminalt differentierad form känd som TEMRA‑celler. Dessa TEMRA‑celler liknar veteran‑soldater—högspecialiserade för anfall, med kraftfull maskineri för att döda målceller. Hos ARIA‑positiva patienter var TEMRA‑cellerna fler, mer klonalt expanderade (vilket innebär att särskilda T‑cellsfamiljer hade multiplicerats) och bar genprogram kopplade till cytotoxicitet, migration genom blodkärl och tecken på kronisk stimulering. Liknande T‑cellsstatus har observerats vid åldrande, kroniska infektioner, multipel skleros och i ryggvätskan hos personer med Alzheimer, där de kan ackumuleras nära blodkärl och hjärnans yta.
Metabol omkoppling och korsprat med andra immunceller
Teamet fann också att dessa CD8‑effektor‑celler hade omkopplat sin metabolism. Istället för att i första hand förlita sig på effektiv energiproduktion i mitokondrierna, skiftade de mot glykolys, ett snabbare men mindre effektivt sätt att generera energi som stöder kortlivad, högintensiv aktivitet. Metabolitmätningar i blodceller bekräftade detta: nivåerna av laktat och pyruvat var ökade, medan nyckelkomponenter i citronsyracykeln var minskade, ett mönster typiskt för inflammatoriska immunceller. Monocyter, en annan typ av vita blodkroppar, visade kompletterande förändringar. Hos ARIA‑positiva patienter slog monocyter på gener för antigenpresentation, vidhäftning till andra celler och produktion av kemokiner—kemiska signaler som attraherar T‑celler. Beräkningsmodeller av ligand‑receptor‑par antydde att monocyter skickade starkare aktiverande och hemmapositionssignaler till CD8‑effektorceller, vilket skapade en miljö som uppmuntrar dessa mördarceller att engagera blodkärlsväggar.
Adresskoder som pekar T‑celler mot hjärnans kärl
Eftersom denna studie endast provtog blod vände sig författarna till en oberoende enkelcellsdatamängd från hjärnor hos lecanemab‑behandlade patienter för att undersöka om samma T‑cellsprogram är kopplade till vaskulära nischer i hjärnan. När de projicerade sina CD8‑undergrupper på denna hjärnkarta visade TEMRA‑ och effektorminnescellerna från ARIA‑positiva patienter transkriptionella "adresskoder"—kombinationer av adhesionsmolekyler och kemokinreceptorer—som matchade endotelceller (blodkärlsceller) i den sjukliga hjärnan. Dessa signaturer tyder på att de expanderade mördarcellerna inte bara är starkt beväpnade och metabolt uppdrivna, utan också primade för att ta sig till och interagera med stressade hjärnblodkärl vid platser för amyloidrensning. 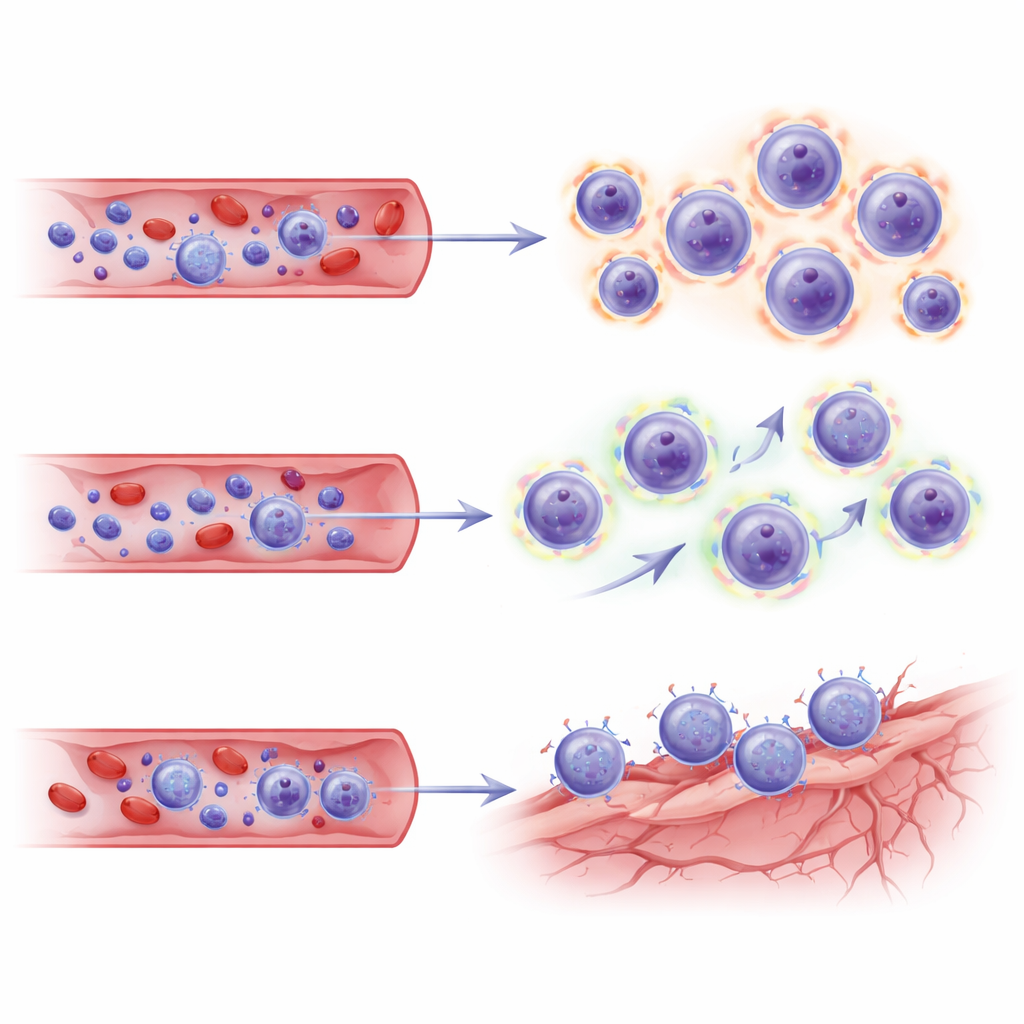
Vad detta kan betyda för patienter och framtida vård
Sammantaget skildrar denna lilla men detaljerade studie ARIA som mer än en passiv bieffekt av amyloidrensning. I stället verkar det vara kopplat till ett koordinerat immunsvar i blodet: expansion och metabol aktivering av specifika mördarcells‑kloner, förstärkt signalering från monocyter och molekylära drag som gynnar engagemang med hjärnans blodkärl. Arbetet bevisar inte att dessa celler orsakar ARIA—immunsvar kan vara en reaktion på vaskulär skada snarare än dess källa—men det ger testbara hypoteser och en ritning för blodbaserade biomarkörer. I framtiden kan mätning av förekomst och metabolt tillstånd hos CD8 TEMRA‑celler, tillsammans med nyckelsignalmolekyler, hjälpa till att identifiera patienter med högst risk för ARIA, styra övervakningsscheman eller till och med inspirera riktade strategier för att tillfälligt dämpa detta immunsvar samtidigt som fördelarna med amyloid‑rensande terapier bevaras.
Citering: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Nyckelord: Alzheimers sjukdom, lecanemab, immunceller, hjärnans blodkärl, biverkningar av behandling