Clear Sky Science · sv
TMEM63-proteiner fungerar som mekaniskt aktiverade kolesterolmodulerade lipid-skramblasar som bidrar till membranets mekaniska motståndskraft
Hur celler förblir intakta vid fysisk påfrestning
Våra kroppars celler pressas, sträcks och skakas ständigt, vare sig i ett bultande hjärta, i arbetande muskler eller i tumörer som tränger genom vävnad. Denna studie kartlägger hur en familj membranproteiner, kallade OSCA/TMEM63, hjälper celler att överleva sådana hårda mekaniska krafter genom att omfördela fetterna i deras yttre skal. Att förstå detta inbyggda stötdämpningssystem kan ge nya insikter i sjukdomar som påverkar hörsel, nervisolering och även spridning av cancer.
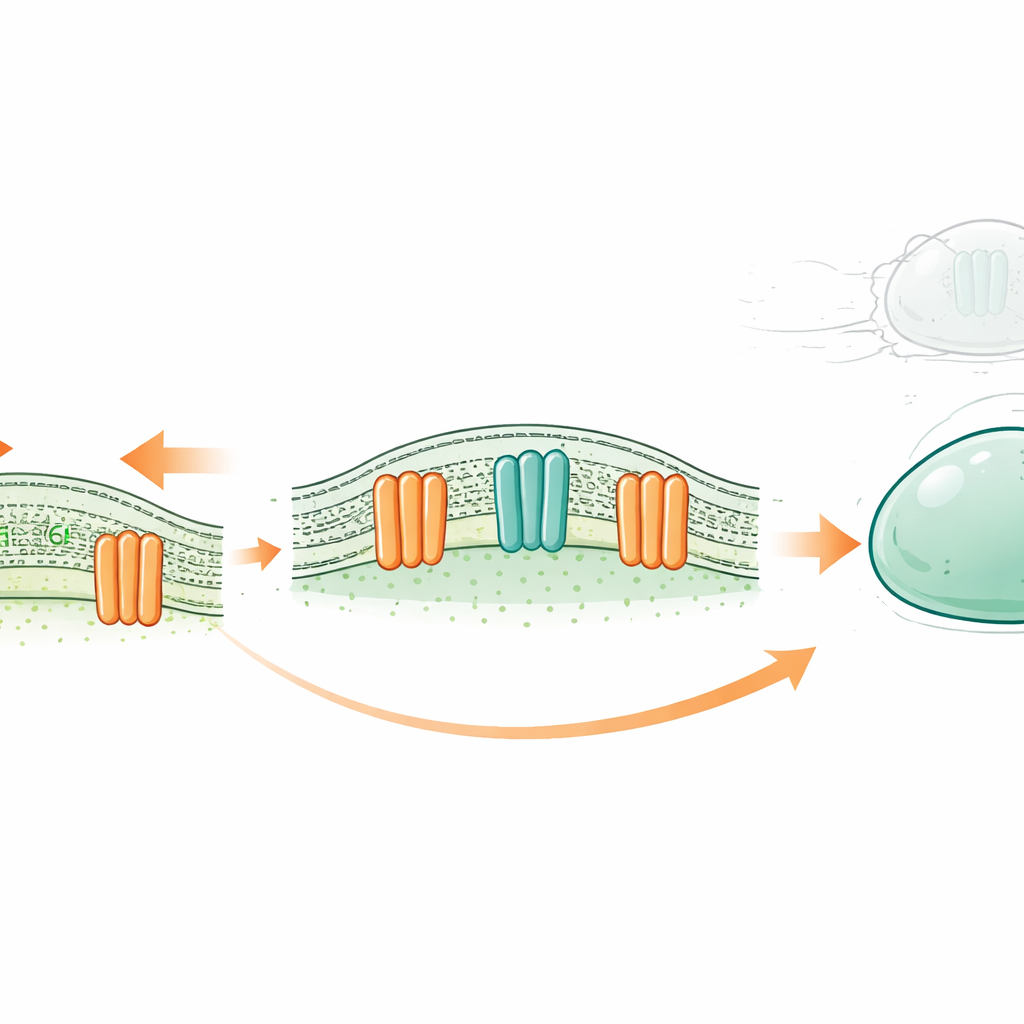
En ny sorts cellulär stötdämpare
Varje cell är omsluten av ett tunt oljigt membran bestående av två lager fettliknande molekyler kallade lipider. Traditionellt har vissa membranproteiner setts som enbart jonkanaler—små ventiler som låter laddade partiklar strömma in och ut som svar på stimuli såsom töjning. OSCA/TMEM63-familjen, som finns från växter till människor, är känd för att öppnas som svar på membranspänning. Tidigare strukturarbete antydde att deras porer till skillnad från klassiska jonkanaler delvis kantas av lipider själva. Det väckte en provocerande fråga: skulle dessa kanaler också kunna fungera som ”skramblasar”, och vända lipider mellan det inre och yttre lagret av membranet när cellen utsätts för kraft?
Att iaktta lipider som vänder över membranet
För att pröva denna idé kombinerade författarna datorsimuleringar med reduktionistiska labsystem byggda av renade komponenter. I simuleringar bäddades öppna varianter av flera OSCA- och TMEM63-proteiner in i modellmembran. Lipidmolekyler rörde sig spontant genom en fåra i dessa proteiner från ena sidan av bilagret till den andra, och bildade ett bälte som kopplade de två bladen samtidigt som en vattenfylld väg för joner lämnades kvar. I parallella experiment byggde teamet jättestora artificiella ”bubblor” (vesikler) innehållande fluorescerande lipider och specifika proteiner. När ett externt ämne släckte fluorescensen på ytan kunde ytterligare signalminskning enbart förklaras av att lipider vände från det inre lagret till utsidan. Vesikler som innehöll OSCA1.1, OSCA1.2, OSCA2.2 eller TMEM63A/B visade denna extra fluorescensminskning, vilket indikerar aktiv skrambling, medan kontrollkanaler som inte skramblar lipider inte gjorde det.
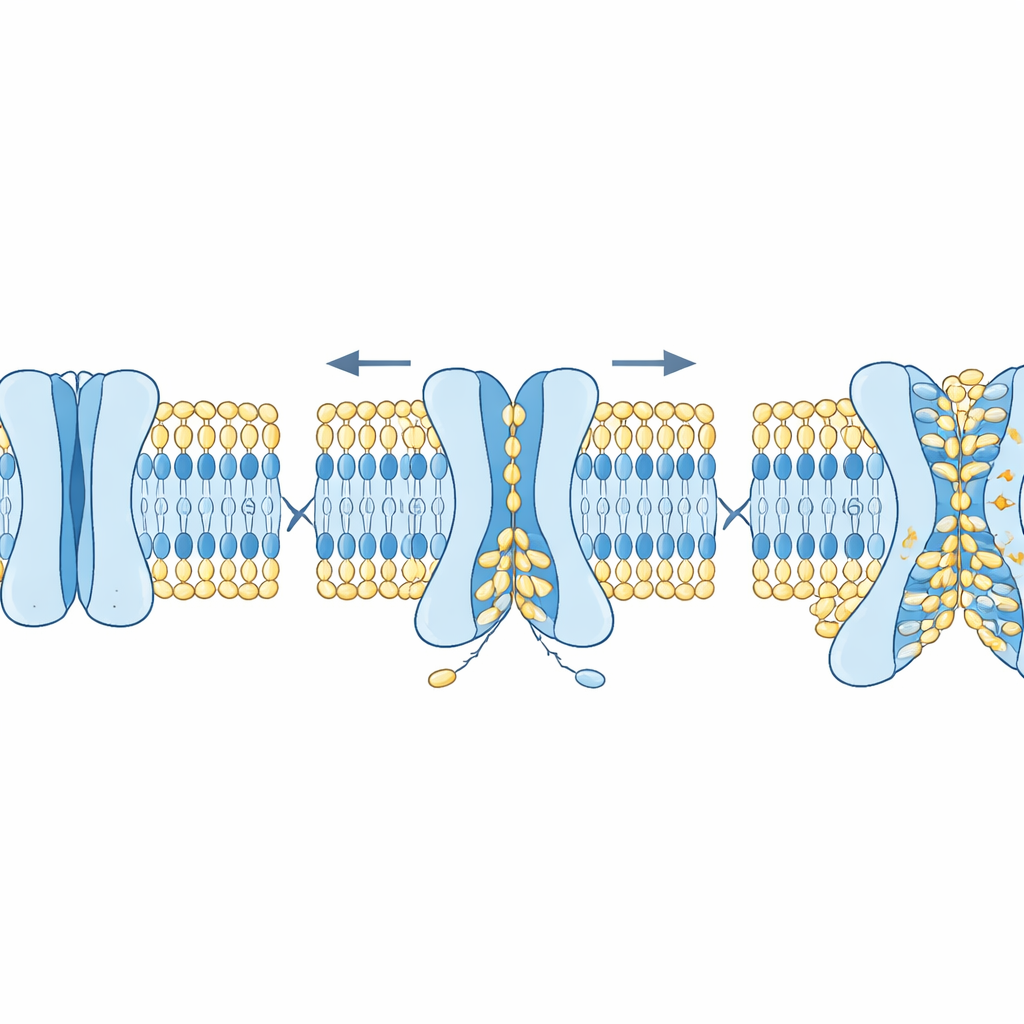
Hur struktur och kolesterol finjusterar processen
Forskarna frågade sedan vilka egenskaper hos TMEM63-proteiner som styr detta dubbla beteende. Med AlphaFold2 genererade de många tänkbara former av mänskliga TMEM63-proteiner, från stängda till alltmer öppna. Simuleringar visade att ett fåtal skrymmande aminosyror fungerar som ”flaskhalsar” i fåran. En rest begränsar huvudsakligen jonflödet, medan andra blockerar lipidrörelse. Mutation av jonsflaskhalsen ökade elektrisk ledningsförmåga utan att i hög grad förändra lipidskrambling, medan mutation av lipidporten gjorde att lipider vände lättare och till och med fick celler att visa ”ät-mig”-signaler på ytan utan ytterligare stimulus. En annan viktig regulator var kolesterol, en styv komponent i cellmembran. Tillsats av kolesterol till modellmembran saktade markant ner lipidskrambling och stabiliserade det stängda tillståndet hos TMEM63A, både i simuleringar och i kryoelektronmikroskopiska strukturer där kolesterol placerade sig i specifika bindningsställen på proteinet.
Mekanisk kraft som på/av-reglage
Om kolesterol normalt håller skrambling i schack inuti celler, vad slår då på det vid rätt tillfälle? Teamet använde ringformade socker-molekyler kallade cyklodextriner för selektivt dra ut lipider ur membranen och därigenom öka spänningen utan att ta bort kolesterol. I cellsstora vesikler aktiverade tillsats av cyklodextrin lipidskrambling av TMEM63A endast när proteinet fanns närvarande, vilket bevisar att ren mekanisk stress ensam kan utlösa vändningen. Liknande tillvägagångssätt i levande celler visade att mild kolesterolborttagning i sig inte var tillräcklig; en efterföljande mekanisk utmaning krävdes för att se stark skrambling. När celler konstruerade för att uttrycka TMEM63A sträcktes upprepade gånger exponerade de snabbt vissa lipider på sin yta, ett kännetecken för skrambling, medan celler som saknade dessa proteiner visade betydligt mindre förändring.
Att skydda celler från ruptur
Utöver att vända lipider förändrade mekaniskt aktiverad skrambling membranens fysiska beteende under extrem stress. I artificiella vesikler utsatta för hög kraft tenderade de utan skramblasar att spricka, medan vesikler som innehöll TMEM63A eller en känd skramblas krympte, bildade tunna tubuli och i hög grad förblev intakta. I en mänsklig hjärntumörcellinje som naturligt uttrycker TMEM63A och TMEM63B gjorde reducerade nivåer av något av proteinerna att cellerna i högre grad gick sönder vid stark mekanisk stress. Tillsammans stöder dessa fynd en modell där OSCA/TMEM63-proteiner fungerar som ventiler som öppnas under spänning och tillfälligt suddar ut den vanliga skillnaden mellan membranets inre och yttre yta. Genom att låta lipider omfördelas snabbt hjälper de till att utjämna spänning och förhindra katastrofala bristningar.
Vad detta betyder för hälsa och sjukdom
Rent praktiskt visar detta arbete att vissa töjningskänsliga kanaler gör mer än att leda elektriska signaler: de omorganiserar också cellens ytterhud för att hjälpa den överleva klämning. TMEM63-proteiner framträder som mekaniskt aktiverade lipid-skramblasar vars aktivitet är fint inställd av membranets sammansättning, särskilt kolesterol. Denna mekanism för mekanisk motståndskraft kan vara viktig där celler utsätts för stora krafter, från isoleringen av nervtrådar och ljudkännande celler i örat till cancerceller som tar sig igenom tät vävnad. Att förstå och så småningom kunna manipulera denna dubbla jonkanal–skramblasfunktion kan öppna nya vägar för att skydda sårbara vävnader—eller, omvänt, göra svårbehandlade cancerceller mer bräckliga.
Citering: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Nyckelord: mekanosensitiva jonkanaler, lipidskrambing, cellmembranets mekanik, kolesterolreglering, TMEM63 OSCA-proteiner