Clear Sky Science · sv
En neurotoxinisk kryptisk peptid som uppstår från TDP-43‑beroende kryptisk splitsning av PKN1
Dolda hot inne i hjärnceller
Många hjärnsjukdomar, inklusive amyotrofisk lateralskleros (ALS) och Alzheimers sjukdom, involverar klumpar av ett protein kallat TDP-43. Forskare vet att när detta protein slutar fungera korrekt förlorar nervceller viktiga budskap och dör så småningom. Denna studie avslöjar en mer överraskande vändning: TDP-43‑svikt kan också få hjärnceller att tillverka ett tidigare okänt, giftigt mini‑protein, som i sin tur skadar minneskretsar. Att förstå denna dolda aktör kan öppna nya vägar för diagnostik och behandling vid förödande demenser.
Hur en cellulär korrekturläsare håller RNA i schack
Inne i neuroner fungerar TDP-43 som en korrekturläsare för RNA, de mellanliggande budskapen mellan DNA och proteiner. Det binder till specifika korta sekvenser och blockerar insättning av lösa ”extra delar” i dessa budskap. När TDP-43 förloras eller förflyttas felaktigt, som vid ALS och i många Alzheimersfall, kan dessa extra delar — kallade kryptiska exoner — smyga in i RNA. Hittills har de flesta kända kryptiska exoner helt enkelt lett till förlust av normalt protein genom att göra budskapet instabilt och snabbt nedbrutet. Huruvida sådana händelser också kunde generera nya, skadliga proteiner var inte klart.
En kryptisk splitsning skapar en toxisk fragment
Forskarlaget fokuserade på en gen kallad PKN1, som hjälper till att upprätthålla cellernas inre stomme och signalflöde i neuroner. Med hjälp av cellmodeller där TDP-43 var minskat upptäckte de en tidigare okänd kryptisk exon, döpt till PKN1‑5a1, insatt mellan två normala segment av PKN1‑RNA. Denna insättning inför ett tidigt stoppsignal och producerar ett förkortat RNA. Anmärkningsvärt nog undkom en del av detta felaktiga budskap cellens kvalitetskontrollsystem och översattes till ett stabilt fragment av PKN1‑proteinet som innehöll endast dess första 207 aminosyror. Teamet kallade denna trunkerade produkt PKN207. De visade att TDP-43 normalt förhindrar detta misstag genom att binda till flera UG‑rika regioner som flankerar den kryptiska exonen; när det bindningen förloras splitsas exonen in och PKN207 produceras.
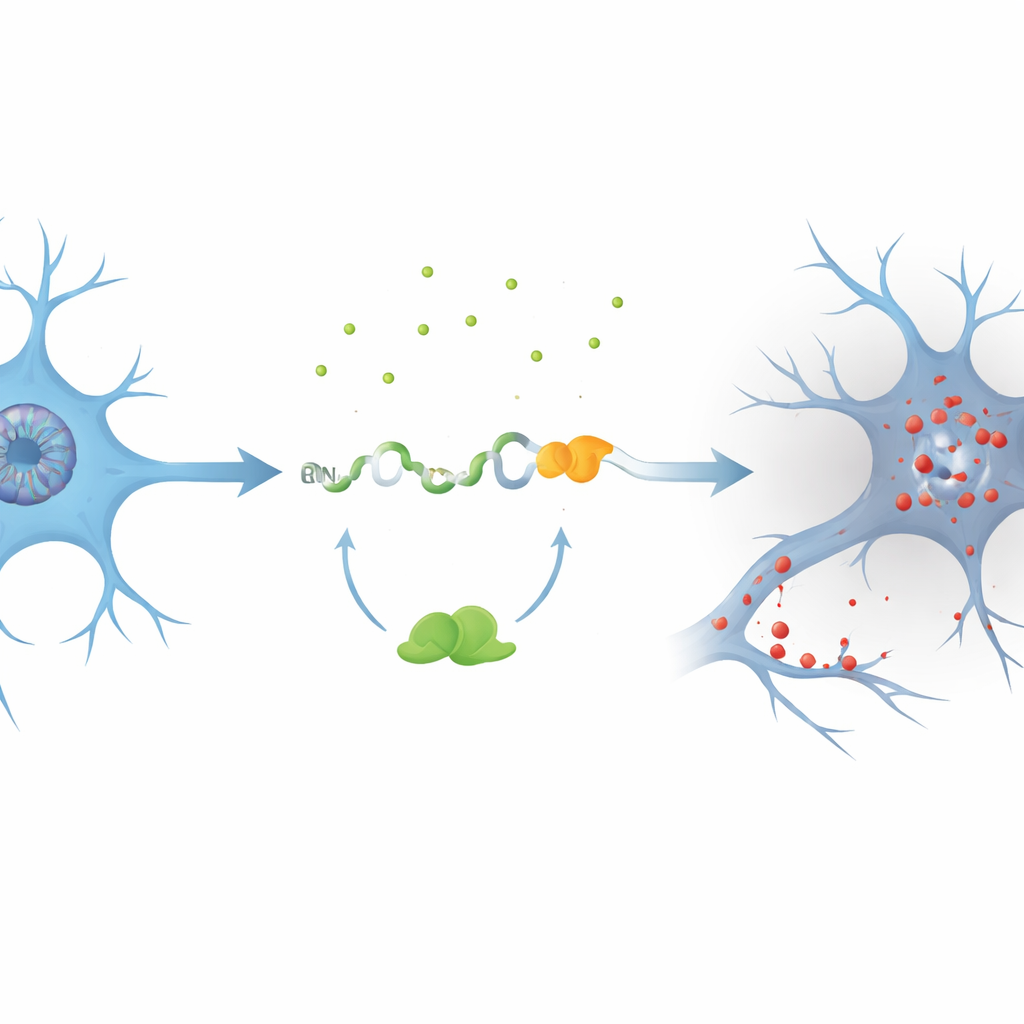
Bevis från patienthjärnor och stora dataset
För att se om denna händelse inträffar vid mänsklig sjukdom grävde forskarna i RNA‑sekvenseringsdata från hundratals ALS‑prov från hjärna och ryggmärg. De fann utbredd aktivering av den kryptiska PKN1‑5a1‑exonen i regioner som är kända för att påverkas av TDP-43‑patologi, såsom motorcortex och ryggmärg, men inte i den relativt sparade lillhjärnan. De framställde sedan mycket specifika antikroppar som bara känner igen den unika svansen hos PKN207, inte fullängds‑PKN1‑proteinet. I hippocampusvävnad från Alzheimerspatienter som också visade onormalt, fosforylerat TDP-43, upptäckte dessa antikroppar ett distinkt band som motsvarade PKN207, medan ett sådant band saknades i kontrollhjärnor. Ytterligare Alzheimer‑dataset bekräftade att den kryptiska exonen slås på redan i tidiga sjukdomsstadier, vilket tyder på att detta molekylära fel kan börja långt innan symtom blir tydliga.
Ett mini‑protein med stort inflytande på minnet
Upptäckten av PKN207 i sjuk mänsklig hjärna väckte den viktiga frågan: är det skadligt? För att testa detta använde teamet virus för att driva produktion av antingen normalt PKN1 eller PKN207 specifikt i hippocampus — ett hjärnområde som är avgörande för minnet — hos unga möss. Månader senare visade båda grupperna av möss försämrat lärande i Morris vattenlabyrint, där de simmade längre för att hitta en dold plattform. Deras ryggmärgsvätska innehöll högre nivåer av ett strukturellt protein, neurofilament light chain, en markör för axonskada. I odlade neuroner utlöste ökad PKN207 cellskada, mätt som läckage av ett enzym som signalerar membranskada. Detaljerad proteomprofilering av hippocampus visade breda förändringar i vägar kopplade till synaptisk styrka (långtids potentiation) och välkända neurodegenerativa sjukdomar, med särskilt stark störning av molekyler som understöder effektiv signalering och en hälsosam nervfiberstomme.
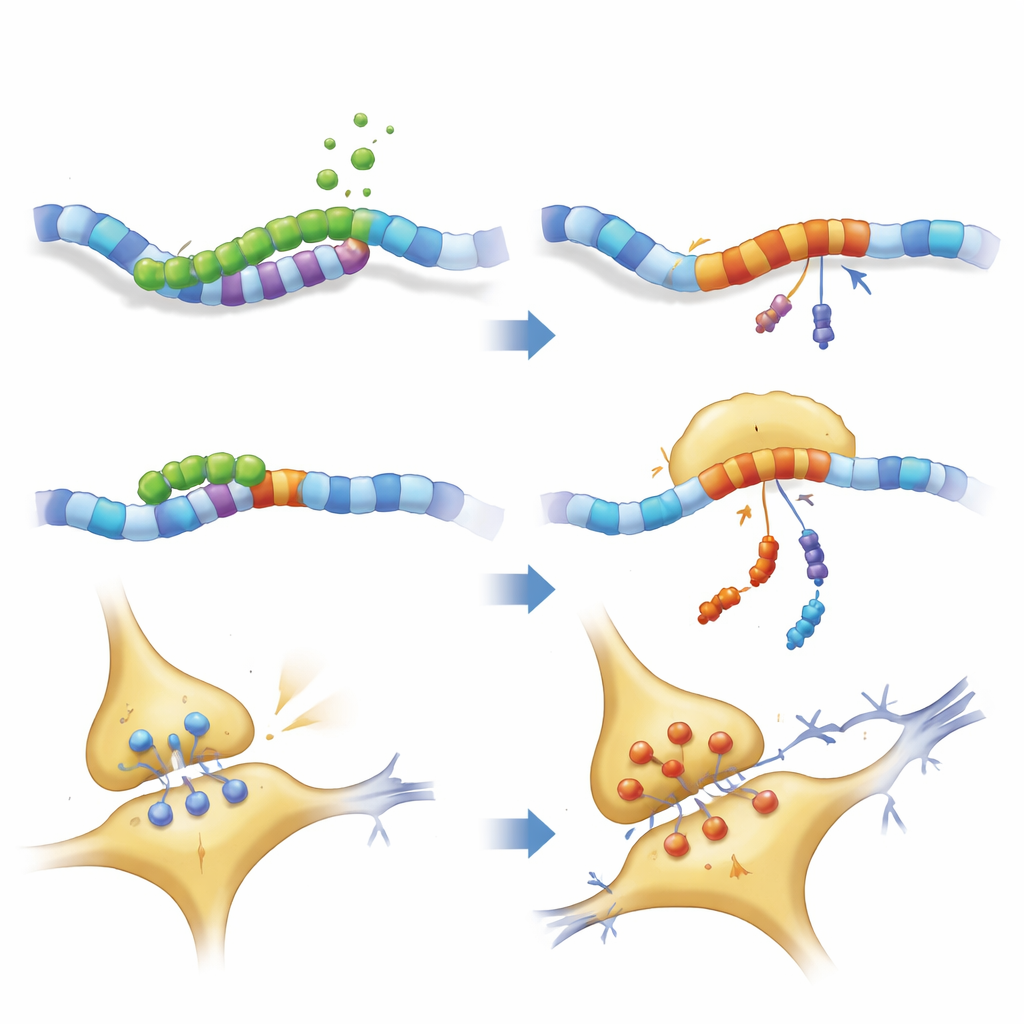
Hur fragmentet stör hjärnans kopplingar
Närmare granskning av neuronernas struktur visade att både fullängds‑PKN1 och PKN207 störde neurofilamentnätverket som ger axonerna deras form och hjälper till att transportera last. Nyckel‑motor‑ och stomproteiner minskade, medan vissa neurofilamentkomponenter ackumulerades, vilket antyder trafikstockningar och möjlig klumpbildning. Elektriska inspelningar från hippocampus‑skivor bekräftade att möss som uttryckte PKN207 hade försvagad långtids potentiation — den process genom vilken synapser förstärks efter upprepad aktivitet och en allmänt accepterad cellulär grund för inlärning och minne. Trots att PKN207 saknar PKN1:s enzymdomän var dess närvaro tillräcklig för att efterlikna och ibland överträffa de störande effekterna av det fulla proteinet, vilket tyder på att den delade N‑terminala regionen på egen hand kan störa neuronal homeostas.
Varför denna upptäckt betyder något för hjärnsjukdomar
Detta arbete lägger ett nytt lager till vår förståelse av TDP-43‑relaterade sjukdomar. I stället för att enbart orsaka förlust av viktiga RNA kan TDP-43‑svikt också framkalla ett stabilt, giftigt mikro‑protein som undergräver synapser och kognition. Den kryptiska PKN1‑5a1‑exonen och dess peptidprodukt PKN207 framstår nu som potentiella biomarkörer för tidig TDP-43‑dysfunktion och som kandidatmål för terapier som korrigerar splitsning eller blockerar det skadliga fragmentet. Mer generellt antyder studien att andra dolda exoner på samma sätt kan ge upphov till sjukdomsdrivande peptider, vilket pekar forskare mot ett rikt — och tidigare förbises — landskap av molekylära förövare i neurodegeneration.
Citering: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Nyckelord: TDP-43, kryptisk splitsning, PKN1, neurodegeneration, Alzheimer och ALS