Clear Sky Science · sv
Motverkande FOX‑proteiner kontrollerar epigenetiskt herpesvirusets balans mellan lytisk och latent fas
Varför dolda herpesvirus är viktiga
Många bär på herpes simplex‑virus livet ut, ofta utan att veta om det. Dessa virus kan ligga tysta inne i nervceller i åratal för att plötsligt blossa upp och orsaka munsår, ögonsjukdomar eller allvarligare problem hos personer med försvagat immunförsvar. Vad som håller viruset sovande större delen av tiden och vad som väcker det igen har länge varit en gåta. Denna studie blottlägger en central del av kontrollsystemet: en dragkamp mellan två motsatta grupper av mänskliga proteiner som omformar det virala DNA:t och avgör om herpes förblir tyst eller börjar producera nya virus.
Två cellulära lag som drar åt olika håll
Forskarna fokuserade på en stor familj av mänskliga DNA‑bindande proteiner kallade FOX‑proteiner, som normalt hjälper till att reglera våra egna gener under utveckling och i ämnesomsättningen. Genom att pröva många FOX‑familjemedlemmar i nervliknande celler fann de två tydliga läger. En grupp (inklusive proteiner som FOXF1) ökade kraftigt replikationen av herpes simplex‑virus typ 1 (HSV‑1) och flera närbesläktade ”alfa”‑herpesvirus. En annan grupp (FOXK1 och FOXK2) gjorde motsatsen och hämmade virusets tillväxt kraftfullt. Denna balans var inte densamma i alla celltyper: icke‑neurala celler och stressade neuroner tenderade att uttrycka mer av de aktiverande FOX‑proteinerna, medan vila hos sensoriska neuroner gav väldigt lite av dem men höga nivåer av de repressiva FOXK‑proteinerna.
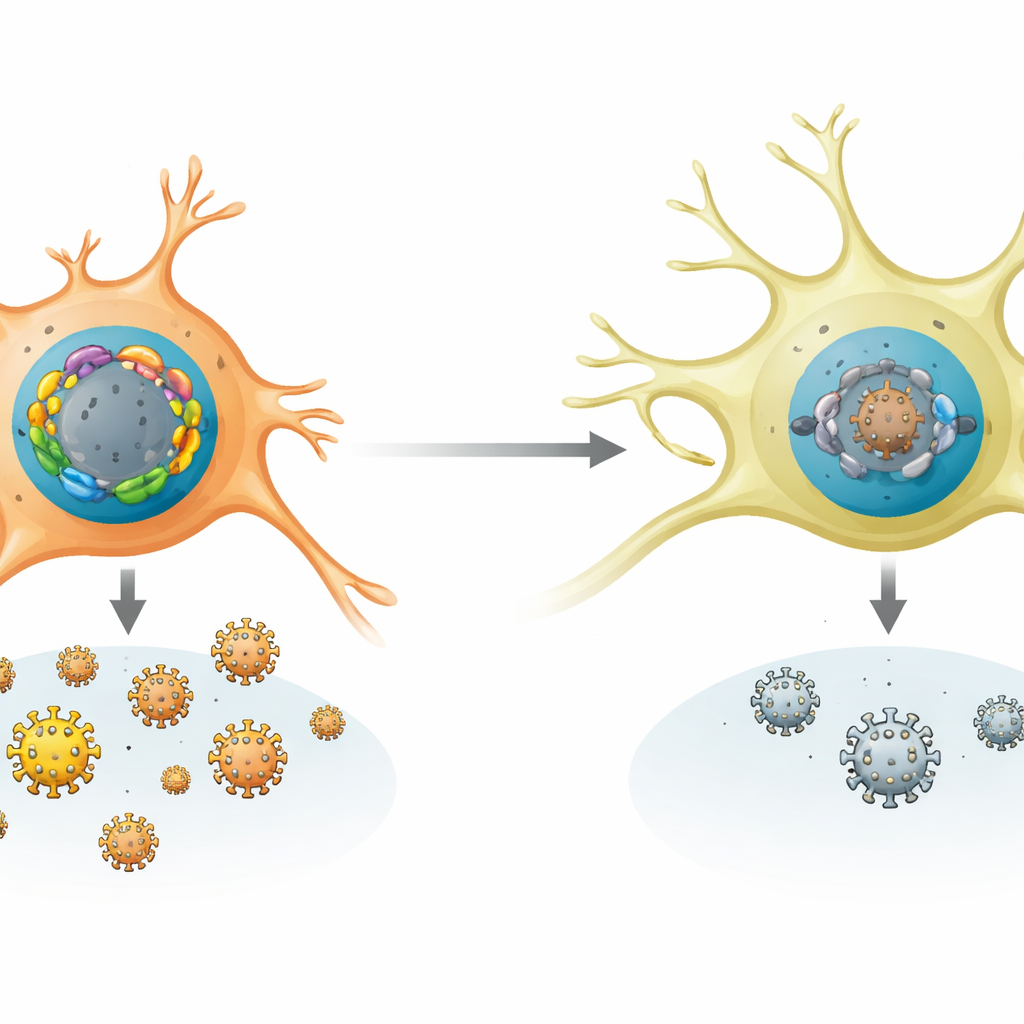
Hur nervceller gynnar det tysta tillståndet
Teamet jämförde FOX‑geners aktivitet över många mänskliga och muscellstyper och i infekterade djur. Sensoriska neuroner, virusets naturliga hemvist vid latens, visade ett mönster som gynnar tystnad: starkt uttryck av FOXK1 och FOXK2 och svagt uttryck av de flesta aktiverande FOX‑gener. Hos möss ökade tidig infektion och senare stressignaler såsom värme eller vävnadsskada selektivt nivåerna av flera aktiverande Fox‑gener utan att minska de repressiva. I odlade musneuroner och i levande möss gjorde borttagning eller nedreglering av FOXK‑proteiner det lättare för HSV‑1 att replikera och att vakna från latens. Omvänt var det tillräckligt att tvinga neuroner att producera extra aktiverande FOX‑proteiner för att trigga reaktivering även utan kemiska signaler, vilket visar hur känsligt det virala tillståndet är för denna FOX‑balans.
Grepp om viralt DNA — öppna eller stänga det
För att förstå den bakomliggande mekanismen kartlade forskarna var FOX‑proteiner binder på det virala genomet. De fann att både aktiverande FOXF1 och repressiva FOXK1 binder brett över HSV‑1‑DNA, inte bara vid några få specifika sekvensmotiv. Detta bindande förlitar sig på en bevarad del av FOX‑proteinerna som tar tag i DNA‑ryggraden snarare än individuella baser, vilket gör att de kan fästa nästan var som helst. När de väl sitter där rekryterar de två proteinlägren olika molekylära partner som omformar kromatinet — kombinationen av DNA och dess paketeringsproteiner. Aktiverande FOX‑proteiner, särskilt FOXF1, associerar med CBP och P300, enzymer som tillsätter acetylgrupper på histoner och luckrar upp kromatin. Det gör det virala DNA:t mer tillgängligt och ökar tidig, medel och sen viral genaktivitet. FOXK1 samarbetar däremot med faktorer som SIN3A och MAX som kopplats till histondeacetylation och genrepression, vilket stramar åt det virala kromatinet och håller gener avstängda.
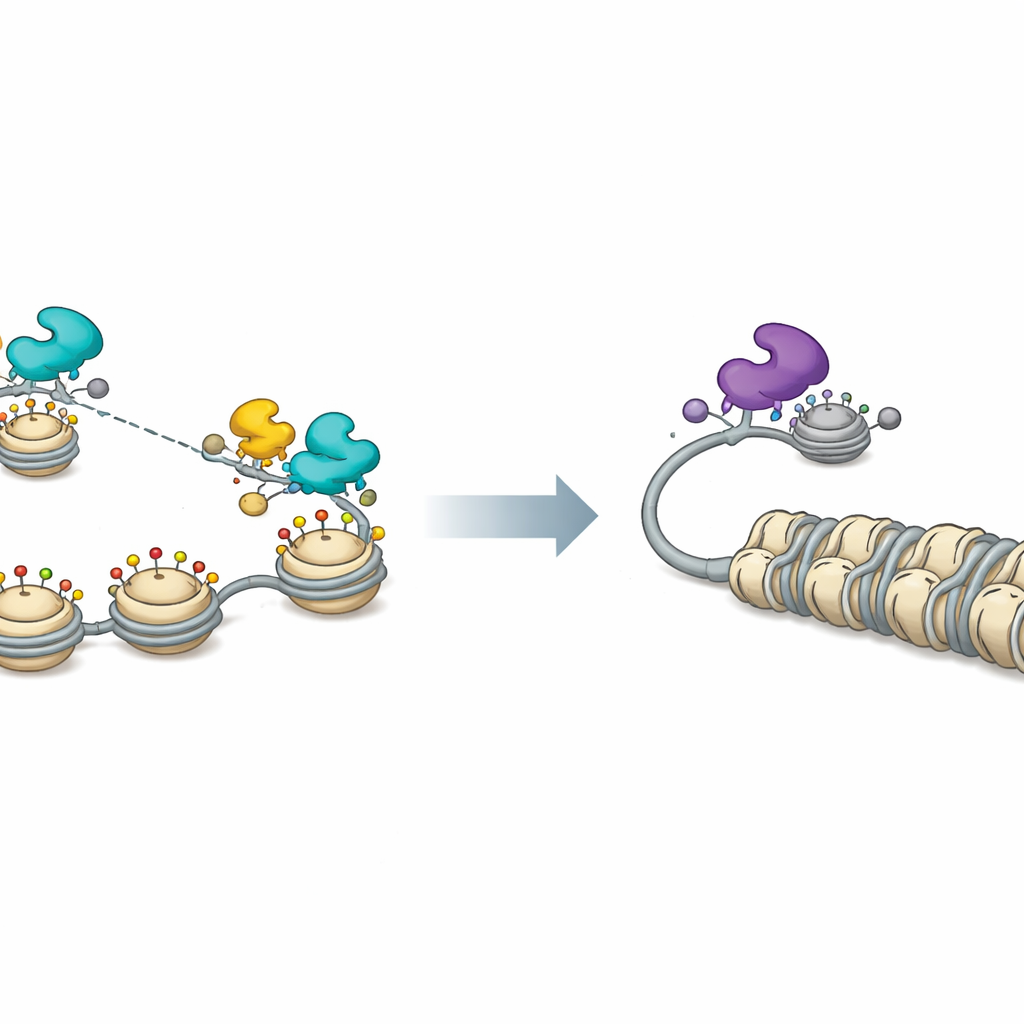
En kromatinswitch för viralt sömn och vakenhet
Mätningar av viralt kromatin bekräftade denna bild. När FOXF1 var närvarande var histoner på viralt DNA avklädda eller kemiskt märkta på sätt som förknippas med öppet, aktivt kromatin, och den övergripande tillgängligheten för virala promotorer ökade över genomet. Uttryck av FOXF1 spred också ut små nukleära strukturer kallade PML‑kärnorganeller, som normalt hjälper till att hålla viralt DNA repressivt. Blockering av CBP och P300 utsuddade många av dessa aktiverande effekter och minskade FOXF1‑driven viral genuttryck. På den repressiva sidan visade forskarna att FOXK1‑associerade partner och histondeacetylasaktivitet var viktiga för att hålla HSV‑1‑replikationen låg; kemisk inhibering av deacetylaser ökade både virusproduktionen och försvagade FOXK1‑medierad suppressiv effekt.
Vad detta betyder för att kontrollera livslång infektion
Tillsammans antyder arbetet att huruvida HSV‑1 är aktivt eller vilande i hög grad beror på blandningen av FOX‑proteiner i den infekterade neuronen. Vila hos sensoriska neuroner gynnar naturligt det repressiva, FOXK‑dominerade tillståndet som pressar viruset in i en djupt tyst, kromatin‑kompakterad form. Stress eller andra förhållanden som höjer nivåerna av aktiverande FOX‑proteiner kan rubba denna balans, öppna det virala kromatinet och tillåta den lytiska cykeln att återstarta. Genom att avslöja denna epigenetiska dragkamp belyser studien nya vägar forskare en dag kan använda för att antingen trycka herpesvirus mer bestämt in i ofarlig latens eller — alternativt — tvinga dem ur gömställen under kontrollerade former så att de kan elimineras.
Citering: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Nyckelord: latens hos herpes simplex‑virus, FOX‑transkriptionsfaktorer, viralt kromatin, epigenetisk reglering, virusreaktivering