Clear Sky Science · sv
Evolutionär omfunktionering av ett metabolt tioolas-komplex möjliggör biosyntes av antibiotika
Hur vardagliga mikrober återuppfinner sin kemi
Många av de antibiotika och läkemedel vi förlitar oss på tillverkas tyst av bakterier. Dessa små kemister använder enzymer — molekylära maskiner — för att bygga komplexa försvarsföreningar. Denna studie avslöjar hur ett kärnmetabolt enzymkomplex, som tidigare användes för grundläggande cellunderhåll, evolutionärt har omkopplats i orala bakterier för att producera ett potent antibiotikum. Att förstå denna omvandling visar inte bara hur naturen uppfinner ny kemi utan ger också ledtrådar för att designa nästa generations läkemedel och biokatalysatorer.
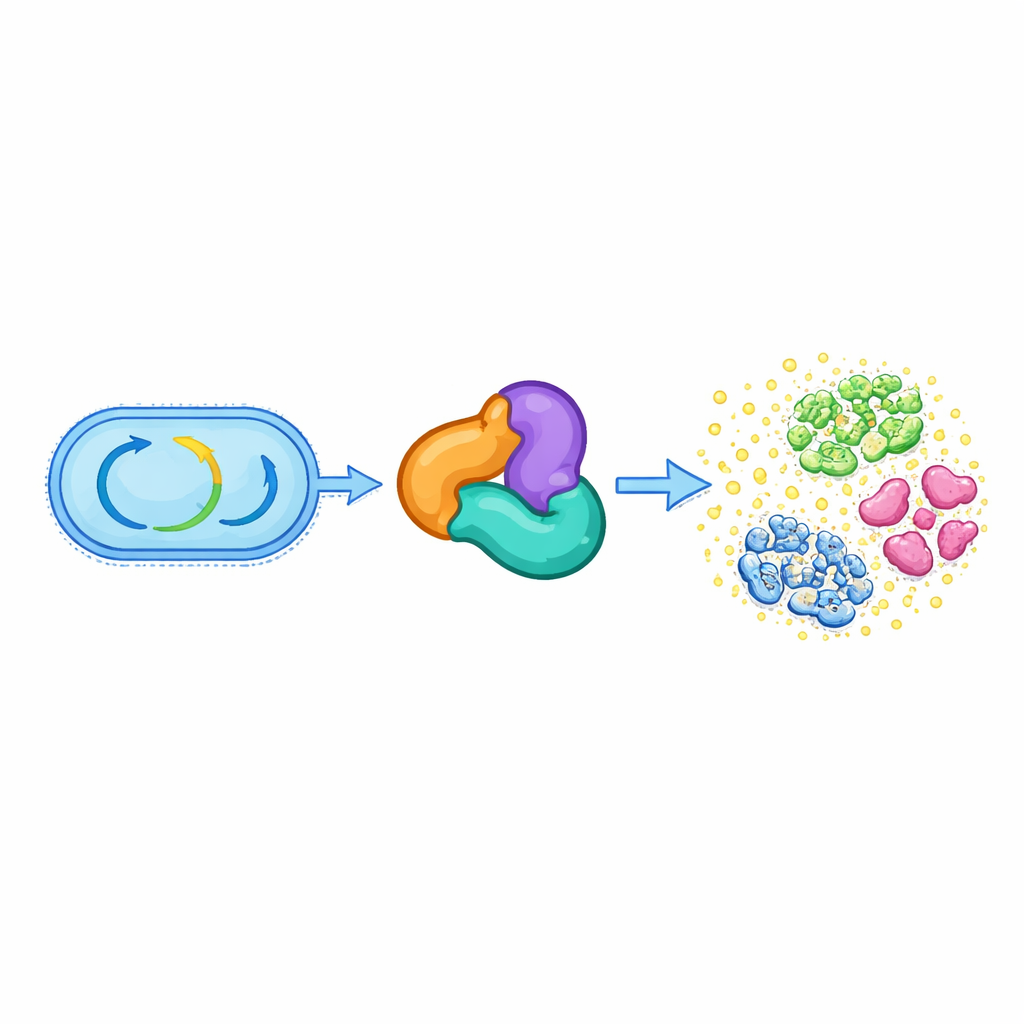
Från basal metabolism till kemiskt vapen
Alla levande celler är beroende av en uppsättning bevarade enzymer som driver deras centrala metabolism, såsom nedbrytning av fetter och uppbyggnad av viktiga molekyler. En sådan grupp, kallad tioolas-superfamiljen, hjälper normalt till att hantera små energirika molekyler som acetyl-CoA och stöder viktiga vägar för syntes av lipider och andra cellkomponenter. Författarna upptäckte att i flera orala Streptococcus-arter har ett trefaldigt tioolasbaserat komplex — bestående av proteiner relaterade till HMGS, ACAT och ett tredje hjälparprotein — övergett sin förfäders metabola roll. I stället fullgör detta komplex nu biosyntesen av ett antibiotikum kallat reutericyclin A, vilket hjälper dessa bakterier att konkurrera i den trånga miljön i munnen.
En ny sorts enzymreaktion på ett antibiotikaskelett
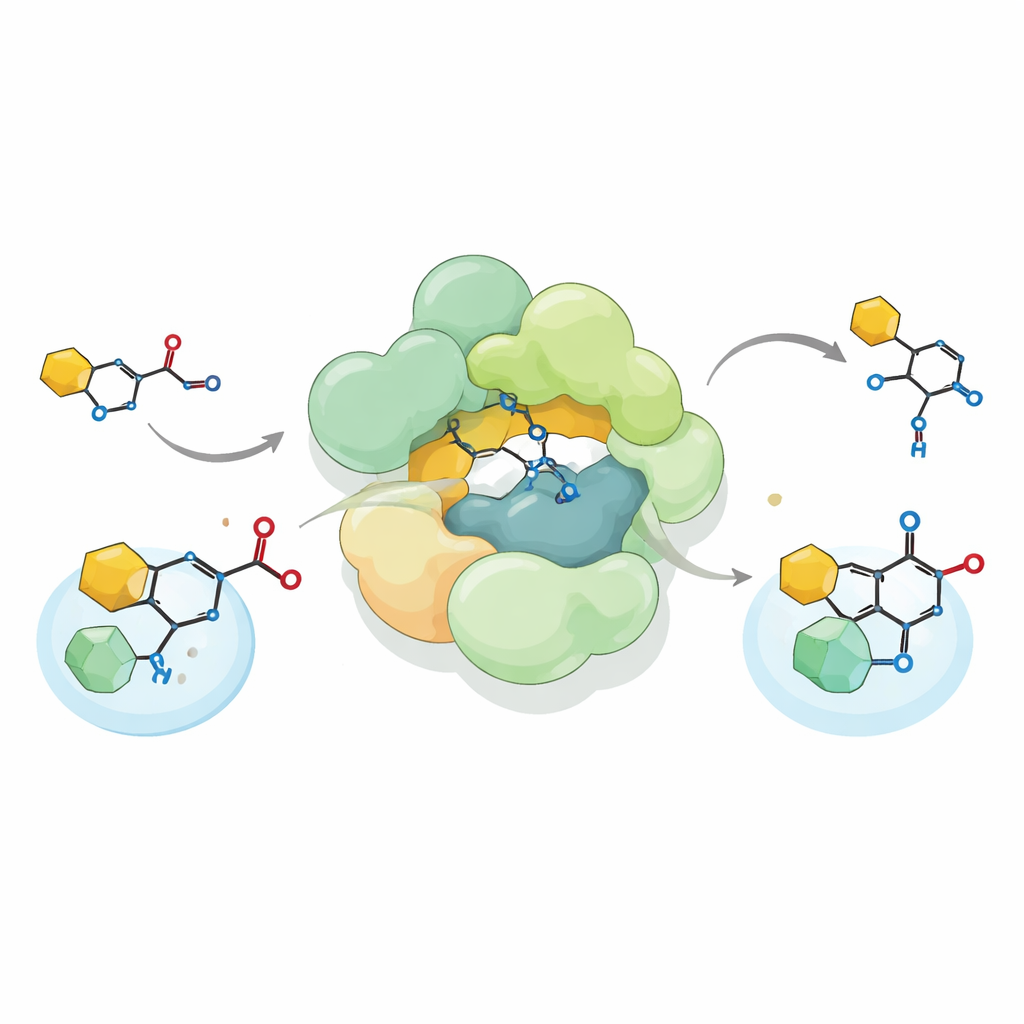
Genom att återuppbygga Streptococcus-komplexet i laboratoriet och mata det med en kemiskt syntetiserad prekursor till reutericyclin A visade forskarna att komplexet utför en ovanlig kol–kol-bindningsbildande reaktion känd som Friedel–Crafts C-acylering. I stället för att fästa en acetylgrupp på syre, som många enzymer gör, installerar det denna grupp direkt på en kolatom i en pyrrolidin-2,4-dionring — en viktig del av reutericyclin-skelettet. Komplexet accepterar både naturliga acetylgivare såsom acetyl-CoA och flera artificiella givare, och kan till och med köra reaktionen i omvänd riktning och bryta den bindning det skapat. Denna flexibilitet utökar den kända repertoaren av biologiska acyltransferaser och antyder hur sådana enzymer kan anpassas för att bygga mångsidiga kemiska produkter.
Omkonstruktion av ett bevarat proteinskelett
Med hjälp av högupplöst kryo-elektronmikroskopi löste teamet den tredimensionella strukturen av Streptococcus-komplexet, kallat SmaATase. Trots sin nya funktion behåller SmaATase en slående arkitektonisk likhet med ett närbesläktat komplex i arkéer som deltar i mevalonatvägen för uppbyggnad av isoprenoida lipider. Båda är stora multimeriska enheter byggda av upprepade moduler och har ett gemensamt hålrum där kofaktorn CoA kan binda och röra sig mellan aktiva ytor. Dock saknas eller är förändrade nyckelkatalytiska rester som är väsentliga för den ursprungliga metabola reaktionen i den bakteriella versionen. Biokemiska tester bekräftar att SmaATase inte längre kan göra det anfädersprodukt HMG-CoA och i stället använder acetyl-CoA enbart som givare för sina nya småmolekylära substrat.
En evolutionär bana från metabolism till antibiotika
För att förstå hur en sådan omfunktionering kan ha utvecklats jämförde författarna sekvenser och aktiviteter hos närbesläktade komplex över många bakterier och arkéer. De identifierade över tusen genkluster som innehåller samma trio av enzymtyper. Vissa stöder fortfarande klassisk tioolas-kemi; andra, som de i Pseudomonas, driver syntesen av andra småmolekylära antibiotika. Ett representativt komplex från Pseudomonas fluorescens verkar befinna sig halvvägs längs denna evolutionära väg: dess HMGS-liknande domän är inaktiverad, men dess ACAT-liknande enhet utför fortfarande en mer konventionell reaktion på CoA-länkade substrat. I SmaATase och dess Pseudomonas-motsvarighet som producerar den växtskyddande föreningen DAPG har ytterligare förändringar runt det aktiva sätet anpassat enzymerna att känna igen icke-standard acceptorer såsom aromatiska ringar eller tetraminsyra-kärnor.
Varför en liten acetylgrupp gör stor skillnad
I slutändan är den biologiska vinsten av denna molekylära förvandling tydlig. När teamet testade de acetylade antibiotika reutericyclin A och DAPG mot en panel av Gram-positiva bakterier visade dessa molekyler stark dödande aktivitet, medan deras oacetylade prekursorer var mycket svagare eller nästan inaktiva. Den lilla acetylgruppen, placerad på precis rätt position av det omfunktionerade enzymkomplexet, förvandlar ett måttligt skelett till ett kraftfullt vapen, vilket gör det möjligt för Streptococcus i munnen eller Pseudomonas vid växtrötter att konkurrera ut grannar. Detta arbete visar hur evolutionen kan återvinna befintliga enzymramar med minimala men strategiska mutationer, och förvandla rutinmässig metabolisk maskineri till specialiserade verktyg för kemiskt försvar — och erbjuder en ritning för ingenjörer som vill designa nya kol–kol-bindningsbildande katalysatorer för läkemedelsupptäckt och syntetisk biologi.
Citering: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Nyckelord: enzymutveckling, biosyntes av naturprodukter, antibiotikakemi, metabol omfunktionering, Friedel–Crafts acylering