Clear Sky Science · sv
Konstruerade alkoholoxidaser katalyserar transesterifiering i vattenmiljö utan konkurrerande hydrolys
Varför denna enzymberättelse är viktig
Många vardagliga produkter, från läkemedel och aromämnen till biodiesel, är beroende av en enkel typ av kemisk bindning kallad en ester. Att framställa och justera dessa estrar effektivt, billigt och på ett miljövänligt sätt är ett huvudmål inom grön kemi. Problemet är att vatten — den idealiska lösningsmedeln ur säkerhets- och hållbarhetssynpunkt — vanligtvis saboterar dessa reaktioner genom att sönderdela estrarna lika snabbt som de bildas. Denna studie avslöjar ett konstruerat enzym som kan bygga estrar i vatten samtidigt som det i praktiken ignorerar det omgivande vattnet, vilket öppnar en väg till renare industriell kemi.
Att ge ett känt enzym ett nytt uppdrag
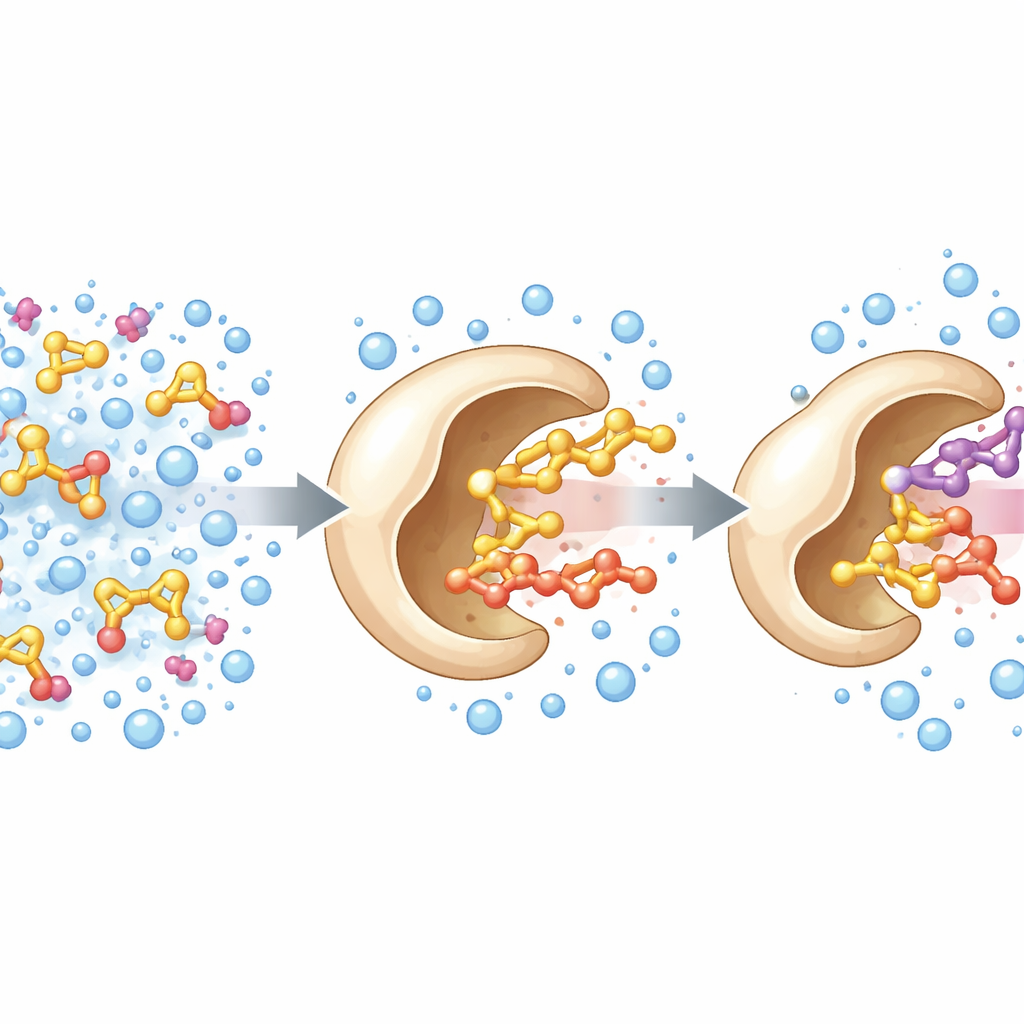
Forskarlaget utgick från ett känt enzym, en alkoholoxidas från en vednedbrytande svamp. I naturen använder detta enzym en flavin‑cofaktor för att avlägsna elektroner från små alkoholer som metanol. Teamet ville vidga dess räckvidd så att det även kunde hantera skrymmande alkoholer, vilka är mer relevanta för finkemikalier och aromer. Med enzymets tredimensionella struktur som karta fokuserade de på tre aminosyror som bildar en slags port in till det aktiva sätet. Genom att randomisera dessa positioner och skärma de uppkomna varianterna upptäckte de en triplett‑mutant — benämnd PcAOx‑VPN — som effektivt kunde bearbeta större alkoholer som bensylalkohol samtidigt som mycket av aktiviteten mot små alkoholer som metanol gick förlorad.
Oväntad förmåga: att bygga estrar i vatten
Vid tester av PcAOx‑VPN i blandningar avsedda att lösa oljiga substrat noterade teamet extra toppar i sina analytiska utslag. Dessa visade sig vara acetylerade produkter: enzymet överförde en acylgrupp från en aktiverad ester‑donator till alkoholer, en reaktion känd som transesterifiering. Anmärkningsvärt nog skedde detta i vattenbaserad buffert, något som normalt leder till stark konkurrerande hydrolys där vatten angriper och förstör estern. Här förenade PcAOx‑VPN effektivt alkoholer och acyldonatorer som vinylacetat för att bilda nya estrar, ofta med utbyten över 80 % och endast måttliga sido‑reaktioner. Samma enzym kunde dessutom verka på ett brett spektrum av alkoholer, inklusive raka kedjor, aromatiska, kirala och svavelinnehållande exempel, och visade i flera fall en tydlig preferens för en spegelbildsform framför den andra.
Att hålla vattnet ur vägen
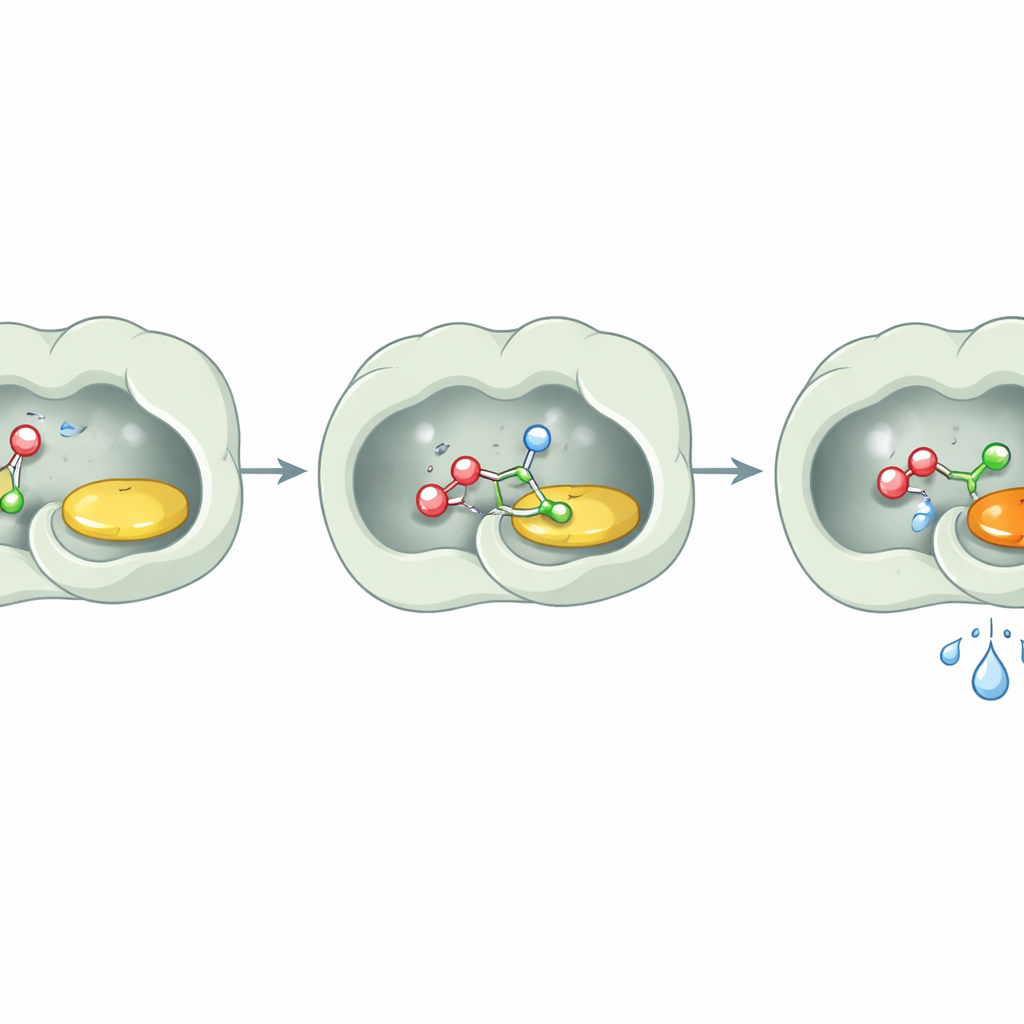
En viktig överraskning var vad enzymet inte gjorde: det hydrolyserade inte estrar i någon märkbar utsträckning. Även efter långa inkubationer med estersubstrat och vatten lämnade PcAOx‑VPN dem i princip intakta såvida ingen ytterligare acyldonator tillfördes. Strukturella studier ger en enkel förklaring. Det aktiva sätet är fodrat med till stor del oljiga, aromatiska aminosyror som skapar en starkt hydrofob ficka. Noggrann analys visade inga vattenmolekyler nära flavin‑cofaktorn, och beräkningsverktyg bekräftade att kanalen in till det aktiva sätet också ogillar vatten. I praktiken bygger enzymet ett litet torrt rum inne i en vattenfylld värld. Alkoholer och aktiverade estrar kan komma in och reagera, men vattenmolekyler hålls på avstånd så att de aldrig får en chans att bryta ned produkten.
Hur reaktionen troligen fungerar inuti
Mekanistiska experiment och mutationsanalys visade att två aminosyror, en histidin och en asparagin, är centrala både för enzymets naturliga oxidationsroll och dess nya transesterifieringsförmåga. Histidinet fungerar som en bas och hjälper till att avlägsna en proton från den inkommande alkoholen för att göra den mer reaktiv, medan asparaginet stabiliserar den laddade tilstånd som uppstår. Tillsammans underlättar de alkoholens angrepp på acyldonatorn för att bilda ett kortlivat mellanled som kollapsar till den önskade estern. Flavinets oxiderade tillstånd krävs också: under syrgasfria förhållanden, när flavinet blir reducerat, upphör transesterifieringen och återupptas först när luft tillsätts igen. Noterbart är att när samma trio mutationer infördes i närbesläktade oxidaser från andra svampar, fick även dessa en robust transesterifieringsaktivitet, vilket tyder på att detta beteende kan generaliseras.
Vad detta betyder för grönare kemi
För icke‑specialister är huvudbudskapet att författarna lärt ett känt enzym ett nytt trick: att bygga användbara estrar direkt i vatten samtidigt som enzymet effektivt ignorerar vattnets tendens att ogöra arbetet. Genom att karva ut en torr, oljevänlig ficka inne i ett protein och finjustera ett fåtal nyckelaminosyror skapade de en katalysator som föredrar alkoholer framför vatten som reaktionspartners. Eftersom samma designprincip fungerar i närbesläktade enzymer kan detta tillvägagångssätt utsträckas till en familj av katalysatorer för framställning av aromer, doftämnen, finkemikalier och möjligen biobränslen i säkrare, mer hållbara processer som i mindre utsträckning förlitar sig på hårda organiska lösningsmedel och i större utsträckning på vatten.
Citering: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Nyckelord: enzymteknik, biokatalys, grön kemi, estersyntes, flavoproteiner