Clear Sky Science · sv
PRMT3-medierad post-translationell anpassning till fasta reglerar metabol flexibilitet
Varför måltidstid och kroppens bränsle spelar roll
Många provar fasta eller tidsbegränsad ätning för att gå ner i vikt eller förbättra blodsockret, men resultaten kan vara ojämna. Denna studie granskar vår ämnesomsättning för att ta reda på varför. Genom att fokusera på bukfett hos möss och på mänskliga prover identifierar forskarna en molekylär strömbrytare som hjälper fettvävnad avgöra om den ska bränna eller lagra bränsle, och visar hur både måltidstiming och ett läkemedel kan växla denna brytare mot bättre hälsa.
En flexibel motor inne i vårt fett
Våra kroppar fungerar bäst när de smidigt kan växla mellan att bränna fett under fasta och att bränna socker efter måltider. Denna ”metaboliska flexibilitet” går ofta förlorad vid fetma, vilket gör det svårare att hantera svängningar i energitillgång och -behov. Teamet studerade visceralt vitt fett — det djupare bukfettet starkt kopplat till diabetes och hjärtsjukdom — och fann att specifika kemiska märken på proteiner, så kallade metylgrupper, ändras med födointag och fasta. Hos både möss och människor bygger två sådana märken, MMA och ADMA, upp i visceralt fett i takt med ökad kroppsvikt och BMI, vilket tyder på att de är markörer för en trög, mindre anpassningsbar ämnesomsättning.
En matningssignal som gör ämnesomsättningen stel
Forskarna fokuserade på ett enzym i fettcellerna kallat PRMT3, som sätter dit dessa metylmärken. Hos möss ökar PRMT3-nivåerna i visceralt fett under natten när djuren äter och sjunker under dagen när de fastar, i ett mönster som noggrant följer nivåerna av MMA och ADMA. Denna rytm beror på insulin och ett nyckelproteinsignalämne, AKT: när mat eller injicerat insulin aktiverar AKT slås PRMT3 på och blir mer modifierat, vilket i sin tur ökar mängden metylerade proteiner. Att blockera AKT eller direkt hämma PRMT3 plattar snabbt till denna metyleringssignal, och kan till och med efterlikna effekten av en mycket längre fasta.
Omdirigering av fettceller från lagring till förbränning
Vad gör dessa kemiska taggar i praktiken? Studieresultaten visar att PRMT3 stabiliserar en transportörprotein kallad SLC25A1 i mitokondrierna — cellens energifabriker. SLC25A1 förflyttar citrat, ett centralt ämnesomsättningsintermediat, ur mitokondrierna till cytosolen där det används för ny fettsyntes. PRMT3 metylerar två specifika argininrester på SLC25A1, vilket gör transportören mer stabil och gynnar citratexport och fettbygge. När PRMT3 blockeras sjunker SLC25A1-nivåerna, citratexporten minskar och fettcellerna skiftar mot att bryta ner socker istället för att bilda mer fett. Hos möss på en fettrik kost minskar ett PRMT3-hämmande läkemedel kroppsfett, förbättrar blodsockerkontrollen och ökar ett mått kallat respiratoriskt utbyteskvot, vilket visar att djuren lättare övergår till att förbränna kolhydrater.
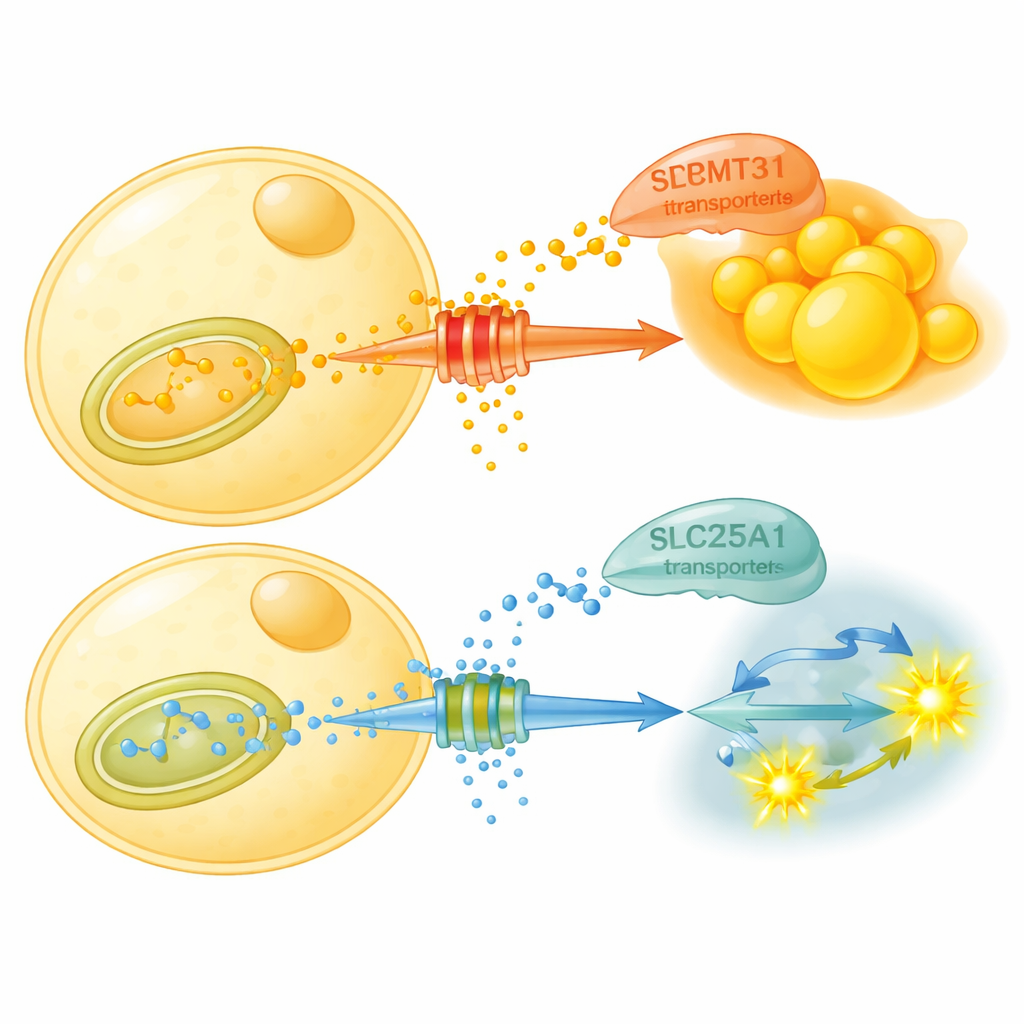
Fastescheman och genetiska justeringar pekar på samma väg
Forskarna undersökte sedan om vanliga fasteupplägg använder samma brytare. Under ett 16:8-schemapå tidsbegränsad ätning — 16 timmars fasta och 8 timmars ätande — gick mössen ner i vikt och hanterade glukos bättre utan att äta mindre totalt. Deras viscerala fett visade lägre nivåer av PRMT3, SLC25A1 och metylerade proteiner, och deras bränsleanvändning blev mer flexibel, särskilt på natten när de normalt äter. Anmärkningsvärt nog gav administration av det PRMT3-hämmande läkemedlet vid bestämda tidpunkter på dagen många av samma fördelar som 16:8-schemat. Genetisk borttagning av SLC25A1 enbart i fettceller skyddade också mössen från dietinducerad hyperglykemi och fettlever, återigen genom att öka sockernedbrytning och energianvändning i fettet, även utan att fettmassan krympte.
Vad detta betyder för framtida behandlingar
Tillsammans tyder fynden på att djupt bukfett innehåller en tidkänslig brytare, styrd av insulin, AKT, PRMT3 och SLC25A1, som avgör om våra kroppar förblir metaboliskt rörliga eller låses i ett lagringsläge. Tidsbegränsad ätning verkar peta denna brytare mot flexibilitet genom att sänka PRMT3 och dess downstream-effekter. Ett läkemedel som hämmar PRMT3 kan återskapa många av dessa fördelar hos överviktiga möss, vilket antyder ett framtida läkemedel som gör fastans metabola fördelar mer tillgängliga. För vardagsläsaren är budskapet att när vi äter, inte bara vad vi äter, kan omforma hur vår fettvävnad hanterar bränsle — med viktiga konsekvenser för vikt, blodsocker och långsiktig hälsa.
Citering: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Nyckelord: metabolisk flexibilitet, tidsbegränsad ätning, visceralt fett, proteinmetylering, glukosmetabolism