Clear Sky Science · sv
En DNA-baserad nanonhet känner av purinerg signalering och styr en immunomkopplare för att lösa inflammation
Att dämpa kroppens larmsystem
När våra vävnader skadas läcker celler ut en ström av kemiska ”larmsignaler” som kallar på immunceller för att bekämpa infektion och rensa bort skräp. Denna reaktion är livsviktig, men om larmet skräller för högt eller för länge kan det driva fram skadlig inflammation i lungor, njurar och andra organ. Denna studie beskriver en liten, programmerbar DNA-baserad enhet som kan känna när larmsignalen är för stark och tyst justera den, vilket hjälper immunsystemet att byta från attackläge till läkningsläge.
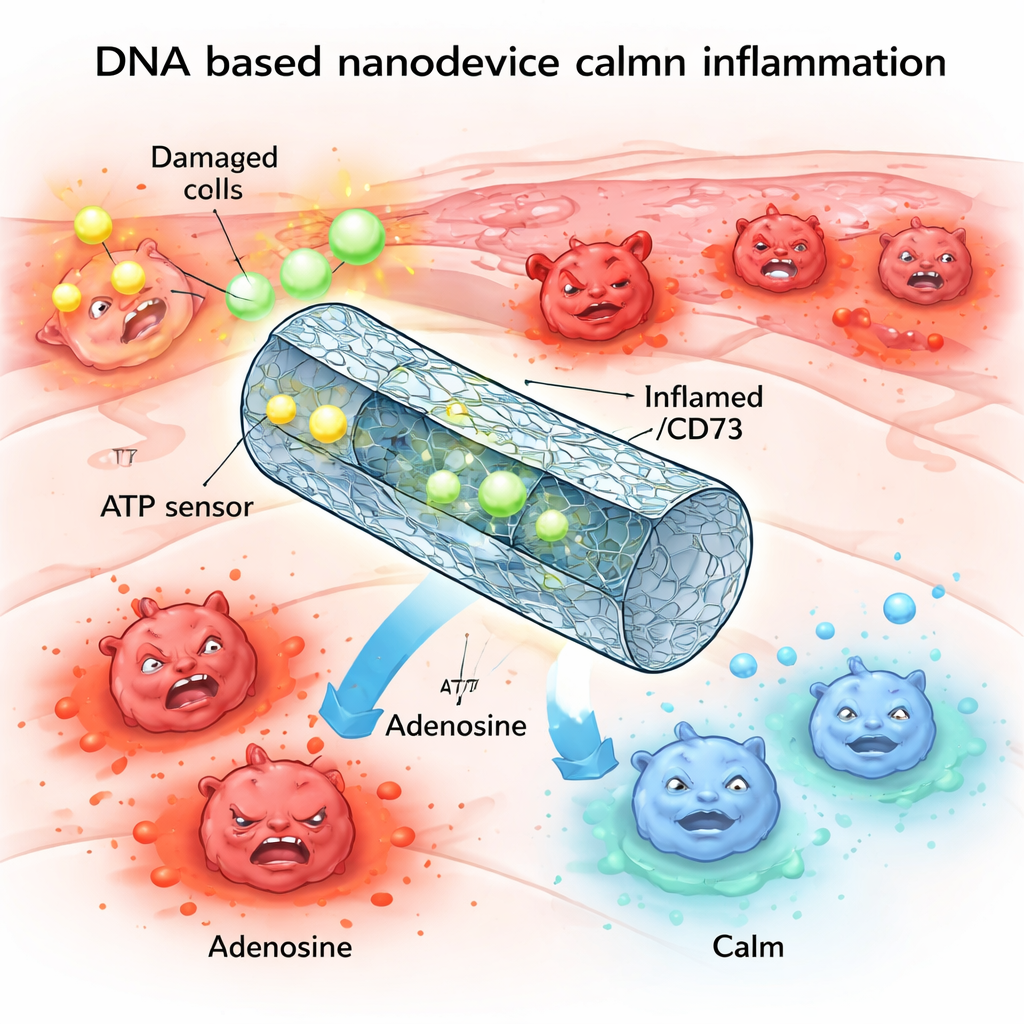
En kemisk signal som kan gå för långt
En av kroppens centrala larmsubstanser är ATP, bäst känd som cellernas ”energivaluta”. Vid skada eller stress läcker stora mängder ATP ut ur skadade celler och hamnar i den omgivande miljön. Där fungerar det extracellulära ATP som en nödsignal, binder till receptorer på immunceller och driver dem mot ett starkt inflammatoriskt tillstånd. Under normala förhållanden bryter enzymer på cellytor snabbt ner överskott av ATP till adenosin, ett närbesläktat ämne med lugnande, antiinflammatoriska effekter. Men i många kroniska eller svåra inflammatoriska sjukdomar är denna nedbrytningsmaskineri försämrad, vilket lämnar höga ATP-nivåer, lågt adenosin och vävnader fast i en skadlig cykel.
Bygga ett smart DNA-rör
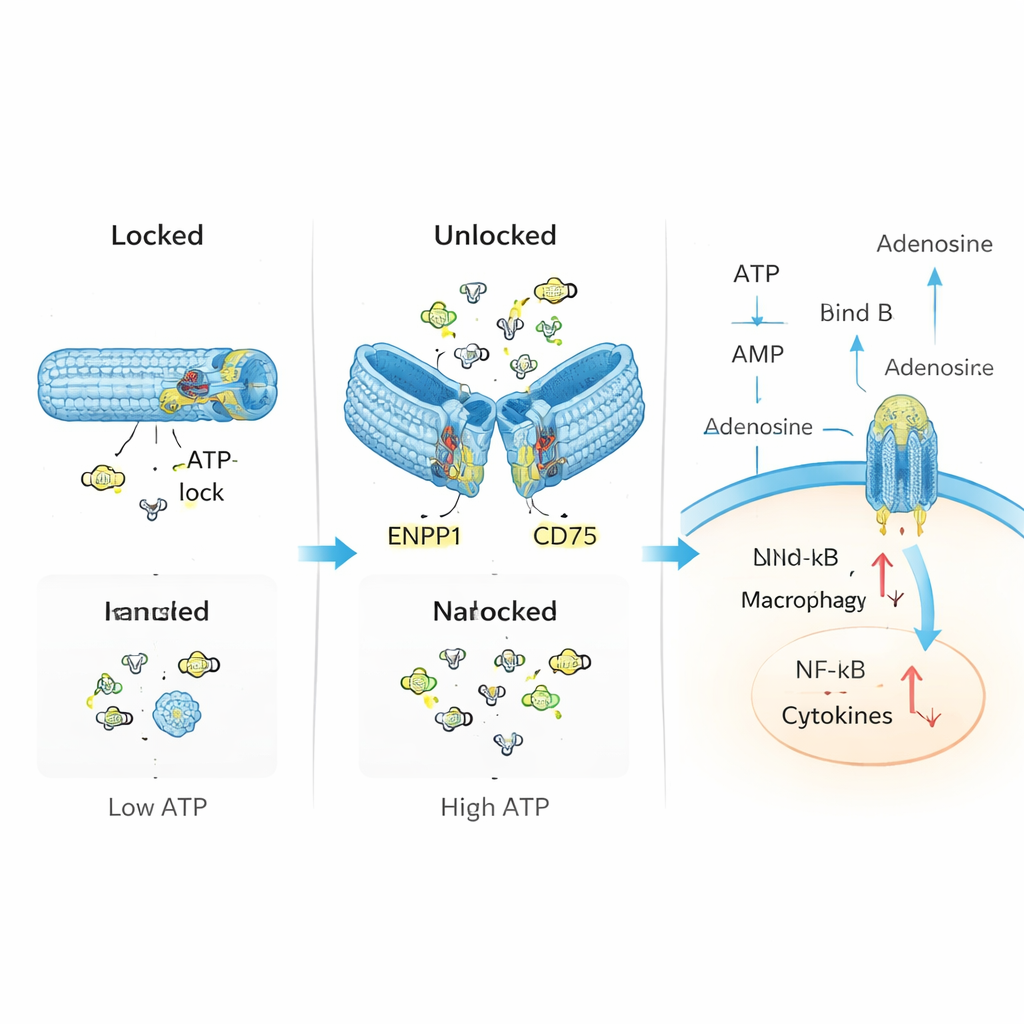
Forskarna ville imitera och reparera detta naturliga kontrollsystem med DNA-nanoteknik. De byggde ett ihåligt rör av DNA, vikt ungefär som origami, och utrustade det med två huvudkomponenter: ”sensorer” som känner igen ATP och enzymer som omvandlar ATP till adenosin. I viloläge hålls röret stängt av korta DNA-segment som också fungerar som ATP-sensorer. När ATP-nivåerna stiger över en viss tröskel, typisk för skadad vävnad, binder ATP till dessa segment, vilket får röret att öppnas och exponera enzymerna ENPP1 och CD73 inuti. Dessa bryter då ner överskottet av ATP och producerar adenosin, vilket försiktigt förskjuter den lokala kemiska balansen från fara mot upplösning.
Bevisa att omkopplaren fungerar
I kontrollerade laboratorietester bekräftade teamet att deras DNA-rör förblir stängt vid låga ATP-nivåer men pålitligt öppnas när ATP blir rikligt, ungefär som en nödventil. När det väl låsts upp omvandlar enheten stadigt ATP till mellanprodukter och slutligen till adenosin, utan märkbar skada på enzymernas aktivitet. I immunceller exponerade för högt ATP minskade denna nanonhet giftiga biprodukter i mitokondrier, sänkte aktiveringen av inflammatoriska vägar som NF-κB och NLRP3-inflammasomen, och ökade signaler kopplade till adenosins lugnande effekter. Med andra ord gjorde enheten mer än att bara suga upp ATP; den omprogrammerade aktivt cellernas beteende från inflammatoriskt till reglerande.
Hitchhiking till skadeställen
Att designa en smart omkopplare är en sak; att få den till rätt plats i kroppen är något annat. För att lösa leveransproblemet fäste forskarna sina DNA-rör på ytan av cirkulerande monocyter, en typ av vita blodkroppar som naturligt söker sig till inflammerad vävnad. Med en kolesterolkopplad DNA-ankare ”parkerade” de stora antal nanonheter på varje cells membran, där enheterna förblev mestadels på ytan snarare än att tas upp av cellen. I musmodeller för akut lung- och njurskada ackumulerades dessa dekorerade monocyter i skadade organ mycket effektivare än fritt flytande enheter, och nanonheterna svarade fortfarande specifikt på högt ATP i den skadade vävnaden.
Hjälpa vävnader att läka
I möss med kemiskt inducerad lung- eller njurskada minskade behandling med DNA-enheten vävnadsskada, uppbyggnad av immunceller och inflammatoriska budbärarmolekyler. Versionen som bars av monocyter fungerade bäst och gav starkare skydd än antingen den fria enheten eller enzymerna ensamma. Djupare genetiska och metaboliska analyser av lungvävnad visade att detta tillvägagångssätt inte bara dämpade inflammatoriska gener utan också hjälpte till att återställa rubbad energimetabolism i cellerna. Viktigt var att enheterna visade låg toksicitet och inte utlöste skadliga immunsvar hos friska djur.
Varför detta är viktigt för framtida terapier
För en icke-specialist är huvudbudskapet att detta arbete demonstrerar en programmerbar, molekylär ”termostat” för inflammation. Byggd av DNA och naturliga enzymer känner nanonheten när en farosignal är för stark och omvandlar den automatiskt till en lugnande signal, vilket hjälper immunceller att lägga ner vapnen och vävnader att reparera sig. Trots att strategin fortfarande är i ett tidigt, experimentellt stadium antyder den en ny klass av behandlingar som inte bara blockerar immunsignalering överallt utan istället lokalt återställer kemisk balans vid skadeställen, vilket potentiellt erbjuder precis kontroll över skadlig inflammation vid många sjukdomar.
Citering: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Nyckelord: DNA-nanonhet, extracellulärt ATP, inflammation, adenosin-signalering, nanomedicin